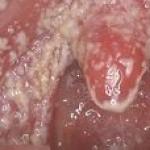
प्राथमिक इम्युनोडेफिशिएंसी क्या है। प्राथमिक इम्युनोडेफिशिएंसी
इम्यूनोलॉजी की धारा।
प्राथमिक (जन्मजात) इम्युनोडेफिशिएंसी
प्राथमिक इम्युनोडेफिशिएंसी की अवधारणा XX सदी के 60 के दशक में विकसित हुई, हालांकि कुछ वंशानुगत रोग प्रतिरक्षा तंत्रपहले वर्णित किया गया है। शुरू से ही, आनुवंशिक रूप से निर्धारित इम्युनोडेफिशिएंसी को "प्रकृति के प्रयोग" (आर। गुड) के रूप में माना जाता था, जिसके अध्ययन से प्रतिरक्षा तंत्र को समझने में मदद मिलती है। दरअसल, कई मामलों में, इम्युनोडेफिशिएंसी के आणविक आधार के विश्लेषण ने प्रतिरक्षा प्रणाली की संरचना और कामकाज के नए विवरणों को प्रकट करना संभव बना दिया, हालांकि, प्राथमिक इम्युनोडेफिशिएंसी के अंतर्निहित दोषों की प्रकृति को अक्सर प्रकटीकरण के बाद जाना जाता है। सामान्य प्रतिरक्षाविज्ञानी नियमितताओं की, जिसकी नैदानिक पुष्टि वे निकले।
प्राथमिक इम्युनोडेफिशिएंसी अत्यंत हैं दुर्लभ रोग... उनमें से अधिकांश का पता 10 5 -10 6 में 1 की आवृत्ति के साथ लगाया जाता है, कुछ - 10 4 में 1 की आवृत्ति के साथ। केवल चयनात्मक IgA की कमी के लिए 500-1000 में 1 की आवृत्ति परिभाषित की गई है। इस समूह की बीमारी मुख्य रूप से पाई जाती है बचपन, चूंकि कई रोगी 20 साल तक जीवित नहीं रहते हैं, और बाकी दोषों की कुछ हद तक भरपाई की जाती है। करने के लिए धन्यवाद सफल इलाजऊपरी आयु सीमा पहले की तुलना में अधिक विसरित पाई गई।
इन रोग संबंधी प्रतिक्रियाओं की विशेष गंभीरता के साथ-साथ महत्वपूर्ण वैज्ञानिक रुचि के कारण रोग का प्रत्येक विशिष्ट मामला प्रस्तुत करता है, प्राथमिक इम्युनोडेफिशिएंसीन केवल प्रतिरक्षाविज्ञानी का ध्यान आकर्षित करें। विश्व संगठनहेल्थकेयर समय-समय पर इस समस्या की स्थिति को दर्शाने वाली सामग्री प्रकाशित करता है।
लब्बोलुआब यह है कि लिम्फोसाइटों के बिना, लेकिन ल्यूकोसाइट्स और पूरक के पूर्ण संरक्षण के साथ, कोई प्रतिरक्षा प्रतिक्रिया नहीं होती है: अकेले, लिम्फोसाइटों के बिना, पूर्व-प्रतिरक्षा सेलुलर और हास्य प्रतिरोध के तंत्र वास्तविक, लगातार बदलते हुए का सामना नहीं कर सकते हैं संक्रामक सूक्ष्मजीवों और कीड़े, साथ ही कृत्रिम खाद्य योजक और दवाओं का सेट। नैदानिक लक्षणऔर पर्याप्त प्रयोगशाला परीक्षणएआर के विनाश और रिलीज के गैर-लिम्फोसाइटिक तंत्र के स्तर पर लिम्फोसाइटों और पैथोलॉजी के स्तर पर पैथोलॉजी को अलग करने की अनुमति दें।
सामान्य रूप से पीआईडी की घटना प्रति 10-100 हजार जीवित नवजात शिशुओं में 1 मामला है। चयनात्मक आईजीए की कमीबहुत अधिक बार होता है - सामान्य जनसंख्या के 500-1500 निवासियों में से 1।
पीआईडी में मुख्य नैदानिक दोष प्रतिरक्षा प्रणाली के मुख्य प्राकृतिक कार्य से मेल खाता है और इसमें संक्रामक रोग शामिल हैं। XX सदी की दूसरी छमाही की शुरुआत से पहले। चूंकि मानवता एंटीबायोटिक दवाओं के बिना रहती थी, संक्रमण से शिशु मृत्यु दर आम थी, और संक्रमण से उच्च शिशु मृत्यु दर की पृष्ठभूमि के खिलाफ, डॉक्टरों ने पीआईडी को अलग नहीं किया, और प्रतिरक्षा विज्ञान अविकसित था। केवल 1920 और 1930 के बीच। चिकित्सा साहित्य में रोगों का वर्णन पहली बार सामने आने लगा, जिसे बाद में पी.आई.डी. के रूप में समझा जाने लगा। पहली नोजोलॉजी की पहचान 1952 में अंग्रेजी चिकित्सक ब्रूटन ने की थी, जिन्होंने एक बीमार बच्चे के रक्त सीरम के वैद्युतकणसंचलन की खोज की थी। पूर्ण अनुपस्थितिजी-ग्लोबुलिन (यानी इम्युनोग्लोबुलिन)। इस बीमारी को ब्रूटन का एग्माग्लोबुलिनमिया कहा जाता है। बाद में यह स्पष्ट हो गया कि पैथोलॉजी एक्स क्रोमोसोम से जुड़ी हुई है, इसका आधुनिक नाम एक्स-लिंक्ड ब्रूटन का एग्माग्लोबुलिनमिया है।
प्राथमिक इम्युनोडेफिशिएंसी का वर्गीकरण:
1. एटी की कमी वाले सिंड्रोम।
2. टी-लिम्फोसाइटों की कमी वाले सिंड्रोम।
3. संयुक्त टी- और बी-कमियां।
4. पूरक घटकों की कमी वाले सिंड्रोम।
5. एनके में दोष वाले सिंड्रोम।
6. फागोसाइट दोष वाले सिंड्रोम।
7. आसंजन अणुओं में दोष वाले सिंड्रोम।
पीआईडी का मुख्य नैदानिक "चेहरा" तथाकथित संक्रामक सिंड्रोम है - सामान्य रूप से संक्रमण के लिए संवेदनशीलता में वृद्धि, संक्रामक रोगों का आवर्तक पाठ्यक्रम, असामान्य रूप से गंभीर नैदानिक पाठ्यक्रम, असामान्य रोगजनक (अक्सर अवसरवादी)। अधिकांश पीआईडी बचपन में प्रकट होते हैं। पीआईडी संदेह है यदि छोटा बच्चाबीमार संक्रामक रोगवर्ष में 10 से अधिक बार। पीआईडी वाले बच्चों में संक्रमण लगातार बना रह सकता है। आपको लैग इन पर ध्यान देना चाहिए आयु संकेतकविकासात्मक, आवर्तक साइनसिसिस, ओटिटिस मीडिया, निमोनिया, दस्त, कुअवशोषण, कैंडिडिआसिस। एक काल्पनिक परीक्षा के साथ, की अनुपस्थिति को प्रकट करना संभव है लसीकापर्व, टॉन्सिल।
यदि नैदानिक सबूत पीआईडी का सुझाव देते हैं, तो निम्नलिखित प्रयोगशाला परीक्षण किए जाते हैं:
1. एचआईवी संक्रमण के लिए विश्लेषण,
2. रक्त गणना का निर्धारण,
3.रक्त सीरम में IgG, IgA, IgM के स्तर का निर्धारण,
4. त्वचा परीक्षणसामान्य एआर के लिए एचआरटी (एआर टेटनस, डिप्थीरिया, स्ट्रेप्टोकोकल, ट्यूबरकुलिन, प्रोटीस मिराबिलिस, ट्राइकोफाइटन मेंटाग्रोफाइट्स, कैंडिडा अल्बिकन्स),
5.यदि आवश्यक हो - टी- और बी-लिम्फोसाइटों की उप-जनसंख्या की गणना,
6. विशेष नैदानिक संकेतों के लिए, पूरक घटकों की सामग्री के लिए विश्लेषण (सी 3 और सी 4 से शुरू),
7. विशेष संकेतों के लिए, फागोसाइट्स की स्थिति का विश्लेषण (सबसे सरल और सबसे जानकारीपूर्ण विश्लेषण टेराज़ोलियम ब्लू डाई की बहाली के लिए परीक्षण है),
8. आणविक आनुवंशिक अनुसंधान, यदि अर्थ (यानी जीन थेरेपी के लिए विशिष्ट संभावनाएं) और साधन हैं।
विश्लेषण एक बार में नहीं किया जाता है, लेकिन चरण दर चरण, जैसा कि डॉक्टर नाक विज्ञान को पहचानने में विफल रहता है या विफल रहता है। सभी विश्लेषण महंगे हैं, और यह "अनावश्यक" परीक्षण करने के लिए प्रथागत नहीं है।
इम्युनोग्लोबुलिन दोष के साथ प्राथमिक इम्युनोडेफिशिएंसी
एक्स-लिंक्ड ब्रूटन एग्माग्लोबुलिनमिया
जिन लड़कों की माताएँ दोषपूर्ण X गुणसूत्र की वाहक हैं, वे बीमार हैं। Defectan का X गुणसूत्र (Xq22) पर एक जीन है; एक बी-लिम्फोसाइट-विशिष्ट प्रोटीन टाइरोसिन किनेज (बीटीके के रूप में ब्रूटन के सम्मान में नामित) को एन्कोडिंग करना, टेस टाइरोसिन किनसे परिवार के सदस्यों के लिए समरूप।
प्रयोगशाला डेटा। कोई परिधीय बी-लिम्फोसाइट्स नहीं हैं। वी अस्थि मज्जासाइटोप्लाज्म में एम-श्रृंखला के साथ प्री-बी-कोशिकाएं होती हैं। आईजीएम और आईजीए सीरम में नहीं पाए जाते हैं, आईजीजी मौजूद हो सकता है, लेकिन पर्याप्त नहीं (40-100 मिलीग्राम / डीएल)। संबंधित Ar रक्त समूहों के प्रतिरक्षी के लिए विश्लेषण और Ar (टेटनस टॉक्सिन, डिप्थीरिया टॉक्सिन, आदि) के टीके के प्रति एंटीबॉडी उनकी अनुपस्थिति को दर्शाता है। टी-लिम्फोसाइट गिनती और टी-लिम्फोसाइट फ़ंक्शन परीक्षण सामान्य हैं।
नैदानिक तस्वीर। यदि कोई पारिवारिक इतिहास ज्ञात नहीं है, तो निदान औसतन 3.5 वर्ष की आयु में स्पष्ट होता है। रोग की विशेषता गंभीर पाइोजेनिक संक्रमण, ऊपरी (साइनसाइटिस, ओटिटिस मीडिया) और निचले (ब्रोंकाइटिस, निमोनिया) के संक्रमण से होती है। श्वसन तंत्र, गैस्ट्रोएंटेराइटिस, पायोडर्मा, सेप्टिक गठिया (बैक्टीरिया या क्लैमाइडियल), सेप्टिसीमिया, मेनिन्जाइटिस, एन्सेफलाइटिस हो सकता है। श्वसन पथ के संक्रमण अक्सर हीमोफिलस इन्फ्लुएंजा, स्ट्रेप्टोकोकस निमोनिया, स्टैफिलोकोकस ऑरियस के कारण होते हैं। दस्त आंतों के बैक्टीरिया या जिआर्डिया लैम्बिया के कारण होता है। विषाणु संक्रमणन्यूरोट्रोपिक वायरस ECHO-19 के साथ विशिष्ट संक्रमण, जो लगातार मेनिंगोएन्सेफलाइटिस का कारण बनता है। बीमार बच्चों में, जब जीवित पोलियोवासीन से प्रतिरक्षित किया जाता है, तो एक नियम के रूप में, श्लेष्मा झिल्ली के माध्यम से पोलियो विषाणु का लंबे समय तक निक्षालन होता है, और एक बहाल और बढ़ते हुए पौरुष के साथ (यानी, बच्चों के समूह में संक्रमण का एक वास्तविक खतरा होता है) पोलियो से ग्रसित स्वस्थ बच्चे, टीकाकृत प्रतिरक्षी कमी वाले बच्चे के संपर्क के परिणामस्वरूप)। ऐसे बच्चों की जांच करते समय विकास मंदता, अंगुलियों के आकार पर ध्यान दिया जाता है ड्रमस्टिक, आकार बदलता है छाती, निचले श्वसन पथ के रोगों के लिए विशिष्ट, लिम्फ नोड्स और टॉन्सिल के हाइपोप्लासिया। लसीकावत् ऊतक के ऊतकवैज्ञानिक परीक्षण में जर्मिनल केंद्रों और प्लाज्मा कोशिकाओं की अनुपस्थिति का पता चलता है।
1. रोगाणुरोधी कीमोथेरेपी।
2. प्रतिस्थापन चिकित्सा: जीवन के लिए हर 3-4 सप्ताह में दाता सीरम इम्युनोग्लोबुलिन की तैयारी का अंतःशिरा जलसेक। इम्युनोग्लोबुलिन की तैयारी की खुराक का चयन किया जाता है ताकि रोगी के सीरम में इम्युनोग्लोबुलिन की एकाग्रता बनाई जा सके जो ओवरलैप हो निम्न परिबंधआयु मानदंड।
3. अवसर आनुवंशिक चिकित्साचर्चा की जा रही है। बीटीके जीन का क्लोन बना लिया गया है, लेकिन इस बात के प्रमाण हैं कि इस जीन का हाइपरेक्स्रीशन हेमटोपोइएटिक ऊतक के घातक परिवर्तन से जुड़ा है।
हाइपरिममुनोग्लोबुलिनमिया सिंड्रोम के साथ एक्स-लिंक्ड एग्माग्लोबुलिनमिया एम
जिन लड़कों की माताएँ दोष की वाहक होती हैं वे लड़के बीमार होते हैं। आणविक दोष, कुछ हद तक संदेह के साथ, सीडी40-लगंडा जीन से संबंधित है। टी-लिम्फोसाइटों में सीडी40एल की अभिव्यक्ति की कमी से बी-लिम्फोसाइटों में इम्युनोग्लोबुलिन के वर्गों के संश्लेषण को एम से अन्य सभी आइसोटाइप में बदलने की असंभवता होती है।
प्रयोगशाला डेटा। IgG, IgA, IgE ज्ञानी नहीं हैं या उनमें से बहुत कम हैं। IgM स्तर बढ़ा हुआ है, यह काफी हो सकता है। एक नियम के रूप में, IgV पॉलीक्लोनल है, कभी-कभी मोनोक्लोनल। लिम्फोइड ऊतक में कोई रोगाणु केंद्र नहीं होते हैं, लेकिन प्लाज्मा कोशिकाएं होती हैं।
नैदानिक तस्वीर। आवर्तक जीवाणु और लचीले संक्रमण, जिसमें ऑप्पुटोनिक (न्यूमोकस्टिस कैरिनी) शामिल हैं। लाइफडेनोपैथी और स्प्लेनोमेगाली हो सकती है। समान नैदानिक तस्वीरविकृति विज्ञान के संभावित रूप से ऑटोसोमल प्रकार के वंशानुक्रम के लिए वर्णन करें, साथ ही उन बच्चों में विकृति विज्ञान के कुछ मामलों के लिए जो रूबेला वायरस के साथ अंतर्गर्भाशयी संक्रमण से गुजरे हैं।
इलाज। ब्रूटन के एग्माग्लोबुलिनमिया के उपचार के समान, अर्थात। रोगाणुरोधी कीमोथेरेपी और दाता सीरम इम्युनोग्लोबुलिन के नियमित आजीवन संक्रमण।
व्याख्यान का पूरा पाठ प्रस्तुत है स्लाइड्स पर।
4.2.1. पीआईडी वेरिएंट की नैदानिक और प्रतिरक्षाविज्ञानी विशेषताएं
वंशानुगत हाइपोगैमाग्लोबुलिनमिया (ब्रूटन रोग)
1) CD19 + लिम्फोसाइटों पर झिल्ली IgM / IgD रिसेप्टर्स (BCR) की उपस्थिति के साथ;
2) CD19 + झिल्लियों पर इन इम्युनोग्लोबुलिन की अभिव्यक्ति की अनुपस्थिति के साथ - लिम्फोसाइट्स
पहला विकल्प बी-लिम्फोसाइटों के प्लाज्मा कोशिकाओं में परिवर्तन के चरण में परिपक्व कोशिकाओं में भेदभाव में देरी से जुड़ा है। दूसरा विकल्प जीन में उत्परिवर्तन के कारण हो सकता है जो भारी श्रृंखलाओं के संश्लेषण को नियंत्रित करता है (गुणसूत्र 14 पर जीन का विलोपन)।
लड़कियों के रक्त में बी-लिम्फोसाइटों की अनुपस्थिति के कई मामलों का वर्णन किया गया है, लेकिन वे संभवतः एक्स-क्रोमोसोमल उत्परिवर्तन के लिए समयुग्मक थे, जिसे उन्होंने चिकित्सकीय रूप से प्रकट किया था।
सामान्य चर प्रतिरक्षा की कमी (अधिग्रहित हाइपोगैमाग्लोबुलिनमिया, वयस्क हाइपोगैमाग्लोबुलिनमिया)
डिस्म्यूनोग्लोबुलिनमिया की सबसे आम अभिव्यक्ति सामान्य चर प्रतिरक्षा कमी (सीवीआईडी) है। यह बी-लिम्फोसाइटों की प्लाज्मा कोशिकाओं में बदलने की क्षमता के उल्लंघन के कारण विकसित होता है। प्रयोगशाला निदान आईजीएम, आईजीजी, आईजीए की कुल सीरम एकाग्रता का पता लगाने पर आधारित है<300 мг%. В клинике чаще всего отмечаются рецидивирующие и хроническиемикробно-воспалительныепроцесы ЛОР-органов, глаз, легких, ЖКТ, гнойные поражения кожи. У детей с ОВИН не формируется специфический поствакцинальный иммунитет. У 1/3 больных отмечается сопутствующая анемия. Характерныгиперплазия лимфоузлов, кольца Пирогова-Вальдейера, увеличениеселезенки.ОВИН предрасполагает к аутоиммунным процессам. У взрослых больных с ОВИН часто развиваетсявосходящий холангит,желчекаменнаяболезнь, артриты и атопические процессы. Заболевание может манифестировать в разном возрасте (детском, подростковом или юношеском, средний возраст пациентов - 25 лет). Как правило, количествоВ-лимфоцитов в крови не снижено,но эти клетки не способны синтезировать иммуноглобулины какого-либо класса, чаще всегоIgG. Очень часто отмечается нарушение функционального состояния В-лимфоцитов. Предполагаются следующие механизмы развития ОВИН: поражениеCD19+-клеток, недостаточность функцийCD4+, дефицит цитокинов, отсутствие кооперации между Т- и В- лимфоцитами вследствие нарушения экспресссииCD40+. Предполагается полигенная природа заболевания. В основе патогенеза могут лежать дефекты одного или нескольких геновHLAIII.
उपवर्गों की कमी आईजीजी
4 ज्ञात IgG उपवर्ग हैं। आईडीएस प्रत्येक उपवर्ग की कमी के साथ विकसित होता है, लेकिन कुल आईजीजी का स्तर सामान्य है। प्रत्येक उपवर्ग के लिए विशिष्ट एंटीसेरा का उपयोग करके ही इस स्थिति का पता लगाया जा सकता है। चूंकि आईजीजी2 और आईजीजी4 स्रावित करने वाले बी-लिम्फोसाइटों के क्लोन की परिपक्वता जीवन के दूसरे वर्ष से पहले नहीं होती है, छोटे बच्चों में इन उपवर्गों की शारीरिक कमी होती है। प्राथमिक IDS वाले 50% रोगियों में IgG4 की कमी 13-20%, IgG2 की कमी होती है। अन्य उपवर्गों के एंटीबॉडी के गठन के कारण IgG1 की कमी को अक्सर चिकित्सकीय रूप से मुआवजा दिया जा सकता है। नैदानिक तस्वीर आवर्तक श्वसन पथ के संक्रमण का प्रभुत्व है।
चयनात्मक कमी पुलिस महानिरीक्षक ए
यह प्राथमिक आईडीएस के सबसे सामान्य रूपों में से एक है, जो 1: 100 - 1: 700 मामलों में होता है। इसी समय, रक्त सीरम में IgA सामग्री 5 mg% (0.05 g / l) से कम है। हास्य प्रतिरक्षा के अन्य संकेतक और सेलुलर प्रतिरक्षा की कार्यात्मक स्थिति बिगड़ा नहीं है। 4 विकल्प हैं:
1) नैदानिक अभिव्यक्तियों के बिना;
2) गतिभंग के साथ - टेलैंगिएक्टेसिया (लुई-बार सिंड्रोम);
3) बढ़े हुए आईजीएम संश्लेषण के साथ आईडीएस के संयोजन में;
4) गुणसूत्र उत्परिवर्तन के साथ संयोजन में।
क्लिनिक में, ईएनटी अंगों और ब्रोन्को-फुफ्फुसीय प्रणाली में सबसे अधिक बार पैथोलॉजिकल प्रक्रियाएं देखी जाती हैं। एक नियम के रूप में, IgA के प्लाज्मा और स्रावी स्तर दोनों घटते हैं, इसके दोनों उपवर्ग। जैसा कि आप जानते हैं, IgA पूरक प्रतिक्रियाओं के एक वैकल्पिक कैस्केड को सक्रिय करता है और इसमें जीवाणुनाशक गतिविधि होती है। स्राव में IgA की अनुपस्थिति या कमी में, ऊतक में एलर्जी और माइक्रोबियल एंटीजन की खुली पहुंच के लिए स्थितियां बनाई जाती हैं और प्रभावकारी कोशिकाओं के साथ उनका सीधा संपर्क देखा जाता है। चिकित्सकीय रूप से, यह एलर्जी और ऑटोइम्यून प्रतिक्रियाओं, डिस्बिओसिस और जठरांत्र संबंधी मार्ग की सूजन संबंधी बीमारियों से प्रकट होता है। IgG वर्ग से संबंधित IgA के प्रति एंटीबॉडी लगभग 40% रोगियों में पाए जाते हैं। प्रमुख दोष , चयनात्मक IDS IgA के विकास के कारण बी-लिम्फोसाइटों के बिगड़ा हुआ टर्मिनल विभेदन होता है। इसके अलावा, तथ्य यह है कि आईजीए गड़बड़ी एक मोनोजेनिक विशेषता के रूप में विरासत में मिली है, और इसकी नैदानिक अभिव्यक्तियाँ बहुरूपी हैं, एक भूमिका निभाती है। चयनात्मक IgA की कमी से तात्पर्य असंशोधित प्रतिरक्षा दोषों से है। CD3 + कोशिकाओं के कार्य बिगड़ा नहीं हैं। इन प्रक्रियाओं को विनियमित करने वाले साइटोकिन्स में आइसोटाइप स्विचिंग और दोषों में विसंगति का सुझाव दिया गया है।
I . के बढ़े हुए संश्लेषण के साथ प्रतिरक्षण क्षमता जीएम
IDS के इस रूप के साथ, IgM सामग्री 300 mg% (0.3 g / l) से अधिक और 3.0 से 10 g / l तक होती है, जबकि इम्युनोग्लोबुलिन के अन्य वर्ग आमतौर पर कम हो जाते हैं (IgG)<200 мг%,IgA<5 мг%).. Кроме повышенной чувствительности к инфекции у таких больных отмечается образование аутоантител к гранулоцитам, тромбоцитам, склонность к аутоиммунным заболеваниям. Наследуется по рецессивному типу. При этом синдроме отмечается низкая активностьCD4+- иCD19+- лимфоцитов у नवजात शिशु, यानी। दोष इम्युनोग्लोबुलिन के संश्लेषण को "वयस्क" प्रकार (आईजीजी की प्रबलता के साथ) में स्विच करने के उल्लंघन पर आधारित है। यह ध्यान में रखा जाना चाहिए कि आईजीएम में वृद्धि के साथ आईडीएस का एक एक्स-लिंक्ड रूप भी है, जो सीडी 40 एल के बिगड़ा संश्लेषण से जुड़ा है और संयुक्त आईडीएस से संबंधित है। ऑटोसोमल रूप के रोगजनन के केंद्र में साइटिडीन डेमिनमिनस जीन में एक दोष है, एक्स-लिंक्ड सीडी 40 जीन में उत्परिवर्तन के कारण टी कोशिकाओं की कमी है।
बच्चों में क्षणिक हाइपोगैमाग्लोबुलिनमिया
यह क्षणिक इम्युनोडेफिशिएंसी प्राथमिक आईडीएस का एक छोटा, सौम्य, लेकिन सामान्य रूप है। संक्षेप में, यह मातृ (प्लेसेंटल) आईजीजी के प्राकृतिक अपचय की अवधि के बाद अपने स्वयं के आईजीजी के संश्लेषण की शारीरिक शुरुआत में पिछड़ने का एक प्रकार है, जो जीवन के तीसरे महीने तक होता है, लेकिन इसका संश्लेषण सामान्य रूप से होना चाहिए 1 वर्ष में फिर से भरना। प्रयोगशाला निदान IgG . में कमी पर आधारित है<0,5 г/л, а такжеIgA<0,02 г/л иIgM<0,04 г/л. Характерны частые респираторные инфекции, патология ЛОР-органов, кожи, дисьактериоз ЖКТ. Транзиторная гипогаммаглобулинемия детского возраста проходит без лечения к 1,5-3 годам.
हाइपर . के साथ सिंड्रोम मैं जी इ - एमिया
1966 में वर्णित है। डेविस एट अल। जैसे जॉब सिंड्रोम (रोगी के नाम से)। यह जीवन के पहले महीनों में सामान्यीकृत एक्जिमाटस डर्मेटाइटिस के साथ पायोडर्मा के रूप में प्रकट होता है। 60-70% मरीज लड़के हैं। चेहरे, गर्दन, खोपड़ी की त्वचा प्रभावित होती है। राइनाइटिस और नेत्रश्लेष्मलाशोथ विशिष्ट हैं। त्वचा पर निशान, आसंजन, "ठंड" फोड़े बन जाते हैं। तेज खुजली होती है। रक्त में, ईोसिनोफिलिया, अक्सर - बाईं ओर एक बदलाव के साथ न्युट्रोफिलोसिस। आईजीई की संरचना में उच्च टाइटर्स में एंटीस्टाफिलोकोकल एंटीबॉडी होते हैं (इसलिए दूसरा नाम - आईजीई में वृद्धि के साथ स्टैफिलोकोकस ऑरियस सिंड्रोम)। आईजीजी में कमी है, ग्रैन्यूलोसाइट्स के केमोटैक्सिस में कमी, शायद हिस्टामाइन की उच्च सांद्रता के कारण, जो मस्तूल कोशिकाओं के सक्रियण पर जारी होती है। रोगी बड़ी संख्या में जहरीले ऑक्सीजन रेडिकल उत्पन्न करने में सक्षम होते हैं, जो चमड़े के नीचे के ऊतकों में ठंड के फोड़े के गठन से जुड़ा होता है। जॉब का सिंड्रोम एक ऑटोसोमल रिसेसिव तरीके से विरासत में मिला है।
टी-सेल प्रतिरक्षा की वंशानुगत और जन्मजात विकृतिटी कोशिकाओं की उनकी परिपक्वता के विभिन्न चरणों में प्रकट होता है - स्टेम सेल से लेकर विशेष उप-जनसंख्या के विकास तक।
लिम्फोसाइटिक डिसजेनेसिस (नेजेलोफ सिंड्रोम, फ्रेंच टाइप पीआईडी)
इस आईडीएस के लिए, इम्युनोग्लोबुलिन के सामान्य स्तर के साथ, टी-सेल प्रतिरक्षा की मात्रात्मक और कार्यात्मक अपर्याप्तता विशिष्ट है। 1964 में वर्णित है। नेज़ेलोफ़। यह एक ऑटोसोमल रिसेसिव तरीके से विरासत में मिला है और जीवन के पहले हफ्तों और महीनों में ही प्रकट होता है। एक विकासात्मक देरी होती है, त्वचा, फेफड़े, फंगल सेप्सिस में प्युलुलेंट फॉसी के साथ एक लंबी सेप्टिक प्रक्रिया अक्सर विकसित होती है। थाइमस और लिम्फ नोड्स का हाइपोप्लासिया व्यक्त किया जाता है। रक्त में - CD3 + लिम्फोसाइटों का एक अत्यंत निम्न स्तर, RBTL और HRT में कम प्रतिक्रिया, CD16 + कोशिकाओं के कार्य में कमी। सबसे अधिक बार, रोग का निदान खराब है।
थाइमस और पैराथायरायड ग्रंथियों का हाइपोप्लासिया ( सी इंड्रोम डि-जॉर्जी)
1965 में लेखक द्वारा वर्णित। यह थाइमस ग्रंथि के अप्लासिया, थायरॉयड और पैराथायरायड ग्रंथियों के अविकसितता की विशेषता है। जो तीसरे और चौथे ग्रसनी जेब के क्षेत्र में उपकला के भ्रूण भेदभाव में एक दोष से जुड़े हैं। अधिक बार लड़कियां बीमार होती हैं। यह जीवन के पहले दिनों से ही दौरे (Ca ++ में कमी के कारण), श्वसन पथ के संक्रमण और पाचन विकारों के रूप में प्रकट होता है। इसे अक्सर बड़े जहाजों और हृदय (सामान्य धमनी रक्त प्रवाह, डबल महाधमनी चाप, डेक्स्ट्रोकार्डिया, आदि) के विकृतियों के साथ जोड़ा जाता है। इम्युनोग्राम नेसेलोफ सिंड्रोम के समान है। संक्रामक प्रतिजनों का स्पेक्ट्रम जो रोग प्रक्रियाओं का कारण बनता है, वायरस, माइकोबैक्टीरियम ट्यूबरकुलोसिस, कवक और कुछ बैक्टीरिया का प्रभुत्व है।
संयुक्त इम्युनोडेफिशिएंसी
वंशानुगत लिम्फोसाइटोफथिसिस (स्विस प्रकार पीआईडी)
यह जीवन के पहले महीनों में ही प्रकट होता है: वजन बढ़ने में देरी, एनोरेक्सिया, खसरा जैसे चकत्ते, थ्रश, त्वचीय कैंडिडिआसिस, बीचवाला निमोनिया, वायरल संक्रमण (चिकनपॉक्स, सीएमवी, आदि)। यह एक ऑटोसोमल रिसेसिव तरीके से या सेक्स से जुड़े लक्षण (75% - लड़के) के रूप में विरासत में मिला है। यह सीडी 3 + - की संख्या में कमी की विशेषता है। कुछ हद तक CD19 + लिम्फोसाइट्स बिगड़ा हुआ कार्यात्मक गतिविधि के साथ। लिम्फोइड ऊतक के हाइपोप्लासिया का उल्लेख किया गया है। कुछ बच्चों में थाइमिक दोष होता है, कुछ मामलों में सीडी 3 + लिम्फोसाइट्स एचएलए एंटीजन I और II - "नग्न लिम्फोसाइट सिंड्रोम" को व्यक्त नहीं करते हैं। HLAII (DR, DQ, DP) की अनुपस्थिति में, malabsorption syndrome (malabsorption) के साथ एक संयोजन विशेषता है।
थायमोमा के साथ पीआईडी (हूड सिंड्रोम)
यह स्ट्रोमा, लिम्फोसाइटोपेनिया, रक्त में इम्युनोग्लोबुलिन के निम्न स्तर के अतिवृद्धि के कारण थाइमिक हाइपरप्लासिया की विशेषता है। थाइमस के विकास में गिरफ्तारी से थायमोमा के साथ आईडीएस का निर्माण होता है, जो कि सीडी 3 + और सीडी 19 + लिम्फोसाइटों की कमी के संयोजन की विशेषता है। यह माना जाता है कि मुख्य दोष स्टेम सेल भेदभाव के शुरुआती चरणों में ही प्रकट होता है। यह अस्थि मज्जा और अप्लास्टिक एनीमिया में एरिथ्रोब्लास्ट की सहवर्ती कमी से प्रकट होता है। इस सिंड्रोम की विरासत पर रोगजनक तंत्र और डेटा का अभी तक पर्याप्त अध्ययन नहीं किया गया है।
विस्कॉट-एल्ड्रिच सिंड्रोम
1937 में पारिवारिक एक्स-लिंक्ड सिंड्रोम (लड़कों में) के रूप में वर्णित। यह खुद को लक्षणों की एक त्रय के रूप में प्रकट करता है: 1) श्वसन प्रणाली और ईएनटी अंगों के आवर्तक और पुराने संक्रमण की प्रवृत्ति, 2) थ्रोम्बोसाइटोपेनिया के कारण रक्तस्रावी सिंड्रोम, 3) एक्जिमा के साथ एटोपिक जिल्द की सूजन। यह नवजात काल से ही प्रकट होता है। थाइमस हाइपोफंक्शन, हीमोग्लोबिन और एरिथ्रोसाइट्स में कमी, ईोसिनोफिलिया, प्लेटलेट्स में कमी और दोष (बिगड़ा हुआ आसंजन, एकत्रीकरण, एटीपी सामग्री में कमी) नोट किया जाता है। पेटीचिया, श्लेष्मा झिल्ली से रक्तस्राव की विशेषता है। त्वचा के घाव लगातार और आवर्तक होते हैं। इम्युनोग्राम में, आईजीएम अक्सर सामान्य आईजीजी स्तर, आईजीए और आईजीई में वृद्धि के साथ घटता है। दोष का आधार लिम्फोसाइटों की कोशिका झिल्ली की संरचना का उल्लंघन है। रोग का निदान अक्सर प्रतिकूल होता है: बच्चे संक्रमण और डिस्ट्रोफी से मर जाते हैं।
घाटा आईजी ऐ गतिभंग-telangiectasias (लुई-बार सिंड्रोम) के साथ संयोजन में
श्वेतपटल और चेहरे के जहाजों के टेलैंगिएक्टेसिया के साथ गतिभंग और अन्य न्यूरोलॉजिकल असामान्यताओं की उपस्थिति, प्रतिरक्षाविज्ञानी दोषों के साथ संयोजन में नोट की जाती है। सेरिबैलम (इसके बाद के शोष के साथ) के कार्य में घाव होते हैं, साथ ही साथ सबकोर्टिकल गैन्ग्लिया, सेरेब्रल कॉर्टेक्स के डाइएनसेफेलिक क्षेत्र, और इसके कारण, पिरामिड संबंधी विकार अक्सर पाए जाते हैं। चाल की गड़बड़ी, धीमी स्वैच्छिक गतिविधियों, हाइपरकिनेसिस, पार्किंसनिज़्म सिंड्रोम और वनस्पति-संवहनी विकारों द्वारा विशेषता। सुस्त निमोनिया अक्सर नोट किया जाता है, जो एटलेक्टासिस, न्यूमोस्क्लेरोसिस और ब्रोन्किइक्टेसिस के विकास में समाप्त होता है। रोगी शारीरिक विकास में पिछड़ जाता है। थाइमस, लिम्फ नोड्स और प्लीहा, आंतों के लसीका तंत्र के हाइपोप्लेसिया का पता चला। इम्युनोग्राम इम्युनोग्लोबुलिन के लिए एफसी-रिसेप्टर्स के साथ बी-लिम्फोसाइटों में कमी, आरबीटीएल में कम प्रतिक्रिया और आईजीए की अनुपस्थिति को दर्शाता है। रोग को वंशानुक्रम के एक ऑटोसोमल रिसेसिव मोड की विशेषता है। मरीजों में सहज क्रोमोसोमल ब्रेक, क्रोमोसोम 7 और 14 में पुनर्व्यवस्था और डीएनए मरम्मत तंत्र का उल्लंघन होता है। पूर्वानुमान प्रतिकूल है।
असफलता इल -2
1983 में वर्णित है। साथ ही, लिम्फोसाइटों के सामान्य स्तर पर PHA और ConA पर कोई प्रोलिफ़ेरेटिव प्रक्रिया नहीं होती है। यह IL-2 की कमी के कारण कोशिकाओं की प्रोलिफ़ेरेटिव गतिविधि के उल्लंघन का संकेत देता है।
असफलता एनके (एसडी 16)
एनके कोशिकाएं एंटीट्यूमर इम्युनिटी के साथ-साथ इंट्रासेल्युलर रोगजनकों की दृढ़ता के लिए प्रतिरोध प्रदान करती हैं। वे -इंटरफेरॉन और IL-2 द्वारा सक्रिय होते हैं। यह कमी चेडियाक-हिगाशी सिंड्रोम में पाई जाती है।
डंकन की बीमारी
यह एक्स-लिंक्ड आईडीएस एपस्टीन-बार वायरस के प्रति संवेदनशीलता में वृद्धि की विशेषता है। जिन लड़कों को संक्रामक मोनोन्यूक्लिओसिस हुआ है, उनमें लंबे समय तक बुखार, लिम्फैडेनोपैथी, लिम्फोसाइटोसिस और यकृत और प्लीहा का बढ़ना विकसित होता है। इम्युनोग्लोबुलिन की सामग्री कम हो जाती है या डिस्म्यूनोग्लोबुलिनमिया मनाया जाता है। लिम्फोप्रोलिफेरेटिव प्रक्रिया का अक्सर घातक परिणाम होता है, जो छोटी आंत के टर्मिनल वर्गों में प्रमुख स्थानीयकरण के साथ-साथ यकृत परिगलन के कारण लिम्फोमा के गठन के कारण होता है।
पूरक प्रणाली की अपर्याप्तता (सी)
पूरक प्रणाली शरीर की प्रतिरक्षा प्रतिक्रियाओं के दौरान विशिष्ट सुरक्षा में वृद्धि प्रदान करती है। इसकी सक्रियता से प्रत्यक्ष कोशिका लसीका होता है और फागोसाइटिक गतिविधि की उत्तेजना होती है। सक्रियण प्रक्रिया सीमित प्रोटियोलिसिस के एंजाइम सिस्टम के कारण होती है।
पूरक प्रणाली को सक्रिय करने का शास्त्रीय तरीका प्रतिरक्षा परिसरों के निर्माण में अपनी भागीदारी सुनिश्चित करता है, जिसमें आईजीएम, आईजीजी 1, 2, 3, हेजमैन कारक का एक टुकड़ा, प्रोटीनएमाइक्रोऑर्गेनिज्म, सीआरपी कॉम्प्लेक्स (उदाहरण के लिए, डीएनए अणु के साथ), कुछ शामिल हो सकते हैं। वायरस से प्रभावित वायरस और कोशिकाएं। सामान्य तौर पर, इस मार्ग का उद्देश्य प्रतिरक्षा साइटोलिसिस को बढ़ाना है।
फागोसाइटोसिस की कमी
कोस्टमैन सिंड्रोम .
1956 में वर्णित है। यह त्वचा और खोपड़ी, निमोनिया, ऑस्टियोमाइलाइटिस, सेप्सिस के आवर्तक जीवाणु संक्रमण द्वारा बचपन में ही प्रकट होता है। यह न्यूट्रोपेनिया, मोनोसाइटोसिस, ईोसिनोफिलिया और एनीमिया की विशेषता है। अस्थि मज्जा में, मायलोसाइट्स की देरी से परिपक्वता के संकेत हैं। यह कुछ अन्य जन्मजात न्यूट्रोपेनिया (ईोसिनोफिलिया के साथ न्यूट्रोपेनिया, चेडियाक-हिगाशी सिंड्रोम, फैंकोनी पैन्टीटोपेनिया) की तरह एक ऑटोसोमल रिसेसिव तरीके से विरासत में मिला है।
चेडियाक-हिगाशी सिंड्रोम।
1952 में वर्णित है। त्वचा, बालों और आंखों के आंशिक ऐल्बिनिज़म, ज्वर की स्थिति, पैन्टीटोपेनिया, संक्रामक और भड़काऊ रोगों की प्रवृत्ति, न्यूरोपैथी की अभिव्यक्तियों के संयोजन द्वारा विशेषता। श्वसन पथ के श्लेष्म झिल्ली और त्वचा पर सूजन प्रक्रियाएं अक्सर स्टैफिलोकोकस ऑरियस या अन्य ग्राम-पॉजिटिव बैक्टीरिया के कारण होती हैं। यह ध्यान दिया जाता है कि हेपेटो-स्प्लेनोमेगाली, त्वचा के रक्तस्राव (थ्रोम्बोसाइटोपेनिया) दिखाई देते हैं, और एक सेप्टिक स्थिति बनती है। अधिकांश रोगी 10 वर्ष की आयु तक जीवित नहीं रहते हैं।
उद्धरण के लिए:रेजनिक आई.बी. आनुवंशिक प्रकृति की प्रतिरक्षा स्थितियाँ: समस्या पर एक नया रूप // RMZH। 1998. नंबर 9। पी. 3
अब यह स्पष्ट हो रहा है कि प्राथमिक इम्युनोडेफिशिएंसी उतनी दुर्लभ स्थिति नहीं है जितनी आमतौर पर मानी जाती थी। हालांकि, नैदानिक विधियों में प्रगति के बावजूद, 70% से अधिक रोगियों में इम्यूनोडिफ़िशिएंसी अवस्था का निदान नहीं किया जाता है। लेख प्राथमिक इम्युनोडेफिशिएंसी के निदान के लिए नैदानिक मानदंड और प्राथमिक प्रयोगशाला विधियों का एक पैनल प्रस्तुत करता है। आजकल, यह स्पष्ट हो जाता है कि प्राथमिक इम्युनोडेफिशिएंसी ऐसी दुर्लभ स्थिति नहीं है जैसा कि पहले माना जाता था। हालांकि, नैदानिक प्रगति के बावजूद, 70% से अधिक रोगियों में इम्युनोडेफिशिएंसी का निदान नहीं किया जाता है। कागज नैदानिक मानदंड और प्राथमिक इम्युनोडेफिशिएंसी के लिए प्राथमिक प्रयोगशाला नैदानिक परखों का एक पैनल देता है। आई.बी. रेज़निक क्लिनिकल इम्यूनोलॉजी विभाग के प्रमुख, बाल चिकित्सा अनुसंधान संस्थान, रूस के स्वास्थ्य मंत्रालय, चिकित्सा विज्ञान के डॉक्टर, रूसी राज्य चिकित्सा विश्वविद्यालय के प्रोफेसर।
आईबी रेजनिक, एमडी, प्रमुख, क्लिनिकल इम्यूनोलॉजी विभाग, बाल चिकित्सा अनुसंधान संस्थान, रूसी संघ के स्वास्थ्य मंत्रालय; प्रोफेसर, रूसी राज्य चिकित्सा विश्वविद्यालय।
परिचय
विकास की अंतर्गर्भाशयी अवधि के दौरान गर्भावस्था के सामान्य पाठ्यक्रम के दौरान, बच्चा बाँझ परिस्थितियों में होता है। जन्म के तुरंत बाद, यह सूक्ष्मजीवों के साथ उपनिवेश करना शुरू कर देता है। चूंकि मुख्य माइक्रोफ्लोरा रोगजनक नहीं है, इस उपनिवेश से बीमारी नहीं होती है। इसके बाद, रोगजनक सूक्ष्मजीवों का संपर्क, जो बच्चे को नहीं मिला है, इसी संक्रामक रोग के विकास का कारण बनता है। रोगज़नक़ के साथ प्रत्येक संपर्क प्रतिरक्षाविज्ञानी स्मृति के विस्तार की ओर जाता है और दीर्घकालिक प्रतिरक्षा बनाता है।
प्रतिरक्षा प्रणाली के चार मुख्य घटक व्यक्ति को वायरस, बैक्टीरिया, कवक और प्रोटोजोआ से लगातार हमलों से बचाने में शामिल होते हैं जो संक्रामक रोगों का कारण बन सकते हैं। इन घटकों में एंटीबॉडी-मध्यस्थता, या बी-सेल, प्रतिरक्षा, टी-सेल प्रतिरक्षा, फागोसाइटोसिस और पूरक प्रणाली शामिल हैं। इनमें से प्रत्येक प्रणाली स्वतंत्र रूप से काम कर सकती है, लेकिन आमतौर पर प्रतिरक्षा प्रतिक्रिया में प्रतिरक्षा प्रणाली के घटकों के बीच बातचीत शामिल होती है।
अंतर्जात, आमतौर पर प्रतिरक्षा प्रणाली के घटकों में से एक के आनुवंशिक रूप से निर्धारित दोष शरीर की रक्षा प्रणाली के उल्लंघन की ओर ले जाते हैं और चिकित्सकीय रूप से प्राथमिक इम्युनोडेफिशिएंसी स्टेट (पीआईडी) के रूपों में से एक के रूप में पाए जाते हैं। चूंकि कई प्रकार की कोशिकाएं और सैकड़ों अणु प्रतिरक्षा प्रणाली के सामान्य कामकाज और प्रतिरक्षा प्रतिक्रिया में शामिल होते हैं, इसलिए कई प्रकार के दोष पीआईडी के अंतर्गत आते हैं। डब्ल्यूएचओ वैज्ञानिक समूह, जो हर 2 साल में पीआईडी समस्या पर रिपोर्ट प्रकाशित करता है, नवीनतम रिपोर्ट में पीआईडी के 70 से अधिक पहचाने गए दोषों पर प्रकाश डाला गया है, जबकि 2 साल पहले उनकी संख्या 50 थी, और 4 साल पहले - केवल 17। पीआईडी के उदाहरण तालिका में दिए गए हैं ... 1.
हाल ही में, आणविक दोषों की खोज के संबंध में, जो कई इम्युनोडेफिशिएंसी से गुजरते हैं, और नैदानिक तस्वीर की महत्वपूर्ण परिवर्तनशीलता और पीआईडी के पाठ्यक्रम की गंभीरता, वयस्कों सहित उनके देर से प्रकट होने की संभावना के बारे में जागरूकता, यह स्पष्ट हो जाता है कि पीआईडी ऐसी दुर्लभ स्थिति नहीं है जैसा कि अब तक माना जाता था। पीआईडी के एक महत्वपूर्ण हिस्से के लिए, आवृत्ति 1/25,000 - 1/100,000 है, हालांकि जन्मजात प्रतिरक्षा दोषों के वेरिएंट, जैसे चयनात्मक IgA की कमी, 1 / 500-1 / 700 लोगों की आवृत्ति के साथ सफेद दौड़ में होते हैं। पीआईडी का समग्र प्रसार अज्ञात है, हालांकि, इम्यून डेफिसिएंसी फाउंडेशन - आईडीएफ (यूएसए) के अनुमानों के अनुसार, यह आंकड़ा सिस्टिक फाइब्रोसिस की घटनाओं से 4 गुना अधिक है।
|
प्रयोगशाला निदान आधुनिक चिकित्सा की मुख्य उपलब्धियों में से एक निदान और उपचार में नए सेलुलर, इम्यूनोकेमिकल और आणविक तरीकों का बहुत तेजी से परिचय है। साथ ही, नैदानिक प्रक्रियाओं पर बहुत अधिक आवश्यकताएं लगाई जाती हैं और गैर-मानकीकृत (वैश्विक स्तर पर) विधियों के उपयोग की केवल एक या कई प्रयोगशालाओं में प्रतिलिपि प्रस्तुत करने की अनुमति नहीं है। तो, एक अध्ययन का परिणाम, जिसमें "टी-लिम्फोसाइट्स", "बी-लिम्फोसाइट्स", "टी-हेल्पर्स", "टी-सप्रेसर्स" और इसी तरह दिखाई देते हैं, सिद्धांत रूप में अपठनीय है, क्योंकि इसे समझना असंभव है उदाहरण के लिए, "शमन टी" की तरह सेल को किस मानदंड के आधार पर निर्धारित किया गया था। इसके अलावा, यह ध्यान में रखा जाना चाहिए कि एक ही कोशिका प्रतिरक्षा प्रतिक्रिया के एक प्रकार को बाधित कर सकती है (एक शमन कार्य कर सकती है) और दूसरा संस्करण (सहायक कार्य) शुरू कर सकती है। इसलिए, मानक तरीकों के परिणामों के आधार पर भी प्रतिरक्षा के शमन या सहायक लिंक की अपर्याप्तता के बारे में अक्सर सामने आने वाले निष्कर्ष, जैसे कि एंटी-लिम्फोसाइटिक एंटीबॉडी के उपयोग, कई मामलों में निराधार हैं। आणविक तंत्र पिछले 5 वर्षों (1993 - 1997) को प्राथमिक इम्युनोडेफिशिएंसी राज्यों में आणविक दोषों के सक्रिय और सफल पता लगाने की विशेषता रही है। विभिन्न यूरोपीय देशों और संयुक्त राज्य अमेरिका में केंद्रों के नेटवर्क की घनिष्ठ बातचीत, व्यक्तिगत केंद्रों की रूपरेखा और संचार के आधुनिक साधनों के बारे में खुली जानकारी अब 90-95% से अधिक मामलों में एक इम्युनोडेफिशिएंसी राज्य के प्रकार को स्पष्ट करना संभव बनाती है। . यह अंतःक्रिया क्या देती है? आणविक निदान ने एक असामान्य, आमतौर पर हल्के पाठ्यक्रम के साथ रोगों के रूपों के अस्तित्व का प्रदर्शन किया है (उदाहरण के लिए, देर से शुरुआत के साथ एक्स-लिंक्ड एग्माग्लोबुलिनमिया, इम्युनोग्लोबुलिन के स्तर में मामूली कमी, 1 - 2% β-लिम्फोसाइट्स की उपस्थिति। परिधीय रक्त)। ऐसे मामलों में सटीक निदान का ज्ञान आवश्यक चिकित्सा आहार का सही विकल्प निर्धारित करता है। आणविक निदान का स्पष्टीकरण, कुछ हद तक, एक व्यक्तिगत पूर्वानुमान के निर्माण में उपयोगी हो सकता है। उदाहरण के लिए, ऐसा लगता है कि विस्कॉट-एल्ड्रिच सिंड्रोम प्रोटीन को कूटने वाले WASP जीन के एक्सॉन 2 में गलत उत्परिवर्तन रोग के एक हल्के और अधिक अनुकूल रूप से अधिक अनुकूल पाठ्यक्रम से जुड़े हैं। आणविक दोष के ज्ञान के आधार पर आनुवंशिक परामर्श, जांच के रिश्तेदारों के बीच पुनरावर्ती जीन के वाहक की पहचान की अनुमति देता है। पीआईडी का प्रसव पूर्व निदान संभव हो जाता है, जो विशेष रूप से इम्यूनोडिफ़िशिएंसी के बोझ से दबे परिवारों में बार-बार गर्भधारण के मामले में महत्वपूर्ण है। जीन थेरेपी की संभावनाओं पर नीचे चर्चा की जाएगी। इसके अलावा, इम्युनोडेफिशिएंसी राज्यों के अध्ययन के लिए आणविक आनुवंशिक दृष्टिकोण मानव प्रतिरक्षा प्रणाली के शरीर विज्ञान के बारे में अपूरणीय सैद्धांतिक जानकारी प्राप्त करने की अनुमति देता है, क्योंकि कई प्रयोगशाला मॉडल, उदाहरण के लिए, एक नष्ट ("नॉक आउट") जीन वाले जानवर, अक्सर फेनोटाइपिक रूप से संबंधित मानव फेनोटाइप के साथ मेल नहीं खाते हैं। सीरम इम्युनोग्लोबुलिन: * आईजीजी * आईजीएम * आईजीए विशिष्ट (पोस्टवाजियल) एंटीबॉडी के स्तर त्वचा परीक्षण एचआरटी एक्स-लिंक्ड एग्माग्लोबुलिनमिया सामान्य चर प्रतिरक्षाविज्ञानी कमी हाइपर-आईजीएम सिंड्रोम चयनात्मक आईजीए की कमी गंभीर संयुक्त इम्युनोडेफिशिएंसी विस्कॉट-ओरेंड्रिच सिंड्रोम इस प्रकार के सबसे व्यापक उपचार की अनुमति देता है। न्यूट्रीएंसी पीआईडी। आगे के निदान से बीमारियों की एक और श्रृंखला की पहचान करना या प्रारंभिक निदान को स्पष्ट करना संभव हो जाता है। यदि एक नैदानिक रूप से मनाया गया इम्यूनोडिफ़िशिएंसी राज्य की प्रयोगशाला की पुष्टि नहीं की जा सकती है, तो यह सलाह दी जाती है कि प्रतिरक्षा के जन्मजात दोषों के क्षेत्र में विशेषज्ञता वाले केंद्रों में अनुसंधान किया जाए और अंतरराष्ट्रीय नेटवर्क में शामिल किया जाए। इस मामले में, नैदानिक निदान "अनिर्दिष्ट पीआईडी" योग्य है, यदि इसके आधार पर, डॉक्टर सही ढंग से रोग का निदान निर्धारित करता है और चिकित्सा निर्धारित करता है। पीआईडी चिकित्सा के लिए उत्तरदायी हैं, जिसका लक्ष्य रोग की सीमाओं को कम करना और रोगी को वयस्कता में उत्पादक जीवन जीने में सक्षम बनाना है। रोगों के इस समूह की रोगजनक, नैदानिक और रोगसूचक परिवर्तनशीलता उनके उपचार को काफी कठिन बना देती है; चिकित्सा की पसंद, एक नियम के रूप में, रोगी की स्थिति के आकलन पर इतना आधारित नहीं है जितना कि संचयी विश्व अनुभव पर, रोग के पाठ्यक्रम और परिणाम पर उपचार के कुछ तरीकों के प्रभाव पर विश्व डेटा में जमा होता है। निष्कर्ष जैसा कि ऊपर से देखा जा सकता है, आधुनिक चिकित्सा प्रतिरक्षा प्रणाली के जन्मजात दोषों वाले रोगियों के उपचार के अवसर प्रदान करती है। नई प्रौद्योगिकियों की शुरूआत की गति सबसे गंभीर प्रकार की प्रतिरक्षाविहीनता वाले रोगियों को भी निराशाजनक मानने की अनुमति नहीं देती है। हमारे देश में आणविक निदान और आनुवंशिक परामर्श उपलब्ध हो गए हैं, और एक अंतरराष्ट्रीय नेटवर्क में केंद्रों को शामिल करने से उनमें से प्रत्येक की क्षमताओं का विस्तार होता है। इसके अलावा, संचार के आधुनिक साधनों का उपयोग पत्राचार परामर्श और डीएनए जैसे जैविक सामग्री के आदान-प्रदान को उपलब्ध कराता है। इसी समय, अप्रत्यक्ष गणना के अनुसार (देखें "परिचय"), पीआईडी के रोगियों के 70% से अधिक (!) का निदान नहीं किया जाता है, और वे सेप्टिक, ऑन्कोलॉजिकल, न्यूरोलॉजिकल, ऑटोइम्यून या अन्य बीमारियों से मर जाते हैं। एक विशेष केंद्र में निदान के बाद के स्पष्टीकरण के साथ क्षेत्रीय और बड़े शहर के अस्पतालों के स्तर पर उपलब्ध प्राथमिक प्रयोगशाला विधियों और प्राथमिक प्रयोगशाला विधियों के एक पैनल का उपयोग रोगी के निवास स्थान पर तर्कसंगत रूढ़िवादी चिकित्सा और अधिक आक्रामक चिकित्सा सुनिश्चित करता है, उदाहरण के लिए, विशेष केंद्रों में बीएमटी। साहित्य:
1. रोसेन एफएस, वेजवुड आरजेपी, ईबल एम, फिशर ए, एयूटी एफ, नोटारंगेलो एल, किशिमोटो टी, रेसनी सीके आईबी, हैमरस्ट्रॉम एल, सेगर आर, चैपल एच, थॉम्पसन आरए, कूपर एमडी, गेहा आरएस, गुड आरए, वाल्डमैन टीए। प्राथमिक इम्यूनोडिफ़िशिएंसी रोग। डब्ल्यूएचओ वैज्ञानिक समूह की रिपोर्ट। क्लिनिकल और प्रायोगिक इम्यूनोलॉजी 1997; 109 (सप्ल। 1): 1 - 28। |
विभिन्न प्रकृति के रोगजनकों के लिए प्रतिरक्षा प्रतिक्रिया के कमजोर होने के कारण, इम्यूनोडेफिशियेंसी मानव शरीर के सुरक्षात्मक कार्यों का उल्लंघन है। विज्ञान ने इस प्रकार की प्रजातियों की एक पूरी श्रृंखला का वर्णन किया है। रोगों के इस समूह को संक्रामक रोगों के पाठ्यक्रम में वृद्धि और वृद्धि की विशेषता है। इस मामले में प्रतिरक्षा के काम में विफलताएं इसके व्यक्तिगत घटकों की मात्रात्मक या गुणात्मक विशेषताओं में बदलाव से जुड़ी हैं।
प्रतिरक्षा गुण
प्रतिरक्षा प्रणाली शरीर के सामान्य कामकाज में एक आवश्यक भूमिका निभाती है, क्योंकि इसे एंटीजन का पता लगाने और नष्ट करने के लिए डिज़ाइन किया गया है जो दोनों बाहरी वातावरण (संक्रामक) से प्रवेश कर सकते हैं और अपनी स्वयं की कोशिकाओं (अंतर्जात) के ट्यूमर के विकास का परिणाम हो सकते हैं। सुरक्षात्मक कार्य मुख्य रूप से जन्मजात कारकों जैसे कि फागोसाइटोसिस और पूरक प्रणाली द्वारा प्रदान किया जाता है। अधिग्रहीत और सेलुलर प्रतिक्रियाएं जीव की अनुकूली प्रतिक्रिया के लिए जिम्मेदार हैं। पूरे सिस्टम का कनेक्शन विशेष पदार्थों - साइटोकिन्स के माध्यम से होता है।
शुरुआत के कारण के आधार पर, प्रतिरक्षा विकार की स्थिति को प्राथमिक और माध्यमिक इम्युनोडेफिशिएंसी में विभाजित किया जाता है।
प्राथमिक इम्युनोडेफिशिएंसी क्या है
प्राथमिक इम्युनोडेफिशिएंसी (पीआईडी) आनुवंशिक दोषों के कारण होने वाली प्रतिरक्षा प्रतिक्रिया के विकार हैं। ज्यादातर मामलों में, वे विरासत में मिले हैं और जन्मजात असामान्यताएं हैं। पीआईडी ज्यादातर जीवन में जल्दी पाए जाते हैं, लेकिन कभी-कभी किशोरावस्था या यहां तक कि वयस्कता तक उनका निदान नहीं किया जाता है।
पीआईडी विभिन्न नैदानिक अभिव्यक्तियों के साथ जन्मजात रोगों का एक समूह है। रोगों के अंतर्राष्ट्रीय वर्गीकरण में 36 वर्णित और पर्याप्त रूप से अध्ययन की गई प्राथमिक इम्युनोडेफिशिएंसी स्थितियां शामिल हैं, हालांकि, चिकित्सा साहित्य के अनुसार, उनमें से लगभग 80 हैं। तथ्य यह है कि सभी बीमारियों को जिम्मेदार जीन की पहचान नहीं की गई है।
केवल एक्स गुणसूत्र की जीन संरचना में कम से कम छह अलग-अलग इम्युनोडेफिशिएंसी की विशेषता होती है, और इसलिए लड़कों में इस तरह की बीमारियों की घटना लड़कियों की तुलना में अधिक परिमाण का क्रम है। एक धारणा है कि अंतर्गर्भाशयी संक्रमण का जन्मजात इम्युनोडेफिशिएंसी के विकास पर एक एटियलॉजिकल प्रभाव हो सकता है, लेकिन इस कथन की अभी तक वैज्ञानिक रूप से पुष्टि नहीं हुई है।

नैदानिक तस्वीर
नैदानिक अभिव्यक्तियाँप्राथमिक इम्युनोडेफिशिएंसी खुद की स्थिति के रूप में विविध हैं, लेकिन एक सामान्य लक्षण है - हाइपरट्रॉफाइड संक्रामक (बैक्टीरिया) सिंड्रोम।
प्राथमिक इम्युनोडेफिशिएंसी, साथ ही माध्यमिक वाले, संक्रामक एटियलजि के लगातार आवर्तक (आवर्तक) रोगों के रोगियों की प्रवृत्ति से प्रकट होते हैं, जो एटिपिकल रोगजनकों के कारण हो सकते हैं।
ब्रोन्कोपल्मोनरी सिस्टम और मानव ईएनटी अंग इन रोगों से सबसे अधिक प्रभावित होते हैं। इसके अलावा, श्लेष्म झिल्ली और त्वचा अक्सर प्रभावित होती है, जो फोड़े और सेप्सिस के रूप में प्रकट हो सकती है। जीवाणु रोगजनक ब्रोंकाइटिस और साइनसिसिस का कारण बनते हैं। जो लोग प्रतिरक्षाविहीन होते हैं वे अक्सर जल्दी गंजापन और एक्जिमा, और कभी-कभी एलर्जी का अनुभव करते हैं। ऑटोइम्यून विकार और घातक नवोप्लाज्म की प्रवृत्ति भी आम है। बच्चों में इम्यूनोडिफ़िशिएंसी लगभग हमेशा मानसिक और शारीरिक विकास में देरी का कारण बनती है।
प्राथमिक इम्युनोडेफिशिएंसी के विकास का तंत्र
इम्यूनोडिफ़िशिएंसी राज्यों के अध्ययन के मामले में उनके विकास के तंत्र के अनुसार रोगों का वर्गीकरण सबसे अधिक जानकारीपूर्ण है।

डॉक्टर प्रतिरक्षा प्रकृति के सभी रोगों को 4 मुख्य समूहों में विभाजित करते हैं:
ह्यूमोरल या बी-सेल, जिसमें ब्रूटन सिंड्रोम (एक्स क्रोमोसोम के साथ एग्माग्लोबुलिनमिया), आईजीए या आईजीजी की कमी, सामान्य इम्युनोग्लोबुलिन की कमी में अतिरिक्त आईजीएम, साधारण चर इम्युनोडेफिशिएंसी, नवजात शिशुओं के क्षणिक हाइपोगैमाग्लोबुलिनमिया और ह्यूमर इम्युनिटी से जुड़ी कई अन्य बीमारियां शामिल हैं।
टी-सेल प्राथमिक इम्युनोडेफिशिएंसी, जिन्हें अक्सर संयुक्त कहा जाता है, क्योंकि पहले विकारों के दौरान ह्यूमर इम्युनिटी हमेशा ख़राब होती है, उदाहरण के लिए, थाइमस का हाइपोप्लासिया (डि जॉर्ज सिंड्रोम) या डिसप्लेसिया (टी-लिम्फोपेनिया)।
फागोसाइटोसिस में दोषों के कारण होने वाली इम्युनोडेफिशिएंसी।
बिगड़ा हुआ काम के कारण प्रतिरक्षण क्षमता
संक्रमण के लिए संवेदनशीलता
चूंकि इम्युनोडेफिशिएंसी का कारण विभिन्न लिंक का उल्लंघन हो सकता है
प्रतिरक्षा प्रणाली, तो संक्रामक एजेंटों की संवेदनशीलता प्रत्येक विशिष्ट मामले के लिए समान नहीं होगी। इसलिए, उदाहरण के लिए, हास्य रोगों के साथ, रोगी को संक्रमण का खतरा होता है जो स्ट्रेप्टोकोकी, स्टेफिलोकोसी के कारण होता है, जबकि ये सूक्ष्मजीव अक्सर जीवाणुरोधी दवाओं के लिए प्रतिरोध दिखाते हैं। इम्युनोडेफिशिएंसी के संयुक्त रूपों के साथ, वायरस, जैसे कि दाद या कवक, जो मुख्य रूप से कैंडिडिआसिस द्वारा दर्शाए जाते हैं, बैक्टीरिया से जुड़ सकते हैं। फागोसाइटिक रूप मुख्य रूप से एक ही स्टेफिलोकोसी और ग्राम-नकारात्मक बैक्टीरिया द्वारा विशेषता है।

प्राथमिक इम्युनोडेफिशिएंसी की व्यापकता
वंशानुगत इम्युनोडेफिशिएंसी काफी दुर्लभ मानव रोग हैं। प्रत्येक विशिष्ट बीमारी के संबंध में इस तरह के प्रतिरक्षा विकारों की घटना की आवृत्ति का आकलन किया जाना चाहिए, क्योंकि उनकी व्यापकता समान नहीं है।
औसतन, पचास हजार में से केवल एक नवजात शिशु जन्मजात वंशानुगत प्रतिरक्षाविहीनता से पीड़ित होगा। इस समूह में सबसे आम बीमारी चयनात्मक IgA की कमी है। इस प्रकार की जन्मजात इम्युनोडेफिशिएंसी औसतन एक हजार नवजात शिशुओं में से एक में होती है। इसके अलावा, IgA की कमी के सभी मामलों में से 70% इस घटक की पूर्ण अपर्याप्तता से संबंधित हैं। साथ ही, एक प्रतिरक्षा प्रकृति के व्यक्ति की कुछ अधिक दुर्लभ बीमारियां, विरासत में मिली, 1: 1,000,000 के अनुपात में फैल सकती हैं।
यदि हम तंत्र के आधार पर पीआईडी रोगों की घटना की आवृत्ति पर विचार करें, तो एक बहुत ही रोचक तस्वीर उभरती है। बी-सेल प्राथमिक इम्युनोडेफिशिएंसी, या, जैसा कि उन्हें भी कहा जाता है, एंटीबॉडी उत्पादन के विकार, दूसरों की तुलना में अधिक बार होते हैं और सभी मामलों में 50-60% खाते हैं। इसी समय, प्रत्येक 10-30% रोगियों में टी-सेल और फागोसाइटिक रूपों का निदान किया जाता है। पूरक दोषों के कारण सबसे दुर्लभ प्रतिरक्षा प्रणाली के रोग हैं - 1-6%।
यह भी ध्यान दिया जाना चाहिए कि पीआईडी की घटना की आवृत्ति पर डेटा अलग-अलग देशों में बहुत भिन्न होता है, जो किसी विशेष राष्ट्रीय समूह के आनुवंशिक पूर्वाग्रह से कुछ डीएनए उत्परिवर्तन से जुड़ा हो सकता है।
इम्युनोडेफिशिएंसी का निदान
बच्चों में प्राथमिक इम्युनोडेफिशिएंसी अक्सर समय से पहले निर्धारित की जाती है,
इस तथ्य के साथ कि जिला बाल रोग विशेषज्ञ के स्तर पर ऐसा निदान करना काफी कठिन है।

यह, एक नियम के रूप में, उपचार की देरी से शुरू होने और चिकित्सा के प्रतिकूल पूर्वानुमान की ओर जाता है। यदि डॉक्टर, रोग की नैदानिक तस्वीर और सामान्य विश्लेषण के परिणामों के आधार पर, एक इम्युनोडेफिशिएंसी अवस्था का सुझाव देता है, तो उसे सबसे पहले बच्चे को एक प्रतिरक्षाविज्ञानी के परामर्श के लिए भेजना चाहिए।
यूरोप में, इम्यूनोलॉजिस्ट का एक संघ है, जो इस तरह की बीमारियों के इलाज के तरीकों के अध्ययन और विकास से संबंधित है, जिसे ईओआई (यूरोपियन सोसाइटी फॉर इम्यूनोडेफिशिएंसी) कहा जाता है। उन्होंने पीआईडी रोगों के डेटाबेस को बनाया है और लगातार अद्यतन कर रहे हैं और काफी त्वरित निदान के लिए एक नैदानिक एल्गोरिथम को मंजूरी दी है।
निदान रोग के इतिहास के संग्रह के साथ शुरू होता है। वंशावली पहलू पर विशेष ध्यान दिया जाना चाहिए, क्योंकि अधिकांश जन्मजात प्रतिरक्षाविहीनता वंशानुगत होती है। इसके अलावा, एक शारीरिक परीक्षण और सामान्य नैदानिक अध्ययनों से डेटा प्राप्त करने के बाद, एक प्रारंभिक निदान किया जाता है। भविष्य में, डॉक्टर की धारणा की पुष्टि या खंडन करने के लिए, रोगी को एक आनुवंशिकीविद् और प्रतिरक्षाविज्ञानी जैसे विशेषज्ञों द्वारा पूरी तरह से जांच से गुजरना होगा। उपरोक्त सभी जोड़तोड़ करने के बाद ही हम अंतिम निदान के बारे में बात कर सकते हैं।
प्रयोगशाला अनुसंधान

यदि निदान के दौरान प्राथमिक इम्युनोडेफिशिएंसी सिंड्रोम का संदेह है, तो निम्नलिखित प्रयोगशाला परीक्षण किए जाने चाहिए:
एक विस्तृत रक्त गणना की स्थापना (लिम्फोसाइटों की संख्या पर विशेष ध्यान दिया जाता है);
रक्त सीरम में इम्युनोग्लोबुलिन की सामग्री का निर्धारण;
बी- और टी-लिम्फोसाइटों की मात्रा का ठहराव।
अतिरिक्त शोध
प्रयोगशाला और नैदानिक परीक्षणों के अलावा, जो पहले से ही ऊपर बताए गए हैं, प्रत्येक विशिष्ट मामले में, व्यक्तिगत अतिरिक्त परीक्षण सौंपे जाएंगे। ऐसे जोखिम समूह हैं जिन्हें एचआईवी संक्रमण या आनुवंशिक असामान्यताओं के लिए परीक्षण करने की आवश्यकता है। डॉक्टर इस संभावना के लिए भी प्रदान करता है कि 3 या 4 प्रकार की मानव इम्युनोडेफिशिएंसी है, जिसमें वह टेट्राज़ोलिन ब्लू इंडिकेटर के साथ एक परीक्षण स्थापित करके और पूरक प्रणाली के घटक संरचना की जांच करके रोगी के फैगोसाइटोसिस के विस्तृत अध्ययन पर जोर देगा।
पीआईडी उपचार
जाहिर है, आवश्यक चिकित्सा मुख्य रूप से प्रतिरक्षा रोग पर ही निर्भर करेगी, लेकिन, दुर्भाग्य से, जन्मजात रूप को पूरी तरह से समाप्त नहीं किया जा सकता है, जिसे अधिग्रहित इम्युनोडेफिशिएंसी के बारे में नहीं कहा जा सकता है। आधुनिक चिकित्सा विकास के आधार पर, वैज्ञानिक आनुवंशिक स्तर पर कारण को खत्म करने का एक तरीका खोजने की कोशिश कर रहे हैं। जब तक उनके प्रयासों को सफलता नहीं मिली, तब तक यह कहा जा सकता है कि इम्युनोडेफिशिएंसी एक लाइलाज स्थिति है। आइए लागू चिकित्सा के सिद्धांतों पर विचार करें।

प्रतिस्थापन चिकित्सा
इम्यूनोडिफ़िशिएंसी का उपचार आमतौर पर प्रतिस्थापन चिकित्सा के लिए कम किया जाता है। जैसा कि पहले उल्लेख किया गया है, रोगी का शरीर स्वतंत्र रूप से प्रतिरक्षा प्रणाली के कुछ घटकों का उत्पादन करने में सक्षम नहीं है, या उनकी गुणवत्ता आवश्यकता से काफी कम है। इस मामले में थेरेपी में एंटीबॉडी या इम्युनोग्लोबुलिन की दवा शामिल होगी, जिसका प्राकृतिक उत्पादन बिगड़ा हुआ है। अक्सर, दवाओं को अंतःशिरा रूप से प्रशासित किया जाता है, लेकिन कभी-कभी रोगी के जीवन को आसान बनाने के लिए चमड़े के नीचे का मार्ग भी संभव होता है, जिसे इस मामले में एक बार फिर चिकित्सा संस्थान का दौरा नहीं करना पड़ता है।
प्रतिस्थापन सिद्धांत अक्सर रोगियों को लगभग सामान्य जीवन जीने की अनुमति देता है: अध्ययन, काम और आराम। बेशक, रोग, हास्य और सेलुलर कारकों से कमजोर प्रतिरक्षा और महंगी दवाओं के प्रशासन की निरंतर आवश्यकता रोगी को पूरी तरह से आराम करने की अनुमति नहीं देगी, लेकिन यह अभी भी एक दबाव कक्ष में जीवन से बेहतर है।
और रोकथाम
यह देखते हुए कि किसी भी जीवाणु या वायरल संक्रमण, एक स्वस्थ व्यक्ति के लिए महत्वहीन, प्राथमिक इम्युनोडेफिशिएंसी के समूह की बीमारी वाले रोगी के लिए घातक हो सकता है, रोकथाम को सही ढंग से करना आवश्यक है। यह वह जगह है जहां जीवाणुरोधी, एंटिफंगल और एंटीवायरल दवाएं खेल में आती हैं। इसे निवारक उपायों पर ठीक से किया जाना चाहिए, क्योंकि एक कमजोर प्रतिरक्षा प्रणाली गुणवत्तापूर्ण उपचार प्रदान करने की अनुमति नहीं दे सकती है।
इसके अलावा, यह याद रखना चाहिए कि ऐसे रोगियों को एलर्जी, ऑटोइम्यून और इससे भी बदतर, नियोप्लास्टिक स्थितियों का खतरा होता है। यह सब, पूर्ण चिकित्सा पर्यवेक्षण के बिना, एक व्यक्ति को एक पूर्ण जीवन शैली का नेतृत्व करने की अनुमति नहीं दे सकता है।
ट्रांसप्लांटेशन
जब विशेषज्ञ यह निर्णय लेते हैं कि रोगी के लिए सर्जरी के अलावा कोई दूसरा रास्ता नहीं है, तो अस्थि मज्जा प्रत्यारोपण किया जा सकता है। यह प्रक्रिया रोगी के जीवन और स्वास्थ्य के लिए कई जोखिमों से जुड़ी है और व्यवहार में, सफल परिणाम के मामले में भी, हमेशा एक प्रतिरक्षा विकार की सभी समस्याओं का समाधान नहीं कर सकती है। इस तरह के एक ऑपरेशन को अंजाम देते समय, पूरे प्राप्तकर्ता को दाता द्वारा प्रदान किए गए उसी के साथ बदल दिया जाता है।
प्राथमिक इम्युनोडेफिशिएंसी आधुनिक चिकित्सा की सबसे कठिन समस्या है, जो दुर्भाग्य से, अभी तक पूरी तरह से हल नहीं हुई है। इस तरह की बीमारियों के लिए प्रतिकूल पूर्वानुमान अभी भी बना हुआ है, और यह दोगुना दुखद है, इस तथ्य को देखते हुए कि वे सबसे अधिक बार बच्चों से प्रभावित होते हैं। लेकिन फिर भी, प्रतिरक्षा की कमी के कई रूप पूर्ण जीवन के अनुकूल हैं, बशर्ते उनका समय पर निदान किया जाए और पर्याप्त चिकित्सा लागू की जाए।