Муковисцидоз у детей: клинические рекомендации родителям. Муковисцидоз: современный подход к диагностике и лечению
Муковисцидоз (кистозный фиброз) - заболевание, сопровождающееся генерализованным поражением экзокринных желёз. Это распространённое аутосомно-рецессивное наследственное заболевание наблюдают у детей с частотой от 1:2000 до 1:12 000 новорождённых. Муковисцидоз широко распространён как в индустриально развитых странах Западной Европы, так и в США, где количество диагностированных больных составляет 7-8:100 000 населения.
Этиология и патогенез
Ген муковисцидоза открыли в 1989 г. В результате мутации гена нарушается структура и функция специфического белка (трансмембранного регулятора MB), локализующегося в апикальной части мембраны эпителиальных клеток, выстилающих выводные протоки поджелудочной железы, желёз кишечника, бронхолёгочной системы, мочевого тракта, и регулирующего транспорт ионов хлора между этими клетками и межклеточной жидкостью. Патогенез поражения отдельных органов и систем при муковисцидозе связан с выделением слизеобразуюшими железами секрета повышенной вязкости. Ранние лёгочные изменения (на 5-7-й неделе жизни ребёнка) связаны с гипертрофией бронхиальных слизистых желёз и гиперплазией бокаловидных клеток. Вязкий бронхиальный секрет тормозит работу реснитчатого эпителия и приводит к нарушению дренажной функции бронхов. Присоединение патогенной микрофлоры (чаще всего золотистого стафилококка, синегнойной и гемофильной палочек) приводит к развитию хронического воспалительного процесса.
Для муковисцидоза характерно формирование диффузного пневмофиброза, бронхоэктазов, что в сочетании с эмфиземой приводит к развитию лёгочной гипертензии, лёгочного сердца, правожелудочковой недостаточности.
Обтурация выводных протоков поджелудочной железы вязким секретом нарушает её внешне- и внутрисекреторную деятельность. Это проявляется в основном нарушением ассимиляции жиров и стеатореей. Аналогичные изменения желёз кишечника в сочетании с нарушением функции поджелудочной железы вызывают мекониальную кишечную непроходимость у новорождённых, выпадение прямой кишки и дистальную интестинальную обструкцию у детей более старшего возраста.
Клиническая картина
Выделяют три основные клинические формы муковисцидоза.
- Смешанная форма с поражением ЖКТ и бронхолёгочной системы (78-80%).
- Преимущественное поражение лёгких (15-20%).
- Преимущественное поражение ЖКТ (5%).
В период новорождённости у детей может развиваться кишечная непроходимость (мекониевый илеус), сопровождающаяся рвотой, вздутием живота, неотхождением мекония, нарастающим токсикозом и эксикозом. Однако чаще муковисцидоз манифестирует в грудном возрасте в связи с переводом ребёнка на смешанное вскармливание. Появляются обильный зловонный замазкообразный жирный стул (изменения связаны с нарушением внешнесекреторной деятельности поджелудочной железы), увеличение печени, прогрессирует дистрофия, возможно выпадение прямой кишки. Характерен внешний вид детей: сухая серовато-землистая кожа, худые конечности с деформацией концевых фаланг пальцев в виде «барабанных палочек», расширенная, нередко деформированная грудная клетка, большой вздутый живот. Затем в клинической картине начинают преобладать бронхолёгочные изменения, определяющие прогноз более чем у 90% больных муковисцидозом. Больных беспокоят упорный навязчивый кашель, бронхорея, одышка. Чрезмерная вязкость мокроты способствует присоединению вторичной инфекции и развитию прогрессирующего хронического бронхолёгочного процесса с диффузным пневмофиброзом, бронхоэктазами, кистами, ателектазами, зонами ограниченного пневмосклероза. Постепенно нарастает лёгочно-сердечная недостаточность.
Муковисцидоз может осложниться развитием пневмоторакса, пиопневмоторакса, кровохарканья, лёгочного кровотечения.
Лабораторные и инструментальные исследования
Для диагностики муковисцидоза применяют определение концентрации хлоридов в потовой жидкости, которое проводят не менее трёх раз. При муковисцидозе концентрация хлоридов в потовой жидкости превышает 60 ммоль/л. При получении пограничных значений концентрации хлоридов в поте (40-60 ммоль/л) необходимо провести анализ ДНК. В настоящее время с успехом применяют пренатальную ДНК-диагностику.
При рентгенографии органов грудной клетки выявляют эмфизему, мигрирующие ателектазы, участки инфильтрации лёгочной ткани и пневмосклероза, усиление и деформацию лёгочного рисунка. При бронхоскопии обнаруживают диффузный гнойный эндобронхит, при бронхографии - распространённый деформирующий бронхит и двусторонние бронхоэктазы. В копрограмме выявляют большое количество нейтрального жира.
Диагностика и дифференциальная диагностика
Основные диагностические критерии муковисцидоза:
- муковисцидоз у сибсов;
- рано развившийся, торпидный к терапии хронический бронхолёгочный процесс;
- типичный кишечный синдром;
- положительный тест на определение хлоридов в поте.
Дифференциальную диагностику проводят с врождёнными бронхолёгочными дисплазиями и пороками развития, коклюшем, затяжным бронхообструктивным синдромом.
Лечение
Лечение при муковисцидозе включает постоянное очищение бронхиального дерева, антибиотикотерапию и нормализацию питания больных.
- Для очищения бронхиального дерева показаны муколитики в больших дозах перорально и в аэрозолях, постуральный дренаж, вибромассаж, аутогенный дренаж, форсированная экспираторная техника дыхания, бронхоскопические санации.
- Антибиотикотерапию следует проводить с учётом результатов микробиологического исследования. При муковисцидозе назначают высокие дозы антибиотиков бактерицидного действия, пролонгированные (2-3 нед) курсы лечения, комбинации препаратов для преодоления резистентности микрофлоры; при обострениях заболевания показано внутривенное введение антибиотиков в сочетании с ингаляционным. В последнее время антибиотики назначают не только во время обострения, но и с профилактической целью при хронической колонизации бронхиального дерева синегнойной палочкой. Используют цефалоспорины II-III поколения, аминогликозиды, карбапенемы. Широко применяют курсы ингаляционной антибактериальной терапии, перорального приёма антисинегнойных препаратов из группы фторхинолонов (ципрофлоксацин), внутривенное введение антибиотиков в домашних условиях, что позволяет уменьшить возможность перекрёстного инфицирования и материальные затраты, повысить качество жизни больных.
- Для нормализация питания больных необходимы высококалорийная диета без ограничения жиров, постоянный прием ферментных препаратов, покрытых оболочкой, резистентной к желудочному соку (например, креон, панцитрат), приём жирорастворимых витаминов A, D, Е, К.
В настоящее время разработана генно-инженерная терапия муковисцидоза.
Диспансерное наблюдение
Больных муковисцидозом необходимо наблюдать в специализированных центрах, сеть которых создаётся в нашей стране. Больных с периодичностью 1 раз в 3 мес подвергают детальному обследованию, включающему антропометрию, определение функции внешнего дыхания, общие клинические анализы крови и мочи, копрограмму, анализ мокроты на микрофлору и чувствительность к антибиотикам. По результатам обследования корригируют лечебно-реабилитационный режим. Не реже 1 раза в год необходимо проводить рентгенографию грудной клетки, определение костного возраста, биохимический и иммунологический анализы крови, ЭхоКГ и УЗИ органов брюшной полости. В последние годы больных активно наблюдают и лечат в дневных стационарах и назначают антибактериальную терапию на дому.
Прогноз
Прогноз при муковисцидозе остаётся неблагоприятным и определяется тяжестью бронхолёгочных изменений. Рано манифестировавший муковисцидоз протекает тяжелее, особенно у детей, перенёсших мекониевый илеус. Значительно ухудшается прогноз при хронической колонизации бронхиального дерева синегнойной палочкой. В то же время успехи диагностики и терапии муковисцидоза привели к значительному увеличению выживаемости больных. Так, если в 50-е гг. XX века около 80% больных умирали в возрасте до 10 лет, то в настоящее время средняя продолжительность жизни больных муковисцидозом составляет 29 лет и более.
Способы диагностики

Первое, что можно сделать для установки диагноза, - это обратиться к врачу в течение первых 10 недель беременности .
Специалисту достаточно взять на анализ пуповинную кровь, а делается такая процедура по показаниям, когда существует риск передачи наследственного заболевания.
Основные причины ранней диагностики:
- семейный анамнез, при котором у близких родственников были зафиксированы случаи развития муковисцидоза;
- длительное бесплодие;
- патологии легких, ЖКТ.
Все генетические исследования можно проводить как внутриутробно, так и после рождения ребенка.
Главным показателем болезни новорожденного можно назвать врожденную мекониевую непроходимость. Не менее информативным исследованием является проба пота ребенка.
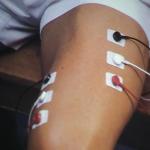
Для этого используется слабой силы электрический ток, помогающий стимуляции потовых желез.
На протяжении часа пот собирают для проведения исследования на специальную фильтровальную бумагу, чтобы определить в нем уровень хлорида.
При муковисцидозе уровень хлорида должен быть более 60 единиц с двух отдельно взятых образцов . У здоровых детей этот показатель значительно ниже, но для только родившихся метод не всегда срабатывает.
В этом случае применяют исследование крови на иммунореактивный трипсиноген . В течение первых 2 дней жизни у ребенка берут кровь из пятки для определения наличия или отсутствия специального белка (трипсиногена).
Положительная динамика свидетельствует о развитии заболевания. Но такое исследование все равно должно подтверждаться потовыми пробами и химическими тестами на наличие генных изменений.
Обязательно проводится копрограмма кала, биохимическое исследование крови, анализ ДНК (в том числе внутриутробно), бронхоскопия, спирометрия, бронхография.
Схемы и методы лечения
Заболевание в легкой форме поддается лечению в домашних условиях, а более тяжелая степень поражения требует длительной терапии в стационаре.
Полностью вылечить болезнь невозможно, но можно облегчить самочувствие, не допустить развития осложнений у ребенка.
Лечение должно быть полноценным, включающим целый комплекс препаратов.
Легочную форму лечат несколько иначе, чем кишечную, а смешанная патология требует индивидуального назначения лекарств в зависимости от степени поражения.
При кишечной форме врач назначает лечебное питание с употреблением большого количества белковой пищи и резким сокращением углеводов и липидов.
В некоторых случаях придется отказаться от молока, но выпивать достаточно много жидкости.
Дополнительно проводится пожизненная медикаментозная терапия - чаще это ферментные препараты (Панкреатин, Мезим). При сопутствующем поражении гепатоцитов применяют гепатопротекторы (Эссенциале, Эссливер).
Иногда при тяжелом поражении может потребоваться пересадка печени. Обязательно надо снабжать организм витаминами, сделать акцент на калорийности пищи. Для ускорения оттока желчи и желудочного секрета назначают Ацетилцистеин.
Совсем другая схема терапии действует при легочном муковисцидозе . В случае проявления признаков пневмонии или при наличии бактериальной инфекции врач назначает антибиотики третьего поколения (цефалоспроины), аминогликозиды и фторхинолоны.
Используются они как в виде инъекций, так и в виде ингаляционных спреев. Обязательно применяют муколитические средства, способствующие разжижению мокроты и ее скорейшему выведению (АЦЦ, Амилорид, Флуифорт).
Нередко в состав терапии включают кортикостероиды или НПВС.
Обязательной процедурой будет ежедневный бронхиальный дренаж, помогающий выведению густой слизи из легких и бронхов. Его можно проводить самостоятельно.
Достаточно уложить ребенка на бок так, чтобы его поясница была несколько выше плеч. Ребенка начинают слегка похлопывать по спине, бокам и грудной клетке, чтобы в процессе создаваемой легкой вибрации легкие очистились от слизи.
Прогноз излечиваемости

Кроме описанных процедур и препаратов, могут быть использованы противоотечные препараты, бронходилататоры.
Обязательной будет и адекватная физическая активность, специальная лечебная гимнастика, прогулки на свежем воздухе.
Болезнь неизлечима, а продлить жизнь, улучшить ее качество можно , только пожизненно принимая все необходимые лекарства.
Продолжительность жизни детей с муковисцидозом зависит от присоединения вторичной бактериальной инфекции, степени развития осложнений.
Если болезнь протекает в легкой форме, то прогноз для жизни благоприятен . При наличии бронхолегочных патологий, нарушений в работе пищеварительного тракта смертность увеличивается (особенно у детей до года).
Своевременно поставленный диагноз и правильная терапия увеличивают шансы на продление жизни. Но если болезнь диагностировали у новорожденного, шансов выжить у него очень мало.
Избежать подобной болезни у своего ребенка родители могут , заранее сделав генетическую диагностику и получив консультацию у профильного врача.
Вконтакте
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ СОЮЗ ПЕДИАТРОВ РОССИИ
Главный внештатный специалист педиатр Минздрава России Академик РАН А.А. Баранов
___________________
МЕТОДОЛОГИЯ............................................. | Ошибка! Закладка не определена. |
ОПРЕДЕЛЕНИЕ.......................................................................................................... | |
ЭПИДЕМИОЛОГИЯ................................................................................................... | |
ЭТИОЛОГИЯ............................................................................................................... | |
ПАТОГЕНЕЗ................................................................................................................ | |
КЛАССИФИКАЦИЯ.................................................................................................. | |
КЛИНИЧЕСКАЯ КАРТИНА..................................................................................... | |
ДИАГНОСТИКА......................................................................................................... | |
ПРИМЕРЫ ДИАГНОЗОВ........................................................................................ | |
ЛЕЧЕНИЕ................................................................................................................... | |
ПРОФИЛАКТИКА.................................................................................................... | |
ПРОГНОЗ................................................................................................................... |
Данные клинические рекомендации подготовлены совместно с Всероссийской ассоциацией для больных муковисцидозом, рассмотрены и утверждены на заседании Исполкома профессиональной ассоциации детских врачей Союза педиатров России на XVII Съезде педиатров России «Актуальные проблемы педиатрии» 15 февраля 2013г., актуализированы в 2014 г. Утверждены на XVIII Конгрессе педиатров России «Актуальные проблемы педиатрии» 14 февраля 2015г.
Состав рабочей группы: акад. РАН Баранов А.А., чл-корр. РАН Намазова-Баранова Л.С., проф., д.м.н. Симонова О.И., проф., к.м.н. Каширская Н.Ю., проф., д.м.н. Кондратьева Е.И., д.м.н. Рославцева Е.А., к.м.н. Горинова Ю.В., к.м.н. Красовский С.А., к.м.н. Томилова А.Ю., к.м.н. Селимзянова Л.Р.
МЕТОДОЛОГИЯ Методы, используемые для сбора/селекции доказательств: поиск в электронных
базах данных.
Описание методов, использованных для оценки качества и силы доказательств: доказательной базой для рекомендаций являются публикации, вошедшие в Кохрейновскую библиотеку, базы данных EMBASE, MEDLINE и PubMed. Глубина поиска - 5 лет.
Методы, использованные для оценки качества и силы доказательств:
консенсус экспертов;
Методы, использованные для анализа доказательств:
систематические обзоры с таблицами доказательств.
Описание методов, использованных для анализа доказательств
При отборе публикаций, как потенциальных источников доказательств, использованная
в каждом исследовании методология изучается для того, чтобы убедиться в ее валидности. Результат изучения влияет на уровень доказательств, присваиваемый публикации, что в свою очередь, влияет на силу рекомендаций.
Для минимизации потенциальных ошибок каждое исследование оценивалось независимо. Любые различия в оценках обсуждались всей группой авторов в полном составе. При невозможности достижения консенсуса привлекался независимый эксперт.
Таблицы доказательств : заполнялись авторами клинических рекомендаций.
Методы, использованные для формулирования рекомендаций: консенсус экспертов.
Индикаторы доброкачественной практики (Good Practice Points – GPPs)
Экономический анализ
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Внешняя экспертная оценка.
Внутренняя экспертная оценка.
независимыми экспертами, которых, прежде всего, попросили прокомментировать, насколько доступна для понимания интерпретация доказательств, лежащая в основе рекомендаций.
От врачей первичного звена получены комментарии в отношении доходчивости изложения данных рекомендаций, а также их оценка важности предлагаемых рекомендаций, как инструмента повседневной практики.
Все комментарии, полученные от экспертов, тщательно систематизировались и обсуждались членами рабочей группы (авторами рекомендаций). Каждый пункт обсуждался в отдельности.
Консультация и экспертная оценка
Рабочая группа
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Соотношение | Методологическое | качество | Пояснения | |||||||||||||||
достоверности | и преимуществ | имеющихся доказательств | применению | |||||||||||||||
отчетливо | Надежные | непротиворечивые | ||||||||||||||||
превалирует | доказательства, | основанные | ||||||||||||||||
выполненных | ||||||||||||||||||
основанная | затратами, | неопровержимые | доказательства, | использоваться | ||||||||||||||
доказательствах | наоборот | представленные | какой-либо | большинстве | ||||||||||||||
высокого качества | другой форме. | у преимущественного |
||||||||||||||||
количества пациентов |
||||||||||||||||||
нашу уверенность в оценке | каких-либо |
|||||||||||||||||
соотношения пользы и риска. | изменений | |||||||||||||||||
исключений | ||||||||||||||||||
отчетливо | Доказательства, | основанные | ||||||||||||||||
превалирует | результатах | выполненных с | ||||||||||||||||
некоторыми | ограничениями | применение | ||||||||||||||||
основанная | затратами, | (противоречивые | результаты, | возможно | ||||||||||||||
доказательствах | наоборот | методологические | большинстве случаев |
|||||||||||||||
умеренного качества | косвенные или случайные и т.п.), | |||||||||||||||||
других веских | основаниях. | |||||||||||||||||
Дальнейшие | исследования | |||||||||||||||||
проводятся), | вероятно, | |||||||||||||||||
влияние на нашу уверенность в | ||||||||||||||||||
оценке соотношения пользы и риска | ||||||||||||||||||
и могут изменить ее. | ||||||||||||||||||
вероятно, | Доказательства, | основанные | Относительно сильная |
|||||||||||||||
будет превалировать | обсервационных | исследованиях, | ||||||||||||||||
возможными | бессистемном клиническом | которая может | ||||||||||||||||
основанная | результатах | выполненных с | изменена | |||||||||||||||
доказательствах | затратами, | существенными | недостатками. | получении | ||||||||||||||
низкого качества | наоборот | доказательств | ||||||||||||||||
расценивается как неопределенная. | высокого качества |
|||||||||||||||||
сопоставима | Надежные | доказательства, | ||||||||||||||||
возможными | основанные | наилучшей |
||||||||||||||||
силы, основанная | рисками и затратами | выполненных | ||||||||||||||||
доказательствах | подтвержденные | зависеть | ||||||||||||||||
высокого качества | неопровержимыми данными. | клинической | ||||||||||||||||
Дальнейшие исследования вряд ли | ситуации | |||||||||||||||||
изменят нашу уверенность в оценке | (обстоятельств), | |||||||||||||||||
соотношения пользы и риска. | пациента | |||||||||||||||||
социальных | ||||||||||||||||||
предпочтений. | ||||||||||||||||||
сопоставима | Доказательства, | основанные | ||||||||||||||||
результатах | выполненных с | Альтернативная | ||||||||||||||||
основанная | осложнениями, | существенными | ограничениями | |||||||||||||||
доказательствах | однако в этой оценке | (противоречивые | результаты, | определенных | ||||||||||||||
умеренного качества | методологические | ситуациях | ||||||||||||||||
неопределенность. | косвенные | случайные), | ||||||||||||||||
доказательства, | некоторых | пациентов |
||||||||||||||||
представленные | какой-либо | лучшим выбором. |
||||||||||||||||
другой форме. | ||||||||||||||||||
Дальнейшие | исследования | |||||||||||||||||
проводятся), | ||||||||||||||||||
уверенность в оценке соотношения | ||||||||||||||||||
пользы и риска и могут изменить ее. | ||||||||||||||||||

Неоднозначность | Доказательства, | основанные на | |||||||||
оценке соотношения | обсервационных | исследованиях, | |||||||||
основанная | пользы, рисков | бессистемного клинического опыта | альтернативные | ||||||||
доказательствах | осложнений; | существенными | подходы могут быть |
||||||||
низкого качества | недостатками. | использованы | |||||||||
сопоставима | расценивается | равной степени. | |||||||||
возможными | неопределенная. | ||||||||||
осложнениями. | |||||||||||
*В таблице цифровое значение соответствует силе рекомендаций, буквенное - соответствует уровню доказательности
ОПРЕДЕЛЕНИЕ
Кистозный фиброз (Муковисцидоз - МВ) - аутосомно-рецессивное моногенное наследственное заболевание, характеризующееся поражением всех экзокринных желёз, а также жизненно важных органов и систем.
Код по МКБ-10
E84 Кистозный фиброз.
E84.0 Кистозный фиброз с лёгочными проявлениями.
E84.1 Кистозный фиброз с кишечными проявлениями.
E84.8 Кистозный фиброз с другими проявлениями.
E84.9 Кистозный фиброз неуточнённый.
ЭПИДЕМИОЛОГИЯ
Частота МВ колеблется среди представителей европеоидов от 1:600 до 1:17000 новорожденных. В РФ частота муковисцидоза составляет по данным ФГБУ Медикогенетического научного центра 1:10000 новорожденных.
В Москве медиана выживаемости составляет 39,5 лет.
ЭТИОЛОГИЯ
Ген МВ был изолирован в 1989 г., он расположен в середине длинного плеча 7 аутосомы, содержит 27 экзонов и охватывает 250 000 пар нуклеотидов. Он контролирует структуру и функцию белка, названного МВТР - трансмембранный регулятор МВ. На сегодняшний день выделено около 2 000 мутаций гена - трансмембранного регулятора проводимости муковисцидоза (МВТР), ответственных за развитие симптомов МВ. Среди них, согласно данным национального регистра, наиболее часто встречаются следующие мутации: F508del (52,79%), СFTRdele (2,3-6,32%), E92K(2,65%), 2184insA (2,02%), 3849+10kbC>T (1,65%), 2143delT (1,65%), G542X (1,33%), N1303K (1,33%), W1282X (1,11%), L138ins (1,06%).
ПАТОГЕНЕЗ

МВТР локализуется в апикальной части мембраны эпителиальных клеток, выстилающих выводные протоки желез внешней секреции (потовых, слюнных, желез в бронхах, поджелудочной железе, кишечнике, урогенитальном тракте), он регулирует транспорт электролитов (главным образом хлора) между этими клетками и межклеточной жидкостью. Последние исследования показали, что МВТР является собственно хлоридным каналом. Мутации гена МВ нарушают не только транспорт, но и секрецию ионов хлора. При затруднении их прохождения через клеточную мембрану увеличивается реабсорбция натрия железистыми клетками, нарушается электрический потенциал просвета, что вызывает изменение электролитного состава и дегидратацию секрета желез внешней секреции. В результате выделяемый секрет становится чрезмерно густым и вязким. При этом страдают легкие, желудочно-кишечный тракт, печень, поджелудочная железа, мочеполовая система (табл 2).
Таблица 2. |
|||||||||||
Патогенез МВ |
|||||||||||
Органы и системы | Патологические процессы | Конечный результат | |||||||||
Бронхообструкция, | Дыхательная недостаточность, |
||||||||||
снижение толерантности к инфекции, | легочная гипертензия, |
||||||||||
колонизация | дыхательных | сердечная недостаточность. |
|||||||||
Pseudomonas aeruginosa (P. aeruginosa) и | |||||||||||
патологическими | |||||||||||
микроорганизмами, | |||||||||||
хроническое | воспаление | дыхательных | |||||||||
бронхоэктазы, | деструкция | ||||||||||
паренхимы легких. | |||||||||||
Поджелудочная железа | Обструкция протоков железы, | Нарушение | |||||||||
появление кист, | жирный, зловонный, обильный), |
||||||||||
недостаточность | поджелудочной | снижение | нутритивного статуса |
||||||||
(внутренне - и внешнесекреторная), | (у детей – отставание в развитии), |
||||||||||
кишечная мальабсорбция. | авитаминозы, | ||||||||||
выпадения прямой кишки, |
|||||||||||
сахарный диабет. | |||||||||||
Холестаз, холелитиаз. | |||||||||||
портальной | гипертензии, |
||||||||||
гиперспленизм, | печеночная |
||||||||||
недостаточность | |||||||||||
Кишечник | Увеличение вязкости/адгезивности каловых | Кишечная непроходимость |
|||||||||
Репродуктивная система (у | Обструкция | последующая | Бесплодие | ||||||||
выносящих протоков яичек, | |||||||||||
азооспермия | |||||||||||
Прогрессирование легочной и сердечной недостаточности является наиболее частой причиной смерти больных (95%). Среди других причин в экономически развитых странах выделяют: осложнения при трансплантации органов – 12%; заболевания печени и печеночная недостаточность - 2,3% случаев; травмы – 2,1%; суицид – 0,8%; другие – 1,3%.
КЛАССИФИКАЦИЯ
Всемирная Организация Здравоохранения, Международная Ассоциация Муковисцидоза, Европейская Тематическая Сеть по проблемам Муковисцидоза, Европейская Ассоциация Муковисцидоза организовали совместную рабочую группу с целью разработки новой классификации.
Последняя актуальная версия для Международной классификации болезней нового пересмотра выглядит следующим образом:
- Классический муковисцидоз с панкреатической недостаточностью (PI);

- Классический муковисцидоз с ненарушенной функцией поджелудочной железы (PS);
- атипичный муковисцидоз;
- изолированная обструктивная азооспермия 2 ;
- хронический панкреатит 2 ;
- аллергический бронхолегочный аспергиллез (ABPA) 2 ;
- диссеминированные бронхоэктазы 2 ;
- диффузный панбронхиолит 2 ;
- склерозирующий холангит 1 ;
- неонатальная гипертрипсиногенемия;
- по крайней мере, одна из мутаций идентифицирована.
Тем не менее, на сегодняшний день, в клинической практике используется классификация, представленная в таблице 3.
Таблица 3. Клиническая классификация муковисцидоза
Характеристика бронхолегочных изм енений | |||||||
активность | Клиническая | Эндоскопическая | Функциональная: | Осложнения |
|||
процесса | вентиляционная | ||||||
недостаточ ность | |||||||
1. Бронхит: | Эндобронхит: | Обструкт | Абсцессы, |
||||
Смешанная | Ремиссия | катаральный, | ателектазы, |
||||
(легочно- | рецидивирую | катарально- | |||||
кишечная) | Рестрикт | пиопневмоторакс, |
|||||
Активность: | хронический | легочное сердце, |
|||||
Легочная | кровохаркание, |
||||||
2. Пневмония: | Ограниченный, | кровотечение |
|||||
Кишечная | повторная, | распространенны | рованный | (легочное, |
|||
рецидивирую | желудочное) |
||||||
гайморит, отечный |
|||||||
Обострение: | синдром, цирроз |
||||||
печени, эквиваленты |
|||||||
пневмония | мекониального илеуса, |
||||||
выпадение прямой |
|||||||
кишки, отставание в |
|||||||
физическом развитии |
|||||||
Конечно в будущем, по мере углубления знаний, эта классификация также потребует пересмотра.
КЛИНИЧЕСКАЯ КАРТИНА
У большинства пациентов первые симптомы МВ выявляются уже на первом году жизни, хотя известны случаи более позднего развития заболевания - вплоть до зрелого возраста.
2 - Дополнительно выделяют сольтеряющую форму или псевдо-синдром Барттера (гипокалий- и натриемия на фоне метаболического алкалоза), неонатальную гипертрипсиногенемию, а также различные атипичные формы заболевания.

Наличие у больного симптомов, указанных в таблице 5, требует проведения дифференциального диагноза МВ. Необходимо учитывать, что перечни симптомов, представленные в таблице 2, составлены в примерном соответствии каждой из рассматриваемых возрастных групп больных МВ. Любой из указанных симптомов может наблюдаться у детей младшего или старшего возраста (табл. 4).
Таблица 4. Клинические проявления, требующие дифференциального диагноза с МВ
Симптомы и синдромы |
||
Рецидивирующие или хронические респираторные симптомы, такие как кашель или одышка |
||
Рецидивирующая или хроническая пневмония |
||
Отставание в физическом развитии |
||
Неоформленный, обильный, маслянистый и зловонный стул |
||
Хроническая диарея |
||
Выпадение прямой кишки |
||
Затяжная неонатальная желтуха |
||
Соленый вкус кожи |
||
Тепловой удар или дегидратация при жаркой погоде |
||
Хроническая гипоэлектролитемия |
||
Данные семейного анамнеза о смерти детей на первом году жизни или наличие сибсов со |
||
сходными клиническими проявлениями |
||
Гипопротеинемия / отеки |
||
Дошкольный | Стойкий кашель с или без гнойной мокроты |
|
Диагностически неясная рецидивирующая или хроническая одышка |
||
Отставание в весе и росте |
||
Выпадение прямой кишки |
||
Инвагинация |
||
Хроническая диарея |
||
Симптом «барабанных палочек» |
||
Кристаллы соли на коже |
||
Гипотоническая дегидратация |
||
Гипоэлектролитемия и метаболический алкалоз |
||
Гепатомегалия или диагностически неясное нарушение функции печени |
||
Школьный | Хронические респираторные симптомы неясной этиологии |
|
Pseudomonasaeruginosa в мокроте |
||
Хронический синусит |
||
Назальный полипоз |
||
Бронхоэктазы |
||
Симптом «барабанных палочек» |
||
Хроническая диарея |
||
Панкреатит |
||
Выпадение прямой кишки |
||
Гепатомегалия |
||
Заболевание печени неясной этиологии |
||
Подростки | Гнойное заболевание легких неясной этиологии |
|
взрослые | Симптом «барабанных палочек» |
|
Панкреатит |
||
Синдром дистальной интестинальной обструкции |
||
Сахарный диабет в сочетании с респираторными симптомами |
||
Признаки цирроза печени и портальной гипертензии |
||
Отставание в росте |
||
Задержка полового развития |
||
Инфертильность с азооспермией у лиц мужского пола |
||
Снижение фертильности у лиц женского пола |
Для МВ свойственно прогрессирующее течение, частые обострения, обусловленные активностью инфекционных агентов: Haemophilus influenzae (H. influenzae), P. aeruginosa, Staphylococcus aureus (S. aureus), Burkholderia cepacia (B. cepacia).

ДИАГНОСТИКА
Диагноз МВ подтверждается при наличии одного или более характерных фенотипических проявлений МВ в сочетании с доказательствами наличия мутации гена МВТР, такими как: выявление мутаций гена МВТР при генотипировании или увеличение уровня хлоридов в секрете потовых желез больного.
Классический метод определения электролитного состава пота(хлора или натрия) методом пилокарпинового электрофореза по Гибсону и Куку (1959г.) является «золотым стандартом диагностики», проводится троекратно. Пограничные значения хлора 40-59 ммоль/л, патология 60 ммоль/л и выше (при навеске пота не менее 100 мг).
Потовый тест с помощью специальных потовых анализаторов позволяет получить результат электролитов в течение 30 минут, с минимальной навеской в 3-10 мкг.
При определении проводимости положительным результатом для муковисцидоза считается показатель: выше 80 ммоль/л; пограничным значением: 50-80 ммоль/л; нормальным – до 50 ммоль/л. Показатели проводимости выше 170 ммоль/л должны быть подвергнуты сомнению.
В качестве дополнительного теста может быть проведено исследование разности назальных потенциалов . В норме пределы разности потенциалов колеблются от -5mV до - 40 mV; у больных муковисцидозом эти пределы составляют от -40 mV до - 90 mV
При отсутствии фенотипических проявлений диагноз МВ может считаться установленным в тех случаях, когда:
- у обследуемого выявлена мутация гена МВТР и/или положительные результаты потовой пробы, а у родных братьев или сестер обследуемого подтвержден диагноз МВ;
- мутация гена МВТР и/или
- положительные результаты потовой пробы были выявлены у новорожденного.
Диагностические критерии МВ
Для решения проблем диагностики МВ, в том числе и его атипичных форм, были разработаны критерии, согласно которым обязательным для МВ является наличие характерного клинического синдрома плюс доказательство какого-либо нарушения функции хлорного канала
В настоящее время существует несколько вариантов диагностических критериев МВ, которыми пользуются специалисты. В случае доступности скрининга новорожденных и методики измерения разности назальных потенциалов актуальна схема, представленная в таблице 5. Для подтверждения диагноза достаточно иметь два признака, по одному из каждого столбца.
Таблица 5. Диагностические критерии МВ.
МВ у сибсов
Положительный неонатальный скрининг
Положительная разность назальных
Плюс потенциалов
Две значимые мутации в гене МВТР
Другим вариантом диагностических критериев является комбинация признаков, представленных в таблице 6. Данные критерии разработаны группой европейских экспертов .
Таблица 6. Диагностические критерии, утвержденные Европейскими стандартами 2014 года
Для цитирования:
Амелина Е.Л., Чучалин А.Г. МУКОВИСЦИДОЗ: СОВРЕМЕННЫЙ ПОДХОД К ДИАГНОСТИКЕ И ЛЕЧЕНИЮ // РМЖ. 1997. №17. С. 8
Муковисцидоз - одно из наиболее частых аутосомно-рецессивных наследственных заболеваний, распространенных среди представителей европейской расы, которое является актуальной причиной заболеваемости и смертности среди детей и подростков. В последние десятилетия число больных, страдающих муковисцидозом, значительно возрoсло в связи с улучшением диагностики и более комплексным подходом к терапии.
В последнее время достигнут определенный прогресс в научном подходе к муковисцидозу в результате достижений в области клеточной патологии, генетики и молекулярной биологии. Эта статья представляет собой обзор текущего состояния проблемы муковисцидоза и затрагивает основные причины, тип наследования, современную терапию и новые достижения в изучении этой патологии.
Cystic fibrosis (CF) is one of the most common autosomal recessive inherited disorders in the European population and represents an important cause of morbidity and mortality among children and young adults. In the past decades the number of the CF patients has increased considerably due to improved diagnosis and a more comprehensive approach to therapy. Recently, the scientific knowledge about CF has been improved as the result of advances in cell pathology, genetics and molecular biology. This article reiews the current status of our understanding of CF: and covers the main causes, mode of inheritance, current therapy and new approaches to the pulmonary disease.
Е. Л. Амелина,
А. Г. Чучалин
НИИ
пульмонологии Минздрава РФ, Москва
Ye. L. Amelina, A. G. Chuchalin
Pulmonology, Ministry of Health of the Russian Federation, Moscow
М
уковисцидоз (МВ) -
наследственное заболевание,
обусловленное системной
дисфункцией экзокринных желез.
Болезнь впервые была описана
сравнительно недавно, в 1938 г.
Патологоанатом Дороти Андерсен
описала кистозную дегенерацию
поджелудочной железы в сочетании с
легочной патологией у маленьких
детей . Тогда возникло английское
название болезни - Cystic fibrosis
(кистозный фиброз). В 1946 г. Farber
предложил термин
"муковисцидоз" (от лат. mucus -
слизь, viscus - вязкий), указывая на
роль повышения вязкости экскрета,
выделяемого экзокринными железами.
Однако еще раньше, в старинных
немецких сказаниях, указывалось,
что если при поцелуе ребенка
ощущается соленый привкус - ребенок
обречен .
Н
-нормальный ген
М
-ген муковисцидоза
Рис. 1. Аутосомно-рецессивный тип наследования при МВ.
За последние
годы стремительно развивалось
научное знание о МВ, механизме его
развития на клеточном и
молекулярном уровне. В настоящее
время известно, что МВ является
самым частым моногенным
заболеванием среди европейцев.
Каждый 25-й представитель
европейской расы является
носителем гена МВ.
Распространенность МВ наиболее
высока в Центральной Европе - 1
больной ребенок на 2000 родов .
Эпидемиологические
исследования по частоте случаев МВ
в России установили противоречивые
данные - от 1: 3860 новорожденных до 1:12 300 .
Рис. 2. Механизм транспорта ионов через апикальную мембрану эпителиальной клетки при МВ.
Прогресс в диагностике и лечении МВ привел к значительным изменениям продолжительности жизни при этом заболевании. В 1938 г. 70% заболевших погибали в течение первого года жизни. В 1996 г. средняя продолжительность жизни больных МВ в США и странах Западной Европы достигла 29 лет. Аналогичный показатель по России составляет лишь 16 лет . В центре МВ взрослых на базе Brompton Hospital наблюдали пациента, достигшего возраста 72 лет. Такое отставание связано с недостаточным развитием общенациональной сети специализированных центров МВ, отсутствием самостоятельной клиники МВ взрослых.
Этиология и патогенез
МВ развивается
в результате мутации гена,
расположенного на длинном плече
седьмой хромосомы. Тип
наследования -
аутосомно-рецессивный (рис. 1).
В настоящее время известно
более 400 мутаций, из которых в
Европе и России наиболее часто
встречается мутации F 508 (потеря
аминокислоты финилаланина в
позиции 508).
Подобное изменение структуры
ДНК приводит к нарушению функции
трансмембранного регулятора МВ
(МВТР) - белка, обеспечивающего
транспорт иона хлора через
апикальную часть мембраны
эпителиальной клетки (рис. 2).
Вследствие этого дефекта анионы
хлора задерживаются в клетке,
усиливают абсорбцию катионов
натрия и воды, "высушивая"
слизь, продуцируемую экзокринными
железами. Увеличение вязкости
экскрета приводит к закупориванию
протоков экзокринных желез,
накоплению экскрета и образованию
кист. Развивается картина
системной дисфункции экзокринных
желез.
Поражаются те органы, в
эпителиальных клетках которых
нарушена функция хлоридных
каналов. Это - верхние и нижние
дыхательные пути, потовыводящие
протоки, выводные протоки слюнных
желез, поджелудочной железы,
желчевыводящие пути, кишечник,
семявыносящие протоки.
Из-за блокады хлоридных каналов
не происходит реабсорбция ионов
хлора и натрия в потовыводящих
протоках, что приводит к
значительному повышению
концентрации этих ионов в 1 мл пота.
Этот феномен используется при
диагностике МВ. Следует также
помнить, что в жаркое время года у
таких больных при физической
нагрузке происходит значительная
потеря электролитов, что может
привести к коллапсу.
Поражение поджелудочной железы,
вызванное закупориванием ее
протоков густым, вязким секретом,
приводит к образованию кист и в
дальнейшем к кистозно-фиброзному
перерождению паренхимы
поджелудочной железы. В результате
развивается внешнесекреторная
недостаточность поджелудочной
железы с явлениями стеатореи,
мальабсорбции с сопутствующей
недостаточностью жирорастворимых
витаминов А, D, E, К, отставанием в
физическом развитии. В более
старшем возрасте из-за фиброзного
перерождения стромы поджелудочной
железы и при поражении островков
Лангерганса развивается
эндокринная недостаточность
поджелудочной железы, приводящая к
формированию сахарного диабета.
Поражение желчевыводящих протоков приводит к развитию билиарного цирроза с портальной гипертензией, выражающейся в варикозном расширении вен пищевода (возможно с кровотечением из них), асцитом, спленомегалией и гиперспленизмом. У всех больных МВ при ультразвуковом исследовании можно выявить картину холестаза, у 15% на этом фоне формируются камни желчного пузыря .


Рис.3.
Обзорная рентгенограмма больного
В., 15 лет, во время обострения
хронического
гнойно-воспалительного процесса в
легких (а) и после курса в/в
антибактериальной терапии (б).
Уменьшилась очаговая и
перибронхиальная инфильтрация,
однако сохраняются грубое усиление
и деформация легочного рисунка,
расширение корней легких,
гипервоздушность.
Основной
механизм поражения кишечника
заключается в том, что из-за
нарушенного транспорта ионов
натрия и хлора содержание
электролитов и жидкости в просвете
кишечника резко снижено, что может
привести к мекониальной кишечной
непроходимости в младенчестве,
выпадению прямой кишки в детстве,
развитию кишечной непроходимости
на уровне илеоцекального угла в
более старшем возрасте.
Двусторонняя атрезия
семявыносящих протоков приводит к
азооспермии и мужскому бесплодию у
97% больных мужчин .
Почти все больные МВ страдают
синуситами, у 30% больных выявляется
полипоз носа .
Патология легких занимает
особое место в клинической картине
МВ. Именно
поражение легких с последующими
осложнениями приводит к 70% смертей
при МВ .
Патологический процесс в легких
начинается после рождения ребенка,
когда в просвете бронхов
формируется густой и вязкий секрет,
приводящий к нарушению
мукоцилиарного клиренса.
Возникающий мукостаз является
благоприятной основой для развития
инфекционно-воспалительных
процессов. Хронический гнойный
бронхит,частые бронхопневмонии
приводят к формированию
ателектазов,
бронхиоло-бронхоэктазов, в более
позднем возрасте возникают
осложнения в виде пневмоторакса,
легочного кровотечения. По мере
прогрессирования патологических
изменений в бронхолегочной системе
нарастает
вентиляционно-перфузионный
дисбаланс, возникает гипоксия,
легочная гипертензия и формируется
хроническое легочное
сердце. Все это ведет к нарастанию
дыхательной и сердечно-сосудистой
недостаточности, являющейся
непосредственной причиной смерти
больного.
Клинические проявления
Большое число
мутаций, в различной степени
воздействующих на количество и
качество белка МВТР в
эпителиальных клетках, определяет
разнообразие клинических
проявлений МВ.
Клинические проявления МВ могут
возникнуть как в раннем
младенческом возрасте, так и в
более поздний период жизни
больного. При относительно
благополучном течении болезни МВ
может длительно протекать
бессимптомно, в некоторых случаях
диагноз ставится при обследовании
по поводу хронического синусита
или мужского бесплодия.
В неонатальном периоде обращают
на себя внимание незначительное
прибавление массы тела, признаки
мальабсорбции. В 10% наблюдений МВ
начинается с мекониального илеуса
в раннем младенчестве .
В постнатальном периоде ведущим
проявлением МВ становятся
повторные бронхолегочные инфекции.
Диагноз МВ ставится на основе
характерной клинической картины в
сочетании с положительным потовым
тестом. Классическую
диагностическую триаду при МВ
составляют:
- положительный потовый тест (хлориды пота более 60 мэкв/л);
- легочная патология инфекционно-воспалительного характера;
- кишечный синдром.
Диагноз подтверждается:
- отягощенным семейным анамнезом;
- положительным результатом генетического анализа;
- повышенным содержанием иммунореактивного трипсина в крови (исследование имеет диагностическое значение при неонатальном скрининге, так как от рождения до 8 нед жизни эти показатели повышены);
- азооспермией, вызванной обструкцией семявыносящих протоков.
При постановке
диагноза МВ взрослым следует
обратить внимание на характерный
вид больного. Это, как правило,
молодые пациенты с признаками
пониженного питания, небольшого
роста, имеющие длительный анамнез
хронического бронхита,
бронхоэктазов, хронического
гайморита или хронического
панкреатита. При активном
расспросе можно выявить жалобы на
диарею, у девушек возможно
нарушение менструального цикла.
При
физикальном исследовании пациента
выявляются астеническое
телосложение, бочкообразная форма
грудной клетки, деформация
дистальных фаланг в виде
"барабанных палочек". Могут
иметь место одышка, акроцианоз. При
аускультации над легкими
выслушиваются разнокалиберные
хрипы. При пальпации живота можно
выявить увеличение размеров
печени, селезенки.
При рентгенологическом
исследовании определяется
гипервоздушность легких, видны
участки инфильтрации или
ателектаза, утолщение стенок
бронхов, возможна картина
пневмоторакса. При проведении
компьютерной томографии
обнаруживаются множественные
бронхоэктазы.
Исследования функции внешнего
дыхания выявляют обструктивные
нарушения в сочетании с
увеличением остаточного объема.
Возможны также рестриктивные
изменения как результат
развившегося пневмосклероза.
Диффузионная способность легких
снижается на более поздних стадиях
заболевания за счет гиповентиляции
.
На электрокардиограмме видны
признаки тахикардии, перегрузки
правых отделов сердца.
Микробиологический анализ
мокроты крайне важен для
определения возбудителя
инфекционного процесса в
бронхолегочной системе, для
прогноза течения болезни и
прицельного назначения
антибактериальной терапии.
Антибактериальные препараты,
рекомендуемые для лечения больных
МВ
| Saphilococcus aureus | Клоксациллин | 25 мг/кг/сут |
| Флуклоксациллин | 70 мг/кг/сут | |
| Фузидиновая кислота | 50 мг/кг/сут | |
| Клиндамицин | 20 - 40 мг/кг/сут | |
| Рифампицин | 15 г/кг/сут | |
| Цефалопориновые антибиотики 1-го и 2-го поколения | 100 мг/кг/сут | |
| Pseudomonas aeruginosa | ||
| Профилактика хронической колонизации | Ципрофлоксацин | 20 - 50 мг/кг/сут внутрь |
| Колистин | 1 - 2 млн ЕД в ингаляциях дважды в сутки | |
| Хроническая колонизация | ||
| Лечение обострений (3 нед) | Азлоциллин | 250 - 500 мг/кг/сут внутривенно |
| или | Пиперациллин | 300 мг/кг/сут внутривенно |
| Амикацин | 15 мг/кг/сут внутривенно | |
| плановые курсы | Гентамцин | 8 - 12 мг/кг/сут внутривенно |
| 2 нед каждые 3 мес | Тобрамицин | 10 - 20 мг/кг/сут внутривенно |
| 2 противосинегнойных | Нетилмицин | 10 - 12 мг/кг/сут внутривенно |
| препарата | Цефсулодин | 100 - 150 мг/кг/сут внутривенно |
| Цефтазидим | 100 - 250 мг/кг/сут внутривенно | |
| Азтреонам | 150 - 250 мг/кг/сут внутривенно | |
| Тиенамицин | 50 - 75 мг/кг/сут внутривенно | |
| Ципрофлоксацин | 15 - 50 мг/кг/сут внутрь, внутривенно | |
| Длительная терапия | ||
| Колистин | 1 - 2 млн ЕД в ингаляциях | |
| Гентамицин | 160 - 240 мг дважды в сутки | |
| Тобрамицин | 100 - 300 мг | |
| Карбенициллин | 1 - 2 г |
Микробный пейзаж при МВ достаточно характерен. В раннем детском возрасте доминирует золотистый стафилококк (Staphilococcus aureus), затем присоединяется гемофильная палочка (Наemofilus influaenzae), в подростковом возрасте появляется синегнойная палочка (Pseudomonas aeruginosa). В последние годы, особенно в странах Западной Европы и Америки, часто высевается Pseudomonas cepacia, или Burgholderia cepacia, резистентная к большинству антибиотиков . Присоединение синегнойной инфекции может иметь различные последствия для больного: от бессимптомного носительства до, чаще, значительного ухудшения течения заболевания с выраженной активизацией воспалительного процесса и ухудшением функциональных показателей.
Лечение
На основании
клинических, функциональных и
микробиологических данных
строится тактика лечения МВ.
Основной целью проводимой
терапии являются:
- уменьшение бронхиальной обструкции;
- борьба с инфекцией;
- улучшение нутритивного статуса больного.
Следует
проводить активное лечение
сопутствующих осложнений,
компенсировать возникающую
дыхательную и сердечную
недостаточность, обеспечивать
максимальный комфорт для больного
в терминальном периоде
заболевания.
В стадии разработки находятся
новые, революционные методы
лечения МВ (например, генная
терапия).
Снижение бронхиальной
обструкции
проводится при помощи
нескольких групп препаратов. Это -
муколитики, бронходилататоры в
сочетании с приемами
кинезитерапии.
Муколитики - препараты,
уменьшающие вязкость мокроты
(N-ацетилцистеин и его аналоги) -
применяются в таблетках,
ингаляциях и внутривенно.
С 1994 г. используется ДНКаза -
препарат, расщепляющий ДНК
разрушенных нейтрофилов в просвете
бронха. Как показали законченные
недавно многоцентровые
исследования, ежедневные
двухкратные ингаляции 2,5 мг
препарата приводит к улучшению
самочувствия больного, уменьшению
числа обострений, улучшению
функциональных показателей и в
итоге - качества жизни больного .
Бронходилататоры также
используются для улучшения
бронхиальной прходимости. Это -
препараты b-агонистов (сальбутамол,
сальметерол) и М-холинолитиков
(ипратропиума бромид).
Эффективность их применения
определяется показателями
обратимости обструкции после
ингаляции препарата при
исследовании функции внешнего
дыхания. Бронходилататоры чаще
всего используются в комплексе
ежедневных процедур, включающих
ингаляции муколитиков и упражнения
кинезитерапии.
Кинезитерапия - это вид
физиотерапии, направленный на
мобилизацию и эвакуацию мокроты из
бронхиального дерева. Наиболее
распространенными формами
кинезитерапии являются цикл
активного дыхания и хаффинг,
аутогенный дренаж, постуральный
дренаж в сочетании с перкуссионным
массажем. Возможно использование
флаттера и PEP -маски (positeve expiratory
pressure) для создания положительного
давления на выдохе и
предотвращения экспираторного
коллапса .
Борьба с инфекцией.
Введение
в арсенал терапевтов антибиотиков
в 1940 г. было самым значительным
событием, изменившим прогноз
больных МВ. Антибиотики и сейчас
являются краеугольным камнем в
лечении этой патологии.
Антибактериальная терапия
назначается с учетом результата
посева мокроты прерывистыми
курсами при обострении или в
плановом порядке, а также в составе
базисной терапии для продления
периода ремиссии между
обострениями (см. таблицу).
Фармакокинетика
антибактериальных препаратв при МВ
изменена: из-за ускорения
метаболизма лекарственных
препаратов в печени и увеличения
почечного клиренса максимальная
концентрация вводимого
антибиотика в сыворотке крови
больного МВ меньше предполагаемой.
Поэтому при МВ требуются большие
дозы препарата с максимальной
частотой введения.
Антибактериальная терапия при
МВ опирается на результаты
микробиологического исследования
мокроты с определением
чувствительности к антибиотикам
выделенного возбудителя .
При лечении обострения
препаратами выбора для
стафилококковой инфекции являются
пенициллиназаустойчивые
пенициллины (флуклоксациллин,
диклоксациллин), цефалоспорины 1-го
и 2-го поколения (цефалексин,
цефаклор), используются также
доксициклин, клиндамицин,
рифампицин,фузидин. В последние
годы из мокроты у больных МВ
высевается иногда
метициллинрезистентный
стафилококк. В таком случае
препаратом выбора становится
ванкомицин.
При колонизации синегнойной
палочки терапия, как правило,
проводится с применением двух
противосинегнойных препаратов,
внутривенно, курсом не менее 14 дней.
Это препараты из группы
цефалоспоринов 3 -го поколения
(цефтазидим), аминогликозидов
(гентамицин, сизомицин, амикацин),
карбапенемов (тиенам, меронем).
Препарат из группы дифторированных
хинолонов - ципрофлоксацин -
единственный противосинегнойный
препарат, производимый и в
таблетированной форме, что очень
важно для амбулаторного ведения
больных.
Лечение обострений начинают при
повышении температуры, усилении
кашля, усугублении одышки,
увеличении количества мокроты.
Объективными показателями
обострения служат: десатурация
кислорода, снижение объема
форсированного выдоха в секунду на
10 % и более, изменения в физикальной
и рентгенологической картине.
Во многих центрах МВ курс
внутривенной терапии при
носительстве синегнойной палочки
проводят каждые 3 мес в плановом
порядке. Внутривенная
антибактериальная терапия может
проводиться не только в условиях
стационара, но и на дому.
Вне обострения рекомендуется
длительная ингаляция
противосинегнойных препаратов
(колимицин, карбенициллин,
гентамицин) для подавления
постоянно текущего инфекционного
процесса. Длительные исследования
эффективности и безвредности
ингаляционной антибактериальной
терапии доказали стабилизацию
клинических проявлений и улучшение
функциональных показателей, а
также уменьшение колонизации
синегнойной палочки. В связи с
отсутствием системного
воздействия побочные действия
ингаляционной антибактериальной
терапии минимальны.
Эффективность ингаляционной
терапии в большой степени зависит
от используемого ингалятора.
Сочетание небулайзера и
компрессора имеет ряд преимуществ
перед ультразвуковым ингалятором.
При использовании небулайзера
достигается лучшая дисперсия, при
которой ингалируемый препарат
проникает в нижние дыхательные
пути; кроме того, ультразвуковой
ингалятор несколько нагревает
препарат, что может изменить свойства антибиотика.
Ежедневное лечение больного МВ
должно выглядеть так: процедуры
начинаются с ингаляции
бронходилататора, если это
показано; затем - ингаляции и/или
таблетированный прием муколитика;
через 10 - 15 мин - кинезитерапия,
откашливание; после паузы -
ингаляция антибиотика.
Улучшение нутритивного
статуса
очень важно для общего
самочувствия пациента и течения
инфекционного процесса, развития
дыхательной мускулатуры, а в итоге -
для прогноза больного МВ .
Для его коррекции необходимо:
- выявить экзокринную недостаточность поджелудочной железы;
- проводить постоянную заместительную терапию ферментными препаратами нового поколения. Это - микросферические ферменты с pH-чувствительной оболочкой (креон, панцитрат). Препарат назначается с каждым приемом пищи в дозе до 2000 ед. липазы на 1 кг массы тела больного. Если при подобной дозировке сохраняются симптомы мальабсорбции или есть признаки гиперацидного гастрита, к терапии добавляют блокаторы H2-рецепторов (циметидин, ранитидин) или ингибиторы протонной помпы (омепразол);
- при адекватной заместительной терапии в диете больных МВ не должно быть ограничений. Наоборот, с учетом постоянно текущего инфекционного процесса калораж питания при МВ должен составлять 120 - 150 % от необходимого, 35% из них за счет жиров;
- необходим дополнительный прием витаминов А, Д, Е, К - как правило, назначают двойное количество обычной дневной нормы.
- при неэффективности перечисленных действий, если у больного значительно уменьшается масса тела, назначают высококалорийные пищевые добавки в форме коктейлей, в дозе, возмещающей 800 ккал/сут для взрослых. При необходимости прибегают к зондовому кормлению в ночное время с использованием пищеводного или желудочного зонда.
Новым
направлением в лечении МВ является
применение противовоспалительной
терапии. Так как бронхиальная
обструкция при МВ в большой степени
обусловлена гиперактивной
воспалительной реакцией,
представляется целесообразным
применение стероидных и
нестероидных
противовоспалительных препаратов.
В американском исследовании,
продолжавшемся 4 года и
закончившемся недавно, выявлено
значительное улучшение
показателей функций внешнего
дыхания у пациентов,
систематически принимающих
ибупрофен, а также уменьшение
необходимости антибактериальных
препаратов .
Кортикостероидные препараты
применяются для лечения больных МВ
при сопутствующей бронхиальной
астме или аллергическом
бронхолегочном аспергиллезе. В
4-годичном исследовании по
выявлению эффективности системной
терапии кортикостероидами в дозе 2
мг/кг через день был получен
значительный клинический и
функциональный эффект. Однако по отсроченным
данным (через 6 лет) были выявлены
отставание в росте, остеопороз,
катаракта у группы больных,
получавших стероиды .
Кортикостероидные препараты
рекомендуется применять короткими
курсами при лечении обострений. В
настоящее время исследуется роль
ингаляционной стероидной терапии в
лечении МВ.
Лечение осложнений.
При
прогрессировании легочной
патологии при МВ развиваются такие
осложнения, как гипоксемия,
приводящая к легочной гипертензии
и развитию легочного сердца. В этом
случае проводятся длительная
кислородотерапия (в соответствии с
показателями газового состава
крови), лечение ингибиторами
ангиотензинпревращающего фермента
(каптоприл, эналаприл), а также
традиционное лечение
развивающейся недостаточности
кровообращения.
Выраженное воспаление
трахеобронхиального дерева,
особенно в зонах бронхоэктазии,
часто приводит к легочному
кровотечению, которое, однако,
редко является непосредственной
причиной смерти больного. При
неэффективности консервативного
лечения рекомендуется проведение
ангиографии с эмболизацией
бронхиальной артерии или
хирургическое вмешательство.
Пневмоторакс - это довольно
частое осложнение МВ у взрослых,
развивающееся из-за разрыва
субплевральных булл. После
удаления свободного воздуха из
плевральной полости при повторных
пневмотораксах осуществляется
химический или хирургический
плевродезис. Сейчас в странах, где
проводится трансплантация легких,
показания к этой манипуляции
сужены.
Трансплантация
является еще
одним шансом для больных МВ после
того, как ресурсы медикаментозной
терапии исчерпаны.
Показаниями к трансплантации
являются выраженная дыхательная
недостаточность с объемом
форсированного выдоха в 1 с менее 30%,
отсутствие противопоказаний,
активное желание больного .
При трансплантации
производится пересадка обоих
легких, возможна также пересадка
комплекса легкие - сердце с
последующей процедурой
"домино", т. е. с пересадкой
сердца больного МВ другому
реципиенту. В связи с выраженной
нехваткой донорских органов иногда
проводится пересадка от живых
доноров (по одной доле от каждого из
родителей), однако эта операция
вызывает множество этических
возражений и проводится крайне
редко .
Еще одной надеждой для больных
МВ и их врачей является генная
терапия . Синтезирован ген белка
МВТР, проводятся активные попытки
ввести этот ген в эпителиальные
клетки бронхов. Доказано, что даже
10% уровень нормального МВТР может
обеспечить физиологическую
функцию легких. Проведены первые
клинические испытания с
использованием вектора
аденовируса (США, Канада) и
липосомами (Англия, Франция).
Клинически значимого результата
пока не получено , однако
исследования продолжаются, так как
в случае успеха наступит новый этап
в лечении МВ - этап этиологического
подхода к лечению этого
заболевания.
Литература:
1. Andersen DH. Cystic
fibrosis of the pancreas and its relation to celiac disease. A
clinical and pathologic study. Am J Dis Child 1938;56:344-99.
2. Чучалин А. Г., Самильчук Е. И.
Муковисцидоз- - состояние проблемы.
Тер. архив - 1993;65;(3):3-8.
3. Hodson ME, Geddes DM (Еds), London: Chapman and Hall,
1995.
4. Потапова О. Ю. Автореферат -
Молекулярно-генетический анализ
кистозного фиброза в России - С.П.
1994, с. 24.
5. Петрова Н. В., Материалы
научно-практической конференции
РДКБ - М - 1995, с. 96.
6. Капранов Н. И. Рачинский С. В.
Муковисцидоз - М. - 1995.
7. Cystic Fibrosis Foundation. 1995. Patient Registry 1994
Annual Data Report. Bethesda, Maryland.
8. Taussig LM. The reproductive system, in Cystic Fibrosis
Brugman, S. M. (Еd. L. M.
Taussig), Thieme-Stratton, New York 1984;324-7.
9. Davis PB, et al. Cystic Fibrosis, Am J Respir Crit Care
Med 1996;154:1229-56.
10. Warner JO, et al. Cystic fibrosis in children, in
Respiratory Medicine (second edition), London
1995:1330-40.
11. van Haren EHJ, et al. Bronchodilator response in adult
patients with cystic fibrosis: effects on large and small
airways. Eur J Respir Dis 1991;4:301-7.
12. Govan JWR, et al. Evidence of transmission of
Pseudomonas cepacia by social contact in cystic fibrosis. Lancet
1993;342:15.
13. Hodson ME. Aerosolized dornase alfa (rhDNase) for
therapy of cystic fibrosis. Am J 1995;151:70-4.
14. Pryor JA and Webber BA. Physiotherapy for cystic
fibrosis-which technique? Physiotherapy 1992;78:105-8.
15. Webb AK. The treatment of pulmonary infection in cystic
fibrosis Scand J Infect Dis Suppl 1995;96:24-7.
16. Cysyic Fibrosis Trust. Management of cystic fibrosis in
adults UK 1995.
17. Konstan MW, et al. 1995 Effect of high-dose ibuprofen
in patients with cystic fibrosis.
18. Niolaizik WH, MH. Schoni, 1996 Pilot study to assess
the effect of inhaled corticosteroids on lung function in
patients with cystic fibrosis J Pediatr 128:271-4.
19. Kotloff, Zuckerman. Lung transplantation for cystic
fibrosis: special considerations Chest March 1996;109(3):787-98.
20. Southern KW. Gene therapy for cystic fibrosis: current
issues. Brit J Hosp Med 1996;55(8):495-9.