Penyakit Pid. Defisiensi imun primer
Defisiensi imun primer(PID) adalah kelainan bawaan sistem kekebalan berhubungan dengan defek genetik pada satu atau lebih komponen sistem imun, yaitu komplemen, fagositosis, imunitas humoral dan seluler. Gambaran umum dari semua jenis PID adalah adanya infeksi kronis berulang yang mempengaruhi berbagai organ dan jaringan dan, sebagai aturan, disebabkan oleh mikroorganisme oportunistik atau oportunistik, yaitu flora virulen rendah. PID sering dikaitkan dengan kelainan anatomis dan fungsional sistem tubuh lain dan memiliki beberapa ciri khas yang memungkinkan untuk membuat diagnosis awal pada bayi baru lahir tanpa pemeriksaan imunologi laboratorium (lihat tabel).
| Data survei | Diagnosa awal |
| Cacat jantung bawaan, hipoparatiroidisme, wajah khas | Sindrom Dee Georgie |
| Abses dingin, wajah khas, kista udara paru-paru | Sindrom hiper-IgE |
| Penyembuhan luka pusar yang lambat | Defek adhesi leukosit (sindrom LAD) |
| Eksim + trombositopenia | Sindrom Wiskott-Aldrich |
| Ataksia + telangiektasia | Sindrom Louis-Bar |
| Albinisme parsial mata dan kulit, butiran raksasa di fagosit | Sindrom Chediak-Higach |
| Tidak ada bayangan timus pada fluoroskopi, kelainan pada perkembangan tulang rusuk | Defek adenosin deaminase |
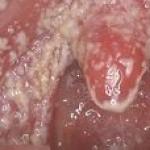
| Lesi pada kulit dan selaput lendir dengan kandidiasis, kandidiasis autoimun, endokrinopati | mukokutan kronis |
Komponen yang berbeda dari sistem kekebalan dapat mengambil bagian yang tidak seimbang dalam eliminasi mikroba dari suatu makroorganisme. Oleh karena itu, berdasarkan sifat proses infeksi, seseorang juga dapat menilai terlebih dahulu komponen kekebalan mana yang tidak cukup bekerja. Jadi, dengan perkembangan selama hari-hari pertama kehidupan seorang anak, proses inflamasi purulen pada kulit dan selaput lendir yang disebabkan oleh kokus piogenik, ada alasan untuk memikirkan keberadaan cacat lahir sistem fagosit. Mereka juga ditandai dengan penyembuhan luka pusar yang sangat lambat dan jatuhnya tali pusar. Proses infeksi yang berhubungan dengan defek pada produksi antibodi biasanya berkembang pada paruh kedua kehidupan anak setelah hilangnya imunoglobulin ibu dari aliran darah. Paling sering, infeksi ini disebabkan oleh mikroorganisme piogenik yang dienkapsulasi (streptokokus, pneumokokus, Haemophiluls influlenzae, dll.) Yang mempengaruhi saluran pernapasan bagian atas dan bawah. Infeksi neisserial yang persisten sering dikaitkan dengan cacat lahir pada komponen komplemen C5-C9. Proses infeksi yang sering disebabkan oleh virus dan patogen intraseluler lainnya menunjukkan adanya cacat pada sistem kekebalan T. Ini juga dapat dibuktikan dengan kandidiasis mukokutan. Triad - pneumonia kronis, jangka panjang, diare dan kandidiasis yang sulit diobati - selalu menjadi dasar asumsi adanya cacat bawaan pada limfosit-T. Cacat gabungan dari sistem kekebalan T dan B dicirikan oleh kursus berat proses infeksi yang berkembang pada bulan pertama kehidupan anak. Tanpa pengobatan yang tepat, anak biasanya meninggal dalam tahun pertama kehidupan.
Pemeriksaan laboratorium dan imunologis dilakukan untuk mengidentifikasi kelainan spesifik pada sistem kekebalan tubuh dan untuk memastikan diagnosis klinis. Diagnostik awal dapat dilakukan dengan menggunakan panel tes laboratorium skrining.
Penggunaan panel tes laboratorium skrining dimungkinkan di hampir semua rumah sakit daerah atau kota di mana terdapat laboratorium diagnostik klinis. Namun, analisis mendalam hanya dapat dilakukan di institusi medis dan profilaksis khusus dengan laboratorium imunologi klinis modern. Pada pasien dengan dugaan PID, aktivitas fungsional fagosit, sistem kekebalan T dan B harus diperiksa secara rinci. Secara lebih rinci, pendekatan metodologis untuk menilai kekebalan akan dijelaskan di bagian yang sesuai.
Saat ini, lebih dari 70 cacat bawaan dari sistem kekebalan telah diidentifikasi, dan jumlahnya kemungkinan akan bertambah seiring dengan peningkatan metode imunodiagnostik molekuler. PID adalah penyakit yang relatif jarang: frekuensinya rata-rata 1 / 25000-1 / 100000. Pengecualian adalah defisiensi IgA selektif, yang terjadi dengan frekuensi 1 / 500-1 / 700. Studi tentang PID sangat menarik untuk imunologi teoretis dan terapan. Analisis mekanisme genetik molekuler yang mendasari cacat ini memungkinkan untuk mengidentifikasi mekanisme baru yang mendasar dari fungsi sistem kekebalan dan, oleh karena itu, untuk mengembangkan pendekatan baru untuk imunodiagnostik dan imunoterapi penyakit yang terkait dengan gangguan sistem kekebalan.
Imunodefisiensi sekunder (SID). Yang cukup menarik untuk imunologi klinis adalah studi tentang SPID, yang, secara kuantitatif, tidak diragukan lagi dominan di antara imunodefisiensi. SPD dipahami sebagai gangguan pada sistem kekebalan yang berkembang pada periode pascakelahiran akhir atau pada orang dewasa dan, seperti yang diyakini secara umum, bukan merupakan akibat dari beberapa cacat genetik. Di antara SPE, tiga bentuk dapat dibedakan secara kondisional: didapat, diinduksi dan spontan. Contoh paling mencolok dari bentuk pertama adalah sindrom imunodefisiensi (AIDS), yang berkembang sebagai akibat dari kerusakan jaringan limfoid manusia oleh virus yang sesuai. Spesies yang diinduksi adalah kondisi seperti itu, yang kemunculannya dikaitkan dengan penyebab spesifik: penyinaran sinar-X, kortikosteroid, sitostatika, trauma dan pembedahan, serta gangguan kekebalan yang berkembang sekunder akibat penyakit yang mendasarinya (diabetes, penyakit ginjal dan hati, proses ganas, dll.). Bentuk-bentuk VID yang diinduksi, sebagai suatu peraturan, bersifat sementara, dan ketika penyebab penyebab dihilangkan, dalam banyak kasus, pemulihan kekebalan yang lengkap terjadi. Berbeda dengan yang diinduksi, bentuk spontan VIS ditandai dengan tidak adanya alasan yang jelas, yang menyebabkan pelanggaran reaktivitas imunologis. Seperti pada PID, bentuk defisiensi imun ini memanifestasikan dirinya dalam bentuk proses kronis, berulang, infeksi dan inflamasi pada aparatus bronkopulmonalis dan sinus paranasal, saluran urogenital dan gastrointestinal, mata, kulit dan jaringan lunak, yang disebabkan, seperti PID, oleh oportunistik atau mikroorganisme oportunistik dengan sifat biologis atipikal dan sering dengan resistensi antibiotik multipel. Dalam istilah kuantitatif, bentuk spontan adalah bentuk dominan dari SPE.
- Penilaian status kekebalan pada imunodefisiensi
Seperti yang telah dicatat, studi tentang status kekebalan pada defisiensi imun harus mencakup studi tentang jumlah dan aktivitas fungsional komponen utama sistem kekebalan, yang memainkan peran utama dalam pertahanan anti-infeksi tubuh. Ini termasuk sistem fagositik, sistem komplemen, sistem kekebalan T dan B. Metode yang digunakan untuk menilai fungsi sistem ini secara kondisional dibagi oleh RV Petrov et al. (1984) untuk tes tingkat 1 dan 2. Menurut para penulis ini, tes level 1 bersifat indikatif dan ditujukan untuk mengidentifikasi cacat berat pada sistem kekebalan tubuh; Tes Level 2 berfungsi dan ditujukan untuk mengidentifikasi "kerusakan" spesifik dalam sistem kekebalan. Kami merujuk pada tes tingkat 1 sebagai metode yang bertujuan untuk mengidentifikasi produk dari fungsi sistem kekebalan yang sesuai, yang menentukan efek antimikrobanya. Tes level 2 bersifat opsional. Mereka secara signifikan memperkaya informasi tentang fungsi sistem kekebalan yang sesuai.
Tes tingkat 1 untuk menilai fagositosis meliputi definisi:
- jumlah absolut neutrofil dan monosit;
- intensitas penyerapan mikroba oleh neutrofil dan monosit;
- kemampuan fagosit untuk membunuh mikroba.
Proses fagositosis terdiri dari beberapa tahap: kemotaksis, adhesi, penyerapan, degranulasi, pembunuhan dan penghancuran objek. Studi mereka memiliki signifikansi tertentu dalam menilai proses fagositosis, karena ada defisiensi imun yang terkait dengan adanya kerusakan di hampir setiap tahap. Hasil utama dari kerja neutrofil dan monosit adalah pembunuhan dan penghancuran mikroba, yaitu, fagositosis lengkap. Untuk menilai pembunuhan, disarankan untuk menentukan pembentukan spesies oksigen reaktif dalam proses fagositosis. Jika tidak mungkin untuk menentukan spesies oksigen reaktif menggunakan chemiluminescence, pembentukan radikal superoksida dapat dinilai dengan reduksi nitro blue tetrozolium. Tetapi dalam kasus ini, harus diingat bahwa pembunuhan mikroba dalam fagosit dilakukan menggunakan mekanisme yang bergantung pada oksigen dan tidak bergantung pada oksigen, yaitu, penentuan spesies oksigen reaktif tidak memberikan informasi lengkap tentang proses ini.
Tes penilaian fagositosis tingkat 2 meliputi definisi berikut:
- intensitas kemotaksis fagosit;
- ekspresi molekul adhesi (CD11a, CD11b, CD11c, CD18) pada membran permukaan neutrofil.
Tes penilaian tingkat pertama sistem kekebalan B meliputi definisi:
- imunoglobulin G, A, M dalam serum darah;
- imunoglobulin E dalam serum;
- penentuan persentase dan jumlah absolut limfosit B (CD19, CD20) dalam darah tepi.
Penentuan tingkat imunoglobulin masih merupakan metode yang penting dan dapat diandalkan untuk menilai sistem B dari sistem kekebalan tubuh. Ini dapat dianggap sebagai metode utama untuk mendiagnosis semua bentuk defisiensi imun yang terkait dengan biosintesis antibodi.
Tes penilaian tingkat 2 dari sistem kekebalan B mencakup definisi berikut:
- subkelas imunoglobulin, terutama IgG;
- sekretori IgA;
- rasio rantai kappa dan lambda;
- antibodi spesifik terhadap protein dan antigen polisakarida;
- kemampuan limfosit untuk memberikan respon proliferasi terhadap mitogen B- (staphylococcus, enterobacterial lipopolysaccharide) dan T-B- (lakonos mitogen).
Penentuan subkelas IgG memiliki beberapa nilai diagnostik, karena pada kadar IgG normal mungkin terdapat defisiensi subkelas imunoglobulin. Pada orang seperti itu, dalam beberapa kasus, keadaan imunodefisiensi diamati, dimanifestasikan dalam peningkatan morbiditas infeksi. Dengan demikian, IgG2 adalah subkelas dari imunoglobulin G, yang sebagian besar mengandung antibodi terhadap polisakarida bakteri berkapsul (Haemophiluls influlenzae, Steptococculs pneulmoniae). Oleh karena itu, defisiensi yang terkait dengan IgG2 serta IgA menyebabkan peningkatan morbiditas. infeksi pernafasan... Gangguan rasio subkelas IgA dan rasio rantai kappa dan lambda juga dapat menyebabkan keadaan imunodefisiensi. Informasi penting tentang keadaan imunitas humoral disediakan oleh definisi antibodi terhadap protein bakteri dan antigen polisakarida, karena tingkat pertahanan tubuh terhadap infeksi khusus ini tidak tergantung pada tingkat umum imunoglobulin, tetapi pada jumlah antibodi terhadap agen penyebabnya. Hal ini terutama ditunjukkan dengan jelas oleh data yang menunjukkan bahwa perkembangan sinusitis kronis dan otitis media hanya bergantung pada defisiensi antibodi IgG3 terhadap Moraxella catarrhalis pada pasien tersebut. Contoh lain yang jelas tentang pentingnya menentukan antibodi spesifik dapat berupa data yang membuktikan bahwa pada individu yang menderita proses infeksi saluran pernapasan yang sering, dengan tingkat normal semua kelas imunoglobulin, titer antibodi terhadap Haemophiluls influlenzae berkurang secara signifikan.
Informasi berharga tentang keadaan kekebalan humoral dapat diperoleh tidak hanya dengan menentukan tingkat imunoglobulin, subkelasnya, atau antibodi terhadap antigen tertentu, tetapi juga dengan mempelajari sifat fungsionalnya. Ini termasuk, pertama-tama, sifat antibodi seperti afinitas, di mana kekuatan interaksi antibodi dengan antigen sangat bergantung. Produksi antibodi afinitas rendah dapat menyebabkan perkembangan keadaan imunodefisiensi. Kami telah menunjukkan bahwa pada individu yang sering dan untuk waktu yang lama menderita penyakit saluran pernapasan, dengan tingkat imunoglobulin normal, tingkat antibodi yang sedikit meningkat terhadap peptidoglikan St.aulreuls, Str.pneulmoniae, Br.catarrhalis, afinitas antibodi terhadap mikroba ini berkurang secara signifikan.
Sifat fungsional yang penting adalah aktivitas opsonisasi imunoglobulin. Sebagaimana dicatat, neutrofil adalah tokoh sentral dalam pertahanan tubuh terhadap mikroba ekstraseluler. Namun, kinerja fungsi ini sangat tergantung pada aktivitas opsonisasi serum darah, di mana imunoglobulin dan komplemen memainkan peran utama dalam aktivitas ini. Dalam sebuah penelitian terhadap 30 pasien dengan bakteremia yang disebabkan oleh bakteri gram negatif, ditemukan bahwa neutrofil pasien ini memiliki kemampuan yang berkurang untuk membunuh E. coli. Ini hanya bergantung pada ketidakmampuan serum darah pasien untuk opsonisasi, karena penambahan serum donor yang sehat ke neutrofil pasien ini sepenuhnya mengembalikan kemampuan neutrofil untuk membunuh E. coli.
Tes tingkat 1 untuk menilai sistem kekebalan T mencakup definisi berikut:
- jumlah total limfosit;
- persentase dan jumlah absolut limfosit T dewasa (CD3) dan dua subpopulasi utamanya: helper/induser (CD4) dan sel pembunuh/penekan (CD8);
- respon proliferatif terhadap T-mitogen utama: phytohemagglutinin dan concanavalin A.
Saat menilai sistem kekebalan B, kami merekomendasikan penentuan jumlah limfosit B, serta tingkat imunoglobulin, sebagai tes tingkat 1. Karena yang terakhir adalah produk akhir utama sel B, ini memungkinkan untuk mengevaluasi sistem kekebalan B dari aspek kuantitatif dan fungsional. Pendekatan ini masih sulit diterapkan dalam kaitannya dengan sistem kekebalan T, karena produk akhir utama limfosit T adalah sitokin, dan sistem untuk penentuannya masih kurang tersedia untuk laboratorium praktis imunologi klinis. Namun demikian, penilaian aktivitas fungsional sistem kekebalan T adalah tugas yang sangat penting, karena dapat dikurangi, kadang-kadang bahkan secara signifikan, dengan jumlah sel T yang normal dan subpopulasinya. Metode untuk menilai aktivitas fungsional limfosit T agak rumit. Yang paling sederhana, menurut kami, adalah reaksi transformasi ledakan dengan menggunakan dua T-mitogen utama: phytohemagglutinin dan concanavalin A. Respon proliferasi limfosit T terhadap mitogen berkurang di hampir semua proses infeksi dan inflamasi kronis, ganas penyakit, terutama sistem hematopoietik; dengan semua jenis terapi imunosupresif, dengan AIDS dan dengan semua imunodefisiensi sel T primer.
Untuk tes tingkat 2 untuk menilai sistem kekebalan T, kami menyertakan definisi:
- produksi sitokin (interleukin-2, (IL-2), IL-4, IL-5, IL-6, gamma-interferon, tumor necrosis factor (TNF), dll.);
- molekul aktivasi pada membran permukaan limfosit-T (CD25, HLA-DR);
- molekul adhesi (CD11a, CD18);
- respons proliferatif terhadap antigen spesifik, paling sering terhadap toksoid difteri dan tetanus;
- reaksi alergi menggunakan tes kulit dengan sejumlah antigen mikroba.
Tidak diragukan lagi, penentuan produksi sitokin oleh limfosit dan makrofag harus menjadi metode metodologis utama dalam imunodiagnosis penyakit yang terkait dengan gangguan sistem kekebalan. Identifikasi sitokin dalam beberapa kasus akan memungkinkan untuk menegakkan diagnosis penyakit dan mekanisme gangguan kekebalan dengan lebih akurat.
Penentuan sitokin pro-inflamasi seperti TNF, IL-1 dan interferon gamma juga penting. Peran mereka sangat besar dalam etiopatogenesis berbagai proses inflamasi akut dan kronis baik yang bersifat infeksi maupun autoimun. Pembentukan mereka yang meningkat adalah penyebab utama syok septik. Dengan sepsis, kadar TNF dalam darah bisa mencapai 1 ng/ml. Data terakumulasi tentang peran sitokin pro-inflamasi dalam etiopatogenesis kolitis ulserativa, multiple sclerosis, rheumatoid arthritis, diabetes tergantung insulin, dll.
Kami menganggap penting bagi imunodiagnostik untuk mempelajari ekspresi molekul aktivasi dan adhesi pada permukaan limfosit-T. Seperti namanya, identifikasi molekul aktivasi memberikan informasi penting tentang tingkat aktivasi sel T. Gangguan ekspresi reseptor IL-2 diamati pada banyak penyakit darah ganas - leukemia sel T, leukemia sel berbulu, limfogranulomatosis, dll. - dan proses autoimun: rheumatoid arthritis, lupus eritematosus sistemik, anemia aplastik, skleroderma, Crohn's penyakit, sarcoeloidosis dan lain-lain.
Menurut pendapat kami, masalah khusus adalah penggunaan tes kulit dalam diagnosis imunodefisiensi sel T. Seperti yang telah disebutkan, atas rekomendasi ahli asing dan sesuai dengan rekomendasi ahli WHO, digunakan sebagai skrining atau tes level 1 untuk menilai kekebalan sistem-T. Hal ini disebabkan oleh dua keadaan. Pertama, tes kulit- ini adalah tes informatif yang paling sederhana dan sekaligus untuk menilai aktivitas fungsional limfosit-T. Tes kulit positif dengan antigen mikroba tertentu sangat mungkin untuk mengecualikan adanya imunodefisiensi sel T pada pasien. Kedua, sejumlah perusahaan Barat telah mengembangkan sistem uji kulit yang mencakup antigen utama untuk menentukan kekebalan sel-T. Ini memungkinkan untuk menilai aktivitas fungsional sistem-T dari sistem kekebalan di bawah kondisi yang dikontrol secara ketat. Sayangnya, sistem seperti itu tidak ada di Rusia dan, oleh karena itu, praktis tidak digunakan untuk menilai sistem kekebalan T.
Penilaian sistem kekebalan pada orang dengan tanda-tanda SID dapat menemui sejumlah kesulitan, dan terutama terkait dengan penilaian hubungan sebab-akibat. Seringkali, perubahan yang dicatat ketika menganalisis parameter sistem kekebalan adalah konsekuensi, bukan penyebab proses patologis. Jadi, pada orang yang sering dan lama sakit (BHR) dengan infeksi pernapasan, tingkat antibodi terhadap bakteri patogen utama dari infeksi ini meningkat tajam. Situasi serupa diamati pada pasien AIDS dengan komplikasi infeksi dari saluran pernapasan. Secara alami, peningkatan titer antibodi terhadap agen penyebab infeksi saluran pernapasan baik pada pasien dengan kelompok BDI maupun pada pasien dengan AIDS adalah konsekuensi dari aktivasi sistem kekebalan sebagai akibat dari proses infeksi-inflamasi pada saluran pernapasan. sistem. Kesulitan lain yang mungkin dihadapi dokter ketika menilai status kekebalan pada pasien dengan proses infeksi dan inflamasi kronis adalah pilihan pendekatan metodologis yang memadai dan pilihan bahan yang memadai untuk penelitian. Meskipun pencapaian imunologi teoretis dan klinis hampir tidak dapat ditaksir terlalu tinggi dan ahli imunologi memiliki serangkaian besar metode modern untuk menentukan keadaan sistem kekebalan, harus diakui bahwa kita masih tahu sedikit tentang fungsi sistem kekebalan secara keseluruhan. . Hubungan spesifik antara perkembangan penyakit tertentu dan pelanggaran berbagai hubungan kekebalan juga belum dipelajari secara memadai. Oleh karena itu, ketika menggunakan metode standar untuk menilai fagositosis, sistem kekebalan T dan B pada pasien dengan proses infeksi dan inflamasi kronis, dokter sering tidak menerima informasi yang meyakinkan tentang gangguan kekebalan. Jadi, misalnya, ketika menentukan status kekebalan sesuai dengan parameter di atas pada pasien dengan penyakit kronis pada sinus paranasal, kami tidak mengungkapkan penyimpangan yang signifikan. Pada saat yang sama, ternyata pasien tersebut memiliki cacat dalam sintesis antibodi IgG3 terhadap Branhamella catarrhalis, dan ini adalah alasan utama pengembangan proses patologis utama. Seperti yang telah dicatat, pada orang yang menderita penyakit menular yang sering pada aparatus bronkopulmonalis, titer antibodi terhadap agen penyebab penyakit ini meningkat. Ternyata afinitas antibodi ini di sebagian besar pasien berkurang secara signifikan. Dan antibodi berafinitas rendah tidak efektif dalam menghilangkan patogen dari tubuh, dan ini mungkin salah satu alasan kronisitas proses infeksi. Ada banyak contoh seperti itu. Dalam semua kasus ini, ada tanda-tanda yang jelas secara klinis dari pelanggaran sistem kekebalan, tetapi mereka tidak selalu dikonfirmasi secara meyakinkan menggunakan metode penelitian imunolaboratorium.
Kami mengusulkan untuk mempertimbangkan kronis, berulang, lamban, sulit untuk merespon pengobatan tradisional menular proses inflamasi berbagai lokalisasi yang terdeteksi pada pasien dewasa sebagai manifestasi dari keadaan imunodefisiensi sekunder, terlepas dari apakah perubahan sistem kekebalan terdeteksi atau tidak menggunakan tes yang digunakan di laboratorium ini, yaitu, untuk mempertimbangkan dalam kasus ini VID sebagai konsep klinis murni. Kami tidak ragu bahwa adanya proses infeksi dan inflamasi kronis adalah hasil dari beberapa jenis kerusakan pada satu atau lebih komponen sistem kekebalan yang melindungi tubuh dari infeksi. Dan jika kerusakan ini tidak diidentifikasi, maka ini bisa menjadi, seperti yang baru saja ditunjukkan, hasil dari pendekatan metodologis yang tidak memadai, penggunaan bahan yang tidak memadai untuk penelitian, atau ketidakmampuan untuk mengidentifikasi kerusakan yang ada pada tahap ini dalam pengembangan ilmu pengetahuan. Contoh khas dari posisi terakhir adalah sindrom LAD, yang terdiri dari gangguan ekspresi molekul adhesi pada sel fagosit. Deteksinya menjadi mungkin hanya berkat munculnya teknologi hibridoma dan munculnya antibodi monoklonal.
Pada saat yang sama, kami menyadari fakta bahwa beberapa alasan khusus harus mendasari perkembangan bentuk spontan SPE. Untuk mempertimbangkan alasan ini, adalah tepat untuk mengingat sekali lagi bahwa kekebalan manusia adalah sistem multikomponen yang kompleks dan faktor resistensi bawaan dan kekebalan yang didapat terlibat dalam melindungi tubuh dari infeksi. Pada tahap awal perkembangan proses infeksi - dalam 96 jam pertama - tubuh dilindungi dari agen infeksi oleh kombinasi faktor kekebalan nonspesifik, seperti: sistem komplemen, protein fase akut, monokin, fagosit, alami sel pembunuh, dll. dari sistem ini mungkin tidak bermanifestasi secara klinis untuk beberapa waktu dalam bentuk peningkatan morbiditas infeksi, karena semua komponen lain dari sistem kekebalan berada dalam keadaan fungsional normal dan mengkompensasi cacat ini. Namun, perubahan yang terjadi dari waktu ke waktu dan di bawah pengaruh berbagai faktor yang tidak menguntungkan dalam komponen kompensasi ini, bahkan jika tidak terlalu signifikan, dapat memiliki efek kumulatif yang mengarah ke manifestasi fenotipik cacat primer dan perkembangan peningkatan morbiditas. Dapat diasumsikan bahwa inti dari banyak, dan mungkin hampir semua bentuk klinis VID, yang dimanifestasikan pada orang dewasa dalam bentuk peningkatan morbiditas infeksi, adalah insufisiensi imunologis utama dari beberapa komponen sistem kekebalan, yang dikompensasi hingga waktu tertentu. karena aktivitas fungsional yang normal atau tinggi dari komponen lain dari sistem ini. Kemungkinan ini dapat dikonfirmasi oleh defisiensi imun variabel umum (CVID), yang paling sering memanifestasikan dirinya dalam infeksi kronis berulang pada aparatus bronkopulmonalis dan sinus paranasal. Penyakit ini ditandai dengan penurunan kadar semua kelas imunoglobulin. CVID memiliki dua puncak: puncak pertama berkembang antara 6-10 tahun, yang kedua - antara 26-30 tahun, dan sebelum perkembangan penyakit, pasien ini praktis orang sehat... Ada banyak bukti bahwa defek imunitas humoral pada pasien CVID berasal dari genetik. Akibatnya, cacat ini dikompensasi hingga waktu tertentu karena aktivitas fungsional normal atau meningkat dari komponen lain dari sistem kekebalan, yang memastikan pertahanan tubuh terhadap infeksi. Selain CVID, ada sejumlah penyakit terkait PID yang terkadang bermanifestasi secara klinis di masa dewasa. Ini termasuk defisiensi IgA selektif, defisiensi subkelas IgG, defisiensi sistem komplemen. Kasus manifestasi primer dalam bentuk PID dewasa, khas hanya untuk masa kanak-kanak, dijelaskan. Ini termasuk defisiensi adenosin deaminase, sindrom Wiskott-Aldrich, agammaglobulinemia terkait-X. Biasanya, dalam kasus ini, timbulnya gejala penyakit yang tertunda adalah akibat dari cacat genetik ringan pada individu. Tetapi tidak mungkin untuk mengecualikan koreksi kompensasi dari cacat primer karena komponen kekebalan lainnya. Perubahan mereka dari waktu ke waktu memungkinkan manifestasi klinis primer, bahkan sedikit cacat pada sistem kekebalan tubuh.
- Penggunaan imunomodulator untuk imunodefisiensi
Terapi imunomodulator tidak efektif atau tidak efektif untuk PID. Metode utama pengobatan mereka adalah terapi antimikroba dan substitusi. Di luar negeri, terapi rekonstruktif digunakan, yang terdiri dari transplantasi sumsum tulang ke anak-anak yang sakit. Metode terapi gen juga sedang dikembangkan secara intensif.
Penggunaan imunomodulator lebih dibenarkan dan disarankan untuk SID. Penunjukan yang terakhir harus selalu dilakukan berdasarkan pemeriksaan klinis dan imunologis. Tergantung pada hasil survei ini, dua kelompok orang dapat dibedakan:
- memiliki tanda-tanda klinis gangguan kekebalan dalam kombinasi dengan perubahan spesifik dalam parameternya yang diidentifikasi menggunakan metode imunologis;
- hanya memiliki tanda-tanda klinis gangguan kekebalan tanpa mengubah parameter kekebalan.
Kriteria utama untuk penunjukan imunomodulator adalah gambaran klinis. Imunomodulator dapat (atau bijaksana) digunakan dalam terapi kompleks pasien dari kelompok pertama dan kedua. Timbul pertanyaan, imunomodulator spesifik apa yang harus diresepkan dengan adanya tanda-tanda SID? Masalah ini terutama akut pada pasien tanpa kelainan yang teridentifikasi pada sistem kekebalan tubuh. Untuk menjawab pertanyaan ini, perlu untuk menganalisis secara singkat mekanisme utama perlindungan anti-infeksi, karena manifestasi utama dari defisiensi imun, sebagaimana telah dicatat, adalah peningkatan morbiditas infeksi. Tujuan utama penggunaan imunomodulator pada pasien dengan tanda-tanda SID adalah untuk meningkatkan daya tahan tubuh terhadap anti infeksi.
Secara konvensional, semua mikroorganisme dapat dibagi menjadi ekstraseluler dan intraseluler. Sel efektor utama dalam perang melawan patogen ekstraseluler adalah neutrofil. Penyerapan dan fungsi bakterisidanya meningkat tajam dengan adanya komplemen dan IgG, serta ketika mereka diaktifkan oleh faktor nekrosis tumor (TNF), interleukin-1 (IL), IL-6 dan sitokin lain yang diproduksi oleh makrofag, sel NK dan limfosit T... Sel efektor utama dalam memerangi patogen intraseluler adalah makrofag, sel NK dan limfosit T. Sifat mikrobisida dan sitotoksiknya meningkat tajam di bawah pengaruh interferon, TNF, dan sitokin lain yang dihasilkan setelah aktivasi oleh antigen patogen dari tiga populasi sel yang sama. Sel pertama yang ditemui oleh patogen yang telah mengatasi selaput lendir atau kulit adalah makrofag jaringan. Makrofag yang telah menangkap mikroba diaktifkan dan mensintesis sejumlah monokin yang meningkatkan aktivitas fungsional monosit/makrofag baru, neutrofil dan sel NK. Makrofag ini, setelah membelah mikroba dengan bantuan sistem enzimnya, menyajikan penentu antigeniknya ke limfosit T dan B, sehingga memulai pengembangan respons humoral dan seluler dan menghasilkan beberapa sitokin yang diperlukan untuk perkembangannya.
Berdasarkan analisis skema perlindungan anti-infeksi yang disederhanakan ini (lihat gambar), dapat disimpulkan bahwa untuk stimulasinya, yang paling tepat adalah penggunaan imunomodulator yang secara dominan bekerja pada sel-sel sistem monosit-makrofag (MMC). ). Ketika sistem ini diaktifkan, seluruh rangkaian faktor spesifik dan nonspesifik dari pertahanan tubuh terhadap infeksi mulai bergerak. Sebelumnya, kami membagi semua imunomodulator menjadi tiga kelompok: eksogen, endogen, dan murni atau polimerik. Obat yang memiliki efek dominan pada sel MMC ditemukan di ketiga kelompok imunomodulator ini. Menuju sangat efisien obat generasi terbaru dengan efek dominan pada sel MMS termasuk polioksidonium, likopid, myelopid, fraksi MP-3-nya.
Baik aktivitas penyerapan dan mikrobisida sel fagosit bergantung pada aktivitas fungsional limfosit T dan, khususnya, pada kemampuannya untuk memproduksi sitokin yang mempersenjatai sel-sel ini. Oleh karena itu, imunomodulator dengan efek dominan pada limfosit T dan menginduksi sintesis sitokin tersebut di dalamnya akan merangsang aktivitas fungsional leukosit neutrofilik dan sel MMS, yaitu, mengaktifkan pertahanan anti-infeksi tubuh. Imunomodulator yang bekerja pada sistem kekebalan T termasuk sejumlah obat yang diperoleh dari timus sapi, serta nenek moyangnya - taktivin. Imunomodulator generasi terbaru dengan efek ini termasuk myelopid (fraksi MP-1) dan immunofan. Jika kita menganggap makrofag sebagai sel pusat dalam aktivasi sistem kekebalan, maka ketika menggunakan imunomodulator dengan efek dominan pada sel ini, kita mengaktifkan sistem kekebalan, yang secara konvensional dapat ditetapkan sebagai sentrifugal, yaitu pergi dari pusat ke pusat. keliling. Menggunakan imunomodulator dengan efek dominan pada sistem kekebalan T, kami mengaktifkan kekebalan ke arah yang berlawanan dengan gerakan alami dari sinyal aktivasi, yaitu, kita berbicara tentang aktivasi sentrifugal. Pada akhirnya, seluruh sistem kekebalan tubuh bergerak, akibatnya pertahanan tubuh terhadap infeksi meningkat. Praktek klinis yang besar menunjukkan bahwa kedua jenis aktivasi kekebalan dapat berhasil digunakan dalam pengobatan kompleks pasien dengan SID. Contoh yang sangat jelas adalah penggunaan imunomodulator untuk pengobatan infeksi bedah, yang dapat berfungsi sebagai contoh khas dari bentuk SID yang diinduksi. Hampir semua obat yang mempengaruhi kekebalan dan disetujui untuk penggunaan medis (levamisole, prodigiosan, pyrogenal, sodium nucleinate, diucifon, taktivin, thymogen, dll.) digunakan untuk mengobati infeksi ini, dan semuanya secara umum menunjukkan hasil klinis yang baik. Saat ini, seorang ahli imunologi telah pilihan besar imunomodulator untuk pengobatan VID, dan hanya setelah aplikasi dalam praktik klinis, yang paling banyak obat yang efektif, yang, seperti aspirin, glikosida jantung, antibiotik, dll., Akan dimasukkan dalam gudang ahli imunologi untuk waktu yang lama. Sebagai aturan, dalam kasus proses infeksi dan inflamasi kronis pada tahap akut, dokter meresepkan antibiotik. Kami percaya bahwa dalam kasus ini, pemberian imunomodulator secara simultan juga dianjurkan. Dengan penggunaan antibiotik dan imunomodulator secara simultan, efek terapeutik daripada dengan pengenalan mereka yang terpisah. Antibiotik membunuh atau menekan aktivitas fungsional patogen; imunomodulator secara langsung (polyoxidonium, lycopid, myelopid) atau tidak langsung (taktivin, imunofan, dll.) meningkatkan aktivitas fungsional fagosit, meningkatkan efek bakterisidalnya. Pukulan ganda diterapkan pada agen penyebab penyakit, yang dengannya efisiensi pengobatan kompleks yang lebih besar tercapai.
Menyimpulkan hal di atas, kami percaya bahwa penggunaan imunomodulator dalam kombinasi dengan obat lain akan membantu ahli imunologi lebih efektif merawat pasien dengan tanda-tanda SID.
Tentang imunodefisiensi secara umum
Inti dari setiap respons imun terletak pada pengenalan dan penghapusan dari tubuh zat asing yang bersifat antigenik, baik yang menembus secara eksogen (mikroorganisme) maupun yang terbentuk secara endogen (sel yang terinfeksi virus, sel yang dimodifikasi oleh xenobiotik, penuaan, sel tumor, dll.) . Tubuh dilindungi dari zat asing oleh faktor humoral dan seluler dari imunitas bawaan dan didapat, yang membentuk kompleks fungsional tunggal, saling melengkapi dan berada dalam kontak dan interaksi yang konstan.
Dalam fungsi sistem kekebalan, seperti halnya sistem tubuh lainnya, gangguan dapat terjadi yang mengarah pada perkembangan penyakit yang merupakan karakteristik, pertama-tama, dari sistem ini. Pelanggaran tersebut antara lain:
- pengenalan yang salah terhadap antigen asing dan diri sendiri, yang mengarah pada perkembangan proses autoimun;
- respons imun hiperergik atau menyimpang, yang mengarah pada perkembangan penyakit alergi;
- kegagalan untuk mengembangkan respons imun yang normal, yang mengarah pada pengembangan defisiensi imun
Catatan!
Beberapa prinsip umum imunoterapi pada pasien dengan tanda-tanda SID
- Alasan utama penunjukan imunomodulator haruslah gambaran klinis, ditandai dengan adanya pengobatan kronis, lamban dan sulit untuk proses infeksi dan inflamasi konvensional.
- Imunomodulator, dengan beberapa pengecualian, tidak digunakan sebagai monoterapi, tetapi, sebagai suatu peraturan, merupakan bagian integral dari perawatan komprehensif
- Saat meresepkan obat antibakteri, antijamur atau antivirus untuk pasien dengan tanda-tanda SID, disarankan untuk meresepkan imunomodulator secara bersamaan dengan efek dominan pada sel MMC.
Bagian imunologi.
Imunodefisiensi primer (bawaan)
Konsep imunodefisiensi primer dikembangkan pada tahun 60-an abad XX, meskipun beberapa penyakit keturunan pada sistem kekebalan telah dijelaskan sebelumnya. Sejak awal, imunodefisiensi yang ditentukan secara genetik dianggap sebagai "eksperimen alam" (R. Good), studi yang membantu memahami mekanisme imunologis. Memang, dalam sejumlah kasus, analisis dasar molekuler dari imunodefisiensi memungkinkan untuk mengungkapkan rincian baru dari struktur dan fungsi sistem kekebalan; namun, sifat cacat yang mendasari imunodefisiensi primer lebih sering diketahui setelah pengungkapan. hukum imunologi umum, konfirmasi klinis yang ternyata.
Imunodefisiensi primer adalah penyakit yang sangat langka. Sebagian besar terdeteksi dengan frekuensi 1 dalam 10 5 -10 6, beberapa - dengan frekuensi 1 dalam 10 4. Hanya untuk defisiensi IgA selektif memiliki frekuensi 1 dalam 500-1000 yang telah ditentukan. Penyakit kelompok ini terdeteksi terutama pada masa kanak-kanak, karena banyak pasien tidak hidup hingga 20 tahun, dan sisanya, cacat dikompensasi sampai batas tertentu. Terimakasih untuk pengobatan yang berhasil ambang usia atas ditemukan lebih menyebar dari sebelumnya.
Karena tingkat keparahan khusus dari reaksi patologis ini, serta minat ilmiah yang signifikan dari setiap kasus penyakit tertentu, imunodefisiensi primer menarik perhatian tidak hanya ahli imunologi. Organisasi Kesehatan Dunia menerbitkan materi yang mencerminkan keadaan masalah ini secara berkala.
Intinya, bagaimanapun, adalah bahwa tanpa limfosit, tetapi dengan pelestarian lengkap leukosit dan komplemen, tidak ada respon imun: sendiri, tanpa limfosit, mekanisme resistensi seluler dan humoral pra-kekebalan tidak dapat mengatasi yang nyata, terus berubah. kumpulan mikroorganisme dan cacing menular, serta bahan tambahan makanan dan obat-obatan buatan. Gejala klinis dan tes laboratorium yang memadai memungkinkan untuk membedakan patologi pada tingkat limfosit dan patologi pada tingkat mekanisme non-limfositik penghancuran dan pelepasan Ar.
Angka kejadian PID secara umum adalah 1 kasus per 10-100 ribu kelahiran hidup. Defisiensi IgA selektif jauh lebih umum - 1 dari 500-1500 penduduk populasi umum.
Cacat klinis utama pada PID sesuai dengan fungsi alami utama dari sistem kekebalan tubuh dan terdiri dari penyakit menular. Sejak sebelum awal paruh kedua abad XX. Karena manusia hidup tanpa antibiotik, kematian bayi akibat infeksi adalah hal biasa, dan dengan latar belakang kematian bayi yang tinggi akibat infeksi, dokter tidak mengisolasi PID, dan imunologi belum berkembang. Hanya antara tahun 1920 dan 1930. dalam literatur medis, deskripsi penyakit mulai muncul untuk pertama kalinya, yang kemudian dipahami sebagai PID. Nosologi pertama diidentifikasi pada tahun 1952 oleh dokter Inggris Bruton, yang, pada elektroforesis serum darah anak yang sakit, mengungkapkan tidak adanya g-globulin (yaitu, imunoglobulin). Penyakit ini disebut agammaglobulinemia Bruton. Kemudian menjadi jelas bahwa patologi terkait dengan kromosom X, nama modernnya adalah agammaglobulinemia Bruton terkait-X.
Klasifikasi imunodefisiensi primer:
1. Sindrom dengan defisiensi AT.
2. Sindrom dengan defisiensi T-limfosit.
3. Gabungan T- dan B-kekurangan.
4. Sindrom dengan defisiensi komponen komplemen.
5. Sindrom dengan defek pada NK.
6. Sindrom dengan defek fagosit.
7. Sindrom dengan cacat pada molekul adhesi.
"Wajah" klinis utama PID adalah apa yang disebut sindrom infeksi - peningkatan kerentanan terhadap infeksi secara umum, perjalanan penyakit menular yang berulang, luar biasa parah perjalanan klinis, patogen atipikal (seringkali oportunistik). Kebanyakan PID bermanifestasi pada anak usia dini. PID dicurigai jika anak kecil menderita penyakit menular lebih dari 10 kali dalam setahun. Pada anak-anak dengan PID, infeksi bisa persisten. Perhatian harus diberikan pada keterlambatan dalam indikator usia perkembangan, sinusitis berulang, otitis media, pneumonia, diare, malabsorpsi, kandidiasis. Pemeriksaan fisik mengungkapkan tidak adanya kelenjar getah bening dan amandel.
Jika bukti klinis menunjukkan PID, tes laboratorium berikut dilakukan:
1.analisis infeksi HIV,
2. penentuan jumlah darah,
3.penentuan kadar IgG, IgA, IgM dalam serum darah,
4. tes kulit HRT untuk Ar biasa (Tetanus Ar, difteri, streptokokus, tuberkulin, Proteus mirabilis, Trichophyton mentagrophytes, Candida albicans),
5.jika perlu - menghitung subpopulasi limfosit T dan B,
6.untuk indikasi klinis khusus, analisis kandungan komponen komplemen (dimulai dengan C3 dan C4),
7. untuk indikasi khusus, analisis keadaan fagosit (analisis paling sederhana dan paling informatif adalah tes untuk pemulihan pewarna biru terazolium),
8. Penelitian genetik molekuler, jika masuk akal (yaitu prospek spesifik untuk terapi gen) dan sarananya.
Analisis tidak dilakukan sekaligus, tetapi langkah demi langkah, karena dokter berhasil atau gagal mengenali nosologi. Semua analisis itu mahal, dan bukan kebiasaan untuk melakukan tes "berlebihan".
Defisiensi Imunoglobulin Primer dengan Defek Imunoglobulin
Bruton agammaglobulinemia terkait-X
Anak laki-laki sakit yang ibunya pembawa kromosom X yang cacat. Defectan memiliki satu gen pada kromosom X (Xq22); mengkodekan protein tirosin kinase B-limfosit spesifik (ditunjuk untuk menghormati Bruton sebagai Btk), homolog dengan anggota keluarga Tes tirosin kinase.
data laboratorium. Tidak ada limfosit B perifer. Sumsum tulang mengandung sel pra-B dengan rantai m di sitoplasma. IgM dan IgA tidak terdeteksi dalam serum, IgG mungkin ada, tetapi tidak cukup (40-100 mg/dl). Analisis antibodi terhadap golongan darah Ar yang sesuai dan antibodi terhadap vaksin Ar (toksin tetanus, toksin difteri, dll.) menunjukkan ketidakhadirannya. Hitung T-limfosit dan tes fungsi T-limfosit normal.
Gambaran klinis... Jika tidak ada riwayat keluarga yang diketahui, diagnosis rata-rata terbukti pada usia 3,5 tahun. Penyakit ini ditandai dengan infeksi piogenik yang parah, infeksi saluran pernapasan atas (sinusitis, otitis) dan bawah (bronkitis, pneumonia), gastroenteritis, pioderma, artritis septik (bakteri atau klamidia), septikemia, meningitis, ensefalitis dapat terjadi. Infeksi saluran pernafasan paling sering disebabkan oleh Haemophilus influenza, Streptococcus pneumonia, Staphylococcus aureus. Diare disebabkan oleh bakteri usus atau Giardia lambia. infeksi virus infeksi khas dengan virus neurotropik ECHO-19, yang menyebabkan meningoensefalitis persisten. Pada anak-anak yang sakit, ketika diimunisasi dengan polio hidup, sebagai suatu peraturan, ada pencucian yang berkepanjangan melalui selaput lendir virus poliomielitis, dan dengan virulensi yang dipulihkan dan meningkat (yaitu, dalam kelompok anak-anak ada bahaya nyata infeksi dari infeksi yang sehat. anak-anak dengan poliomielitis akibat kontak dengan anak imunodefisiensi yang divaksinasi). Saat memeriksa anak-anak seperti itu, perhatian diberikan pada keterbelakangan pertumbuhan, jari-jari dalam bentuk stik drum, perubahan bentuk dada, karakteristik penyakit pada saluran pernapasan bagian bawah, hipoplasia kelenjar getah bening dan amandel. Pemeriksaan histologis jaringan limfoid menunjukkan tidak adanya pusat germinal dan sel plasma.
1. Kemoterapi antimikroba.
2. Terapi substitusi: infus intravena preparat imunoglobulin serum donor setiap 3-4 minggu seumur hidup. Dosis persiapan imunoglobulin dipilih untuk menciptakan konsentrasi imunoglobulin dalam serum pasien yang tumpang tindih dengan batas bawah norma usia.
3. Kemungkinan terapi genetik sedang dibahas. Gen Btk telah diklon, tetapi ada bukti bahwa hiperekskresi gen ini dikaitkan dengan transformasi ganas jaringan hematopoietik.
Agammaglobulinemia terkait-X dengan sindrom hiperimunoglobulinemia M
Anak laki-laki yang ibunya pembawa cacat itu sakit. Cacat molekuler, dengan tingkat kecurigaan tertentu, berkaitan dengan gen lagnda CD40. Kurangnya ekspresi CD40L dalam limfosit-T menyebabkan ketidakmungkinan mengalihkan sintesis kelas-kelas imunoglobulin dalam limfosit-B dari M ke semua isotipe lainnya.
data laboratorium. IgG, IgA, IgE tidak terdeteksi atau jumlahnya sangat sedikit. Tingkat IgM meningkat, itu bisa secara signifikan. Sebagai aturan, IgV adalah poliklonal, kadang-kadang monoklonal. Tidak ada pusat germinal di jaringan limfoid, tetapi ada sel plasma.
Gambaran klinis. Infeksi bakteri dan fleksibel yang berulang, termasuk oppuronic (Pneumocustis carinii). Mungkin ada lyfadenopathy dan splenomegali. Gambaran klinis yang serupa dijelaskan untuk jenis warisan patologi yang diduga autosomal, serta untuk beberapa kasus patologi pada anak-anak yang telah mengalami infeksi intrauterin dengan virus rubella.
Perlakuan. Mirip dengan pengobatan agammaglobulinemia Bruton, yaitu kemoterapi antimikroba dan infus imunoglobulin serum donor seumur hidup secara teratur.
Teks lengkap dari kuliah disajikan pada slide.
Setiap orang memiliki sistem kekebalan yang dirancang untuk mengenali dan melindungi tubuh dari zat asing. Tujuan akhir dari kekebalan adalah untuk menghancurkan mikroorganisme, sel-sel atipikal yang menyebabkan dampak negatif pada kesehatan manusia. Tergantung pada asalnya, imunodefisiensi primer dan sekunder dibedakan. Dengan defisiensi imun, semua infeksi dan penyakit menjadi lebih sulit, lebih sering berubah menjadi bentuk kronis dan mengalami komplikasi.
Apa itu defisiensi imun primer?
Immunodeficiency primer adalah kondisi herediter atau didapat selama perkembangan janin, di mana ada masalah dalam fungsi sistem kekebalan tubuh. Dengan kata lain, seorang anak dilahirkan tanpa kemampuan untuk bertahan melawan infeksi dan virus apa pun. Imunodefisiensi primer pada anak-anak didiagnosis pada usia dini... Pasien yang sakit parah biasanya meninggal. Dalam beberapa bentuk penyakit, gejala pertama sudah dapat dideteksi pada usia dewasa. Ini terjadi ketika pasien memiliki kompensasi yang baik untuk bentuk penyakit tertentu. Gambaran klinis diekspresikan oleh proses infeksi berulang dan kronis. Ini sering mempengaruhi sistem bronkopulmoner, organ THT, kulit dan selaput lendir. Imunodefisiensi primer dapat menyebabkan perkembangan limfadenitis purulen, abses, osteomielitis, meningitis, dan sepsis.
Beberapa bentuk dimanifestasikan oleh alergi, penyakit autoimun, dan dapat memicu perkembangan tumor ganas. Imunologi akan membantu mengenali defisiensi imun primer - ilmu yang mempelajari mekanisme pertahanan diri tubuh terhadap zat berbahaya.
Didiagnosis imunodefisiensi kongenital cukup sulit. Diagnosis dini sangat penting karena alasan berikut:
- diagnosis tepat waktu dan terapi yang ditentukan dengan benar berkontribusi pada pelestarian kualitas hidup yang tinggi pada pasien selama bertahun-tahun;
- diagnosis defisiensi imun primer dan pengenalan gen yang rusak memungkinkan untuk menjelaskan kepada anggota keluarga dalam bentuk yang dapat diakses tentang hasil laporan genetik medis dan untuk melakukan diagnosa intrauterin.

Imunodefisiensi primer: klasifikasi
Immunodeficiency mengacu pada perubahan terus-menerus dalam sistem kekebalan tubuh yang disebabkan oleh cacat pada satu atau lebih mekanisme respon imun. Ada empat jenisnya:
- Berkaitan dengan usia, timbul pada usia dini atau usia tua.
- Dibeli.
- Menular, dipicu oleh virus.
- Bawaan (defisiensi imun primer).
Klasifikasi defisiensi imun primer adalah sebagai berikut:
- Defisiensi imun berhubungan dengan kerusakan beberapa jenis sel:
● Disgenesis retikuler - ditandai dengan tidak adanya sel punca sama sekali. Bentuk penyakit ini tidak sesuai dengan kehidupan.
● Defisiensi imun gabungan parah yang disebabkan oleh defek pada limfosit T dan limfosit B. - Kekurangan kekebalan, karena kekalahan sel-T terutama: sindrom Di George, yang ditandai dengan tidak adanya atau keterbelakangan timus (kelenjar timus) dan kelenjar paratiroid, cacat jantung bawaan, kelainan bentuk pada struktur wajah. Penyakit ini dapat disertai dengan kelainan pada perkembangan kerangka, ginjal, dan sistem saraf.
- Defisiensi imun, dengan kerusakan dominan pada sel B.
- Kekalahan sel myeloid memprovokasi imunodefisiensi primer. Penyakit granulomatosa kronis memiliki cacat nyata dalam produksi spesies oksigen reaktif. Akibatnya, terjadi infeksi kronis yang dipicu oleh bakteri atau jamur.
- Defisiensi imun berhubungan dengan defek pada sistem komplemen. Cacat ini menyebabkan kurangnya atau tidak adanya lengkap berbagai konstituen pelengkap.
Ada juga defisiensi imun seluler, humoral seluler, dan humoral primer. Bentuk seluler dari defisiensi imun termasuk defek yang terkait dengan defisiensi limfosit, makrofag, sel plasma. Bentuk humoral disebabkan oleh defisiensi antibodi.
Apa itu imunodefisiensi sekunder?
Jenis imunodefisiensi ini bukan penyakit keturunan. Itu diperoleh sepanjang hidup. Perkembangannya dapat disebabkan oleh pengaruh faktor-faktor yang bersifat biologis, kimiawi dan ekologis. Orang yang menjalani gaya hidup tidak sehat, makanan kurang gizi, dan berada dalam keadaan stres yang konstan tidak terlindungi dari defisiensi imun sekunder. Paling sering orang dewasa sakit.
Klasifikasi imunodefisiensi sekunder
Di antara keadaan sekunder defisiensi imun, saya membedakan tiga bentuk:
- diperoleh, contohnya adalah AIDS, dipicu oleh kekalahan sistem kekebalan oleh virus human immunodeficiency;
- diinduksi, akibat paparan rangsangan spesifik dalam bentuk sinar-x, penggunaan kortikosteroid, trauma dan pembedahan;
- spontan, ditandai dengan tidak adanya penyebab yang jelas yang menyebabkan timbulnya defisiensi imun.
Imunodefisiensi sekunder juga dibagi menjadi reversibel dan ireversibel. Varian dari defisiensi imun reversibel dapat berupa kelaparan dan defisiensi kehidupan yang terkait. komponen penting... Infeksi HIV adalah contoh dari bentuk imunodefisiensi yang ireversibel.
Tanda-tanda imunodefisiensi
Gejala utama penyakit ini adalah kecenderungan seseorang terhadap penyakit menular yang sering. Imunodefisiensi primer ditandai dengan infeksi pernapasan berulang. Di sini perlu untuk membedakan dengan jelas antara orang dengan defisiensi imun dan kekebalan yang lemah.

Gejala yang lebih khas dari penyakit ini adalah terjadinya infeksi yang bersifat bakteri, dengan sering kambuh. Ini memanifestasikan dirinya dalam sakit tenggorokan yang berulang, gatal di hidung, yang mengarah pada perkembangan sinusitis kronis, bronkitis, dan otitis media. Tubuh dalam proses pengobatan tidak dapat sepenuhnya menghilangkan agen penyebab penyakit, dan karena itu kambuh. Imunodefisiensi primer pada anak dapat menyebabkan penyakit autoimun seperti endokrinopati autoimun, anemia hemolitik, artritis reumatoid... Anak-anak dalam kondisi ini rentan terhadap beberapa agen infeksi sekaligus. Juga khas untuk keadaan ini merupakan gangguan pada sistem pencernaan. Imunodefisiensi primer pada orang dewasa dapat dimanifestasikan oleh adanya jumlah yang besar kutil dan papiloma pada tubuh.
Diagnosis defisiensi imun primer

Diagnosis penyakit dimulai dengan pengumpulan anamnesis. Dokter harus melihat riwayat keluarga, terutama jika anak dengan bentuk primer didiagnosis. Pasien harus diperiksa, kondisi selaput lendir dan kulit, ukuran hati dan limpa. Diagnosis semacam itu juga ditandai dengan manifestasi berupa radang mata, pembengkakan lubang hidung, batuk kronis yang berkepanjangan.
Untuk diagnosis yang akurat, tes darah terperinci harus dilakukan, yang akan menunjukkan jumlah sel yang berbeda dalam tubuh, tingkat imunoglobulin. Analisis adalah wajib, yang akan menunjukkan kandungan protein dalam darah, yang menunjukkan kemampuan tubuh untuk melawan berbagai infeksi.
Diagnosa sebelum lahir
Telah ditetapkan bahwa imunodefisiensi primer adalah penyakit keturunan dan tidak jarang seperti yang diperkirakan. Sampai saat ini, menjadi mungkin untuk mengidentifikasi pembawa gen yang bermutasi dan menasihati keluarga yang berencana melahirkan anak yang berisiko terkena penyakit tersebut. Jika keluarga sudah memiliki anak dengan kondisi ini, ia menjalani analisis mutasi, setelah itu studi diagnostik embrio dilakukan. Untuk ini, analisis molekuler cairan ketuban, yang mengandung sel-sel janin, dilakukan.
Komplikasi setelah imunodefisiensi
Imunodefisiensi primer dan sekunder dapat menimbulkan komplikasi berupa penyakit infeksi berat seperti sepsis, pneumonia dan abses. Mengingat berbagai macam penyakit yang disebabkan oleh defisiensi imun, kemungkinan komplikasi harus ditentukan secara individual.
Pengobatan imunodefisiensi

Imunodefisiensi primer, pengobatan yang merupakan proses yang kompleks dan panjang, memerlukan gaya hidup sehat dan menghindari infeksi. Sebelum meresepkan pengobatan yang kompleks, diagnosis yang akurat harus ditetapkan dengan mengidentifikasi hubungan yang rusak dalam sistem pertahanan kekebalan. Jika kekurangan imunoglobulin terdeteksi, terapi penggantian dengan serum yang mengandung antibodi dilakukan sepanjang hidup. Komplikasi yang timbul pada penyakit infeksi diobati dengan antibiotik, obat antivirus dan antijamur. Dalam beberapa kasus, imunodefisiensi primer diobati dengan imunoglobulin yang diberikan secara subkutan atau intravena.
Imunokoreksi juga dilakukan melalui transplantasi sumsum tulang dan penggunaan imunomodulator.
Anak-anak dengan kondisi ini tidak boleh divaksinasi dengan vaksin hidup. Orang dewasa yang tinggal dengan anak divaksinasi hanya dengan vaksin polio yang tidak aktif.
Imunodefisiensi sekunder memiliki gangguan yang kurang menonjol dalam fungsi sistem kekebalan tubuh.
Penyakit ini dipicu oleh gangguan pada sistem hematopoietik, yang dapat bersifat bawaan dan didapat. Sumsum tulang berhenti membuat sel darah. Kekurangan eritrosit, trombosit dan leukosit terungkap.
Terjadinya dapat dipicu oleh intoleransi individu, khususnya beberapa narkoba... Alasan sensitivitas ini tidak selalu jelas, tetapi mungkin terkait dengan cacat genetik pada sel hematopoietik.
Penyebab lain terjadinya juga dapat:

Tanda-tanda anemia aplastik
Gejala kondisi ini meliputi:
- kelelahan dan kelemahan konstan;
- detak jantung tidak teratur;
- pucat kulit;
- sering mimisan;
- pendarahan berkepanjangan setelah luka;
- gusi berdarah;
- penyakit menular yang sering;
- pusing dan migrain.
Pengobatan anemia aplastik
Kasus penyakit ringan hanya membutuhkan pemantauan pasien secara konstan. Dalam kondisi yang lebih kompleks, transfusi darah, transplantasi sumsum tulang, dan obat-obatan khusus yang merangsang sel-sel hematopoietik digunakan. Imunosupresan sering digunakan dalam pengobatan untuk membantu melemahkan respons kekebalan tubuh dengan menyebabkan sel-sel sistem kekebalan tidak merespons jaringan tulang. Dalam beberapa tahun terakhir, semakin sering, dokter cenderung melakukan transplantasi sumsum tulang dini, yang menghindari banyak komplikasi.
Pencegahan defisiensi imun primer
Sindrom imunodefisiensi primer adalah penyakit keturunan, dan, karenanya, tidak ada tindakan pencegahan untuk itu. Untuk menghindari manifestasi keadaan imunodefisiensi, perlu untuk menentukan kemungkinan pembawa gen yang rusak dalam keluarga, di mana riwayatnya positif. Untuk patologi seperti imunodefisiensi gabungan yang parah, diagnosis intrauterin dimungkinkan.

Sebagai profilaksis untuk terjadinya defisiensi imun sekunder, seseorang harus menjalani gaya hidup yang benar, melakukan aktivitas fisik sedang, dan menghindari infeksi HIV ke dalam tubuh. Dan untuk ini Anda perlu menghindari hubungan seksual yang tidak aman dan memastikan bahwa peralatan medis steril digunakan. Penyakit yang dipicu oleh defisiensi imun bersifat kompleks dan berbahaya dalam bentuk apa pun. Sikap hati-hati terhadap kesehatan seseorang, pendekatan terpadu dan akses tepat waktu ke dokter akan membantu menyelamatkan masa depan kita - anak-anak kita.
UNTUK MEMBANTU DOKTER PRAKTIS
UDC 612.216-112
Diterima 31 April 2008
L.M. KARZAKOVA, O.M. MUCHUKOVA,
N.L. CERITA
Defisiensi imun primer dan sekunder
Rumah Sakit Klinis republik,
Rumah Sakit Anak Kota No. 3, Cheboksary
Prinsip-prinsip diagnostik dan pengobatan keadaan imunodefisiensi dipertimbangkan. Banyak perhatian diberikan pada penyakit imunodefisiensi primer. Diberikan tersusun disponsori Daftar utama defisiensi imun Chuvashia.
Berikut adalah prinsip-prinsip diagnostik dan pengobatan keadaan defisiensi imun. Perhatian besar tertarik pada penyakit defisiensi imun primer. Ini berisi daftar penyakit defisiensi imun utama di Chuvashia, yang dibuat oleh penulis.
Imunodefisiensi, gangguan respons imun, dibagi menjadi dua kelompok besar - primer (bawaan) dan sekunder (didapat), yang disebabkan oleh berbagai pengaruh endogen (penyakit) dan eksogen (misalnya, faktor lingkungan negatif). Imunodefisiensi primer (PID), sebagai suatu peraturan, disebabkan oleh defek genetik dan hanya kadang-kadang non-herediter yang muncul selama periode embrionik. Manifestasi khas PID adalah pelanggaran resistensi anti-infeksi dengan perkembangan infeksi berulang dan / atau kronis dari berbagai lokalisasi. Jenis patogen infeksius di mana tubuh menjadi hipersensitif bergantung pada defek pada satu atau lain mata rantai respons imun. Dengan demikian, cacat dalam produksi antibodi (insufisiensi hubungan humoral dari respons imun) menyebabkan penurunan resistensi terutama terhadap bakteri (staphylococcus, streptococcus, pneumococcus, Escherichia coli, Proteus, Klebsiella) dan enterovirus. Peningkatan kerentanan terhadap virus, infeksi protozoa, tuberkulosis, kriptokokosis, leishmaniasis adalah karakteristik dari pelanggaran hubungan seluler dari respons imun. Dengan defek pada fagositosis, penyebab paling umum dari sindrom infeksi adalah mikroorganisme yang menghasilkan katalase (staphylococci, E. coli, Serratia marcescens, Nocardia, Aspergillus, dll.), sebagian besar bakteri dan jamur gram negatif (Candida albicans, Aspergillus). Defek pada sistem komplemen dimanifestasikan oleh infeksi yang disebabkan oleh flora kokus dan Neisseria. Dengan pelanggaran gabungan dari respon imun (combined immunodeficiency), sindrom infeksi disebabkan oleh bakteri dan virus, jamur, protozoa.
Dalam beberapa kasus, sindrom infeksi digabungkan dengan manifestasi non-imunologis - dengan gejala yang jelas dari organ dan sistem lain. Jadi, sindrom DiGeorge memanifestasikan dirinya tidak hanya dalam pelanggaran hubungan seluler kekebalan, tetapi juga dalam aplasia atau hipoplasia timus dengan agenesis kelenjar paratiroid, malformasi jantung dan pembuluh darah besar, stigma disembriogenesis (langit-langit sumbing, tidak adanya daun telinga, dll). Pada sindrom Louis-Bar, defisiensi imun gabungan (penurunan jumlah limfosit T, penurunan kadar IgA) dikombinasikan dengan ataksia serebelar dan telangiektasia pada kulit dan sklera mata. Defek imun gabungan (penurunan jumlah limfosit T, penurunan kadar IgM) dalam kombinasi dengan eksim dan trombositopenia terjadi pada sindrom Wiskott-Aldrich.
Defisiensi imun primer
Kasus pertama dari keadaan defisiensi imun bawaan (agammaglobulinemia karena pelanggaran produksi imunoglobulin yang ditentukan secara genetik) dijelaskan oleh Bruton pada tahun 1952. Sejak itu, lebih dari 100 cacat utama yang berbeda dari sistem kekebalan telah dikenali. Beberapa PID cukup umum. Misalnya, frekuensi defisiensi IgA selektif mencapai 1:500. Untuk sebagian besar PID lainnya, angka ini adalah 1:50.000 - 1: 100.000. Menurut berbagai publikasi, ada underdiagnosis yang jelas dan kelambatan dalam waktu diagnostik PID di dunia. Atas inisiatif Jeffrey Model Foundation (USA) dan ESID (European Society for the Study of Immunodeficiencies), kriteria telah dikembangkan untuk mencurigai PID pada pasien.
kriteria PID:
1. Penyakit otitis media yang sering (6-8 kali setahun).
2. Sering terkena penyakit sinusitis (4-6 kali setahun).
3. Lebih dari dua pneumonia dikonfirmasi.
4. Abses dalam yang berulang pada kulit dan organ dalam.
5. Perlunya terapi jangka panjang (lebih dari 2 bulan) dengan antibiotik untuk menghentikan infeksi.
6. Perlunya antibiotik intravena untuk menghentikan infeksi.
7. Lebih dari dua infeksi berat (meningitis, osteomielitis, sepsis).
8. Ketertinggalan tinggi dan berat badan bayi.
9. Infeksi jamur persisten pada kulit di atas usia 1 tahun.
10. Kerabat menderita PID, kematian dini akibat infeksi berat, atau gejala-gejala ini.
Deteksi lebih dari satu gejala yang terdaftar pada pasien harus waspada PID dan menjadi sinyal untuk studi imunologi. Peran dan tempat PID dalam struktur morbiditas dan mortalitas di dunia sangat penting, yang menjadi alasan dibuatnya register PID nasional di Eropa Barat, Amerika, Australia. Analisis data yang termasuk dalam register memungkinkan untuk menilai frekuensi terjadinya PID di berbagai belahan dunia, populasi etnis, untuk menetapkan bentuk patologi yang berlaku dan dengan demikian menciptakan prasyarat untuk meningkatkan kualitas diagnosis penyakit langka. bentuk penyakit dengan membandingkan kasus baru dengan analog yang tersedia di register. Sejak 1992, Rusia juga telah mempertahankan daftar PID berdasarkan data dari analisis rawat inap dan rujukan pasien ke departemen Pusat Penelitian Negara Federasi Rusia "Institute of Immunology". Namun, banyak kasus PID yang terdiagnosis di daerah masih belum ditemukan. Pembentukan register apa pun harus didasarkan pada klasifikasi penyakit yang seragam. Karena singkatnya sejarah studi PID, klasifikasinya masih belum final. Grup Ilmiah WHO menerbitkan laporan dan rekomendasi tentang taksonomi PID setiap 2-3 tahun, dan seiring berjalannya implementasi metode modern diagnostik, jumlah bentuk penyakit yang dijelaskan dan urutan klasifikasinya berubah secara signifikan . Sesuai dengan klasifikasi WHO terbaru (2004), PID dibagi menjadi beberapa kelompok berikut:
1. PID dengan defek antibodi yang dominan (imunodefisiensi humoral):
Agammaglobulinemia terkait dengan kromosom X (CVAGG);
· Defisiensi imun variabel umum (CVID);
Agammaglobulinemia dengan or normal tingkat tinggi IgM;
· Defisiensi IgA selektif;
· Hipogammaglobulinemia sementara pada masa bayi (awal imunologis yang terlambat).
2.PID dengan defek sel T yang dominan:
- defisiensi primer sel CD4+;
- defisiensi IL-2;
- defisiensi sitokin multipel;
- cacat transduksi sinyal + miopati;
- defek pada masuknya kalsium dengan miopati.
3. Keadaan imunodefisiensi gabungan:
- imunodefisiensi gabungan yang parah (SCID);
- sindrom Wiskott-Aldrich;
- ataksia - aleangiectasia (sindrom Louis-Bar).
4. Cacat fagositosis:
- penyakit granulomatosa kronis;
- Sindrom Chediak-Higashi.
5. Cacat sistem komplemen.
6. Imunodefisiensi terkait dengan cacat utama lainnya di luar sistem kekebalan:
- sindrom hiper-IgE (sindrom Job);
- kandidiasis mukokutaneus kronis;
- limfangiektasia usus;
- akrodermatitis enteropatik.
7. Defisiensi imun yang berhubungan dengan proses limfoproliferatif.
Bentuk PID yang paling umum adalah sebagai berikut.
Agammaglobulinemia terkait-X, atau penyakit Bruton (1:50 000), diamati pada anak laki-laki pada bulan ke 5-9 kehidupan, ketika terjadi penurunan imunoglobulin ibu yang ditransplantasikan. Penyakit ini dimanifestasikan oleh infeksi piogenik berulang (pneumonia, sinusitis, mesotimpanitis, meningitis). Penting gejala diagnostik - Kelenjar getah bening, limpa tidak merespon dengan peningkatan proses inflamasi. Sebuah studi imunolaboratorium mengungkapkan: 1) penurunan atau tidak adanya -globulin dalam serum darah; 2) penurunan kadar IgG serum (kurang dari 2 g / l) tanpa adanya atau penurunan tajam kadar IgM dan IgA; 3) tidak adanya atau penurunan tajam jumlah limfosit B (CD19 + atau CD20 +) dalam sirkulasi kurang dari 2%; 4) tidak adanya atau hipoplasia amandel; 5) ukuran kecil kelenjar getah bening; 6) fungsi limfosit T yang diawetkan.
CVID (1:10 000 - 1:50 000) adalah kelompok penyakit yang heterogen dengan defek pada produksi antibodi dan tipe pewarisan yang berbeda. Istilah "variabel" berarti manifestasi penyakit pada berbagai usia (anak-anak, remaja, dewasa) dengan variasi individu dalam jenis dan tingkat keparahan imunodefisiensi. Menurut gambaran klinis, CVID menyerupai penyakit Bruton, perbedaan utamanya adalah pada waktu manifestasi penyakit: usia rata-rata manifestasi klinis CVID adalah 25, diagnosisnya adalah 28 tahun. Kelangsungan hidup pasien tergantung pada tingkat penurunan tingkat IgG dan ketidakcukupan komponen seluler dari respon imun: semakin jelas mereka, semakin dini pasien dengan CVID meninggal. Bentuk PID ini mempengaruhi pria dan wanita secara setara. Seperti semua imunodefisiensi humoral, CVID secara klinis dimanifestasikan oleh pneumonia berulang dan kronis, sinusitis, otitis media, bronkiektasis sering terbentuk, pada setengah kasus, saluran pencernaan terpengaruh dengan gejala malabsorpsi, penurunan berat badan, diare, hipoalbuminemia, dan vitamin. kekurangan. Ditandai dengan proses inflamasi kronis di usus (infeksi enterovirus) dengan perkembangan hiperplasia limfoid nodular. Sekitar sepertiga pasien mengalami splenomegali dan/atau limfadenopati difus. Pada 22% kasus, timbul manifestasi autoimun (anemia pernisiosa atau hemolitik, trombositopenia, neutropenia, artritis reumatoid, disfungsi kelenjar tiroid). Sebuah studi imunolaboratorium mengungkapkan: 1) jumlah limfosit B yang bersirkulasi normal atau sedikit berkurang; 2) penurunan kadar IgG dan IgA serum, pada tingkat yang lebih rendah - tingkat IgM; penurunan konsentrasi total IgG + IgA + IgM kurang dari 3 g / l; 3) jumlah total Sel T normal atau agak berkurang karena penurunan jumlah subpopulasi T-helper; 4) penurunan indeks imunoregulator CD4+/CD8+.
Defisiensi IgA selektif (1:700 pada bule; 1:18500 dalam bahasa Jepang) ditandai dengan penurunan kadar IgA serum hingga 0,05 g/l dan di bawahnya (cukup sering hingga 0) dengan kadar normal kelas imunoglobulin lainnya. Jika konsentrasi IgA lebih tinggi dari 0,05 g / l, tetapi di bawah 0,2 g / l, maka diagnosis "defisiensi IgA parsial (sebagian)" harus dibuat. Dalam kebanyakan kasus, defisiensi IgA tidak menunjukkan gejala, namun, pada beberapa individu, defisiensi IgA bermanifestasi sebagai infeksi sinopulmonal dalam kombinasi dengan manifestasi alergi (dermatitis atopik, demam, asma bronkial, edema Quincke, dll.) dan autoimun (skleroderma, rheumatoid arthritis, vitiligo). ), tiroiditis.
Hipogammaglobulinemia sementara pada anak-anak ("awal imunologis yang lambat") ditandai dengan rendahnya kadar imunoglobulin. Timbulnya penyakit adalah dari 5-6 bulan, ketika anak tiba-tiba, tanpa alasan yang jelas, mulai sakit dengan infeksi piogenik berulang pada ginjal dan saluran pernapasan. Hal ini disebabkan fakta bahwa IgG ibu yang diterima oleh transplantasi anak dikatabolisme pada usia ini, dan produksi IgGnya sendiri, biasanya mulai dari bulan ke-4, tertunda. Dalam bentuk imunodefisiensi ini, kadar IgG dan IgA sering diturunkan, sedangkan kadar IgM berada dalam kisaran normal atau bahkan meningkat. B-limfosit, kelenjar getah bening dan amandel tidak berubah. Gangguan imunodefisiensi sementara ini terjadi pada 5-8% bayi (biasanya bayi prematur atau anak-anak dari keluarga immunocompromised) dan biasanya sembuh tanpa pengobatan pada usia 1,5-4 tahun.
Sindrom hiper-IgE (sindrom Job). Diagnosis "sindrom Job" didasarkan pada peningkatan berulang (setidaknya dua kali lipat) dalam konsentrasi serum total IgE di atas 1000 IU / ml dengan adanya dermatitis dan infeksi purulen dalam berulang dengan kursus "dingin": abses kulit, jaringan subkutan, kelenjar getah bening, otitis media. Bahaya khusus adalah episode pneumonia akut yang parah, termasuk episode destruktif dengan hasil pada pneumokel, abses hati. Ditandai dengan anomali skeletal, fraktur spontan tulang tubular, gambaran wajah displastik kasar. Mekanisme patogenetik penyakit ini adalah Th1 tidak mampu memproduksi interferon-γ. Hal ini menyebabkan peningkatan aktivitas Th2, yang dimanifestasikan dalam peningkatan produksi IgE. Yang terakhir menyebabkan pelepasan histamin, yang menghambat perkembangan respons inflamasi (pembentukan abses dingin dikaitkan dengan ini). Selain itu, histamin menghambat kemotaksis neutrofil.
Kandidiasis mukokutaneus kronis. Hal ini ditandai dengan lesi candida pada kulit, selaput lendir, kuku, kulit kepala. Penyakit ini didasarkan pada cacat unik pada limfosit-T, yang terdiri dari fakta bahwa sel-sel ini tidak dapat mengembangkan respons normal, khususnya, untuk menghasilkan faktor yang menghambat migrasi makrofag (MIF) ke antigen Candida albicans. . Tes kulit HRTT untuk antigen ini juga negatif. Pada saat yang sama, pasien memiliki jumlah limfosit T yang normal, dan respons mereka terhadap antigen lain tidak terganggu. Respon humoral terhadap antigen Candida tidak berubah. Sindrom ini dikaitkan dengan endokrinopati poliglandular autoimun. Terapi antijamur simtomatik digunakan dalam pengobatan.
Penyakit granulomatosa kronis (CGD). Ini adalah bentuk cacat fagositosis bawaan. Neutrofil memiliki kemotaksis normal, aktivitas penyerapan, tetapi pembentukan "ledakan pernapasan" terganggu. Mikroorganisme katalase-positif (Staphylococcus aureus, E. coli, Klebsiella, Serratia marcescens, Salmonella, jamur Aspergillus) membentuk granuloma di kelenjar getah bening, hati, paru-paru, dan saluran pencernaan. Ditandai dengan perkembangan limfadenitis berulang, abses (hati, paru, perirektal), osteomielitis, stomatitis ulseratif, rinitis, konjungtivitis. Beberapa pasien yang didiagnosis dengan CGD di masa kanak-kanak hidup hingga usia 30 tahun. Diagnosis dikonfirmasi oleh tes NBT (tes pemulihan tetrazolium nitro biru), yang memiliki nilai nol untuk patologi yang sedang dipertimbangkan. Pengobatan: asupan profilaksis harian antibiotik antistaphylococcal, interferon subkutan-γ 3 kali seminggu.
Berdasarkan pengamatan, kami telah membuat Daftar PID Chuvashia, yang mencakup 19 pasien dengan 7 bentuk defisiensi imun (Tabel 1).
Tabel 1
Daftar imunodefisiensi primer Chuvashia
Dari lebih dari 100 formulir PID terverifikasi yang diketahui, kami telah menetapkan 7. 19 formulir PID dijelaskan dalam daftar nasional Rusia. Perhatian ditarik pada fakta bahwa 15 dari PID yang disajikan dalam register didiagnosis hanya setelah pasien dipindahkan ke jaringan dewasa layanan medis. Daftar tidak termasuk anak-anak dengan hipogammaglobulinemia sementara pada usia dini. Hal ini disebabkan kurangnya kriteria diagnostik yang jelas untuk bentuk PID ini dan kesulitan dalam membedakan dengan keadaan imunodefisiensi sekunder pada anak di bawah usia 3 tahun. Selain itu, register tidak mengandung SCID, yang diketahui disebabkan oleh defek pada mekanisme humoral dan seluler dari respon imun, dan menyebabkan kematian anak-anak pada usia yang sangat dini. Mereka biasanya didiagnosis secara retrospektif pada otopsi dengan perbandingan klinis dan patologis. Sayangnya, di republik kami, biro patologis tidak mendaftarkan SCID, menghapus kematian kasus-kasus cacat sistem kekebalan yang diucapkan untuk infeksi berat tertentu (sepsis, meningitis, dll.). Tingkat insiden defisiensi IgA selektif juga tidak benar. Menurut banyak penulis, prevalensi bentuk PID ini adalah 1:500. Misalnya, dalam daftar PID wilayah Ural Selatan, penyakit ini menempati urutan pertama dalam hal frekuensi kejadian, dan mayoritas dengan defisiensi IgA selektif adalah anak-anak. Hanya pasien dewasa dengan PID yang dipertimbangkan yang termasuk dalam daftar republik kami. Tingkat deteksi defisiensi IgA selektif yang rendah kemungkinan besar terkait dengan variabilitas manifestasi klinis dari defek imunologis, yang seringkali diekspresikan dengan sangat lemah. Sejumlah besar pasien dengan imunopatologi memiliki peningkatan insiden infeksi virus pernapasan. Adalah penting bahwa peningkatan frekuensi infeksi, yang sering terjadi pada anak usia dini, menurun secara signifikan pada tahun-tahun berikutnya. Lebih dari 20% pasien dengan defisiensi IgA selektif menderita penyakit alergi dan autoimun. Pada beberapa pasien, defek imunologis tidak bermanifestasi secara klinis. Mungkin, frekuensi rendah defisiensi IgA selektif dalam register republik disebabkan oleh deteksi yang tidak memadai oleh spesialis. Contoh PID yang terdeteksi dengan baik di Chuvashia adalah CVID, yang terletak di daftar nasional Federasi Rusia di tempat kedua dalam hal prevalensi setelah defisiensi IgA selektif. Alasan identifikasi CVID yang efektif adalah kesadaran yang baik dari dokter jaringan dewasa tentang kriteria diagnostik untuk patologi ini karena demonstrasi berulang pasien pada analisis klinis dan konferensi Asosiasi Dokter Chuvashia.
Jadi, di Chuvashia, tingkat deteksi imunodefisiensi gabungan, defisiensi IgA selektif rendah, yang tampaknya disebabkan oleh kurangnya pengetahuan dasar tentang imunologi klinis di antara dokter dari berbagai spesialisasi (termasuk tentang masalah yang berkaitan dengan manifestasi klinis, diagnosis PID), serta dengan penggunaan metode diagnostik imunologis yang tidak memadai oleh dokter.
Imunodefisiensi sekunder. Keadaan imunodefisiensi sekunder sebagian besar umum di antara kontingen dewasa. Cacat yang didapat pada respon imun seluler lebih sering diamati, lebih jarang pada humoral. Alasan untuk ini, tampaknya, adalah bahwa sel T lebih sensitif terhadap faktor apoptogenik daripada sel B yang dilindungi dari kematian apoptosis oleh antigen Bcl pro-onkogen yang diekspresikan pada membrannya, dan apoptosis diketahui sebagai mekanisme utama kematian sel sel T. sistem kekebalan tubuh dan perkembangan defisiensi imun. Setiap faktor yang dapat menginduksi proses apoptosis sel T (radiasi pengion, stres, peningkatan kadar glukokortikosteroid dan etanol, infeksi, dll.) dapat memainkan peran kausal dalam terjadinya imunodefisiensi sel T sekunder. Insufisiensi sekunder dari respon imun humoral, sebagai suatu peraturan, berkembang dengan latar belakang penyakit serius yang sudah ada. Kondisi utama yang menyebabkan defisiensi didapat dari mekanisme humoral dari imunitas adaptif adalah sebagai berikut:
1) kekurangan protein yang terkait dengan sindrom malabsorpsi, pankreatitis kronis, penyakit celiac, penyakit luka bakar (sintesis molekul imunoglobulin terganggu karena kurangnya "bahan bangunan" - asam amino);
2) kondisi yang menyebabkan hilangnya imunoglobulin dan sel imunokompeten - sindrom nefrotik (dengan glomerulonefritis, filter glomerulus dapat dilewati tidak hanya untuk protein dengan berat molekul rendah, tetapi juga dengan berat molekul tinggi - globulin, termasuk imunoglobulin), perdarahan, limfore, luka bakar;
3) multiple myeloma (myeloma adalah klon abnormal dari B-limfosit yang telah memperoleh sifat pertumbuhan tak terkendali, memproduksi imunoglobulin dari kelas yang sama, satu spesifisitas, myeloma yang tumbuh menggantikan klon normal limfosit B di sumsum tulang, memproduksi imunoglobulin lainnya, sekitar 108, spesifisitas yang berbeda, selama pengembangan IgA myeloma mengurangi kadar IgG dan IgM, IgG myeloma disertai dengan penurunan IgA dan IgM, dan pada IgD myeloma dan penyakit rantai ringan, tiga kelas utama imunoglobulin berkurang);
4) sindrom splenektomi (ketika limpa diangkat, respon imun seluler menderita pada tingkat yang lebih rendah, tetapi hubungan humoral secara signifikan terhambat, karena limpa sebagian besar merupakan organ produksi antibodi).
Dengan kondisi ini, penurunan kandungan antibodi ke tingkat hipo-, agammaglobulinemia dapat diamati. Berbeda dengan bentuk bawaan dengan cacat sekunder dari mekanisme humoral dari respon imun, kadar imunoglobulin bervariasi tergantung pada perjalanan dan tingkat keparahan proses utama, isinya dapat dinormalisasi (tanpa terapi penggantian dengan obat imunoglobulin) selama periode tersebut. dari remisi penyakit yang mendasarinya.
Dipandu oleh data para ahli WHO, berikut ini harus disebut sebagai faktor etiopatogenik dari insufisiensi sekunder dari respon imun seluler:
1) paparan faktor fisik dan kimia:
- fisik (radiasi pengion, gelombang mikro, suhu udara tinggi atau rendah di zona iklim kering, dll.);
- kimia (imunosupresan, kemoterapi, kortikosteroid, obat-obatan, herbisida, pestisida, polusi industri lingkungan garam logam berat);
2) cara hidup manusia modern (tidak aktif secara fisik, kelebihan informasi dengan perkembangan penyakit "informasi");
3) malnutrisi (kekurangan mikronutrien esensial dalam ransum air-makanan harian - seng, tembaga, besi, vitamin - retinol, asam askorbat, alfa-tokoferol, asam folat; malnutrisi energi-protein, kelelahan, cachexia, gangguan metabolisme, obesitas);
3) infeksi virus:
- akut - campak, rubella, gondok, cacar air, flu, hepatitis, herpes, dll.;
- persisten - hepatitis B kronis, panensefalitis sklerosis subakut, AIDS, dll.;
- bawaan - cytomegaly, rubella (TORCH-kompleks);
4) invasi protozoa dan kecacingan (malaria, toksoplasmosis, leishmaniasis, trichinosis, ascariasis, dll.);
5) infeksi bakteri (staphylococcal, pneumococcal, meningococcal, tuberculosis, dll.);
6) tumor ganas, terutama limfoproliferatif;
7) penyakit autoimun;
- kondisi yang menyebabkan hilangnya sel imunokompeten (perdarahan, limfore);
- intoksikasi eksogen dan endogen (keracunan, tirotoksikosis, diabetes mellitus dekompensasi);
- pelanggaran regulasi neurohormonal (efek stres - trauma parah, pembedahan, fisik, termasuk olahraga, kelebihan beban, trauma mental);
- imunodefisiensi alami - anak usia dini, usia gerontologis, wanita hamil (paruh pertama kehamilan).
Imunodefisiensi sekunder adalah tajam(disebabkan oleh penyakit infeksi akut, trauma, keracunan, stres, dll.) dan kronis(berkembang dengan latar belakang penyakit pioinflamasi kronis, tumor, stres kronis, terapi imunosupresif, ketika tinggal di daerah dengan kondisi ekologi dan geokimia yang tidak menguntungkan, dll.). Imunodefisiensi akut didiagnosis berdasarkan deteksi kelainan pada indikator imunogram - penurunan jumlah limfosit T (CD3 +), T-helper (CD4 +), penurunan indeks imunoregulasi (CD4 + / CD8 +). Mereka, sebagai suatu peraturan, bersifat sementara dan secara bertahap berhenti dengan perjalanan yang menguntungkan dan pengobatan etiopatogenetik yang memadai dari penyakit yang mendasarinya dengan penggunaan yang terkenal, yang disebut obat dan agen fortifikasi (vitamin, adapagens, prosedur fisioterapi, dll.), serta terapi metabolisme energi (wobenzym, coenzyme Q10) ... Imunodefisiensi kronis dapat terjadi dalam tiga varian: 1) dengan tanda klinis dan laboratorium, 2) dengan tanda klinis tanpa adanya kelainan laboratorium, 3) dengan faktor penyebab (misalnya, hidup dalam kondisi lingkungan), tidak adanya manifestasi klinis dan adanya gangguan imunologis ... Jenis pertama lebih umum. Pada tipe kedua, ketika imunodefisiensi hanya dimanifestasikan secara klinis, tetapi tidak ada perubahan yang ditemukan pada imunogram tipikal, kerusakan sistem kekebalan pada tingkat yang lebih halus, yang tidak terdeteksi selama penelitian rutin, tidak dikecualikan. Secara formal nilai normal indikator status kekebalan, yang merupakan cerminan dari respons individu dari sistem kekebalan, dapat menjadi "patologis" untuk individu tertentu, tidak dapat memberikan tingkat resistensi organisme yang cukup tinggi. Tipe ketiga, yang mengungkapkan dirinya hanya sebagai tanda imunolaboratorium dari defisiensi imun, pada dasarnya, adalah pra-penyakit, faktor risiko penyakit yang terkait dengan defisiensi imun sekunder - infeksi, autoimun, onkologis, dll. Seringkali jenis imunodefisiensi ketiga disertai dengan tanda-tanda sindrom kelelahan kronis.
Sindrom Kelelahan Kronis dan Disfungsi Imun (CFS). Ini pertama kali dijelaskan oleh A. Lloyd et al Pada tahun 1984 dan ditandai sebagai kelelahan kronis yang dialami oleh pasien, yang tidak hilang setelah istirahat dan seiring waktu menyebabkan penurunan kinerja yang signifikan, baik mental maupun fisik. Deteksi ketidakseimbangan sistem kekebalan yang diucapkan pada pasien dengan CFS adalah dasar untuk transformasi nama penyakit menjadi sindrom kelelahan kronis dan disfungsi kekebalan. CFS terdaftar terutama di daerah yang secara ekologis tidak menguntungkan dengan level tinggi pencemaran lingkungan dengan zat kimia berbahaya atau dengan peningkatan tingkat radiasi. Faktor-faktor ini secara negatif mempengaruhi keadaan sistem kekebalan (terutama, mekanisme seluler kekebalan adaptif), yang tampaknya mendukung persistensi virus laten dengan kerusakan pada sistem saraf pusat dan aktivasi virus laten (virus herpes, virus Epstein-Barr). ). Permulaan manifestasi klinis CFS, sebagai suatu peraturan, dikaitkan dengan transfer masuk angin, lebih jarang - stres emosional... Gejala CFS terdiri dari kelelahan parah, kelemahan otot yang tidak hilang setelah tidur malam, kesulitan tidur, tidur dangkal dengan mimpi buruk, dan keadaan depresi berulang. Untuk pasien dengan CFS, terutama orang muda, sensitivitas terhadap infeksi virus pernapasan khas. Pasien mengeluh nyeri dan sakit tenggorokan (faringitis non-eksudatif). Pada beberapa pasien, penurunan berat badan, warna kulit pucat, dan penurunan turgor dicatat. Menurut sejumlah peneliti, dasar patofisiologis CFS adalah gangguan imunologis. Memang, pada kebanyakan pasien, ditemukan penurunan jumlah sel T, penurunan aktivitas proliferasi, penurunan fungsi sel NK, dan disimunoglobulinemia. Perawatan kompleks pasien dengan CFS termasuk penunjukan antidepresan trisiklik, obat antiinflamasi nonsteroid, imunomodulator dan adaptogen di bawah kendali imunogram.
Prinsip-prinsip koreksi keadaan imunodefisiensi. Koreksi insufisiensi humoral termasuk penunjukan imunoterapi substitusi dan stimulan produksi antibodi. Imunoterapi substitusi diindikasikan ketika konsentrasi total imunoglobulin menurun di bawah 5 g / l. Sediaan imunoglobulin (sandoglobulin, octagam, intraglobin atau imunoglobulin manusia normal untuk pemberian intravena) diberikan secara intravena 2 kali seminggu dengan dosis 0,1-0,2 g / kg dalam dosis bulanan hingga 1,2 g / kg. Stimulan produksi antibodi diindikasikan untuk agammaglobulinemia sesuai dengan jenis CVID: myelopid 3 mg (0,3% larutan 1 ml) secara intramuskular setiap hari 6-8 suntikan, natrium nukleinat - 0,2 g 3 kali sehari secara oral selama 21 hari atau Derinat larutan 1,5% 5 ml dengan interval 2-3 hari 8-10 injeksi intramuskular.
Dalam kasus kerusakan pada tautan fagositik, gunakan: polioksidanium 0,006-0,012 g untuk orang dewasa setiap hari pada 5 suntikan pertama, kemudian dengan interval 2-3 hari, untuk kursus 7-10 suntikan intramuskular; lycopid 1 tablet sekali sehari di bawah lidah selama 10 hari (tablet untuk orang dewasa - masing-masing 0,01 g); Solusi Derinat 0,25% - 2 tetes di hidung 3-4 kali sehari selama 10 hari.
Dalam kasus cacat pada tautan seluler kekebalan adaptif, berikut ini digunakan: 1) persiapan yang berasal dari timus (thymalin 0,010-0,020 gi / m pada malam hari 7-10 suntikan; timogen 0,01% -1 ml i / m setiap hari - 3 -10 suntikan; immunofan 0,005% - 1,0 ml s / c atau i / m 5-7 suntikan setiap hari atau setelah 2-3 hari, untuk kursus 8-10 suntikan); 2) obat interferon (interferon leukosit manusia 1.000.000 IU / m 2 kali seminggu hingga 6 bulan; reaferon 3.000.000-5.000.000 IU / m 2 kali seminggu selama 4 minggu hingga 6 bulan); 3) analog rekombinan IL-2 - roncoleukin 500.000-1.000.000 IU IV drip atau s / c dengan selang waktu 48-72 jam 3-5-10 suntikan; 4) stimulan interferonogenesis endogen (amiksin 0,125 g - pada hari pertama 2 tablet setelah makan, kemudian setiap hari 1 tablet; sikloferon - tablet 0,15 g dan larutan injeksi 12,5% - 2 ml, ditentukan sesuai dengan skema dasar untuk 1 , 2, 4, 6, 8, 11, 14, 17, 20, 23, 26, 29 hari).
BIBLIOGRAFI
- L.V. Kovalchuk, A.N. Cheredeev Apoptotic immunodeficiencies // Masalah modern alergologi, imunologi klinis dan imunofarmakologi: Abstrak. laporan 2 nat. Kongres RAKI. M., 1998.S. 615-619.
- Reznik I.B. Keadaan saat ini dari pertanyaan tentang imunodefisiensi primer // Pediatri. 1996. Nomor 2. S.4-14.
- Yartsev M.N., Yakovleva K.P. Daftar negara-negara imunodefisiensi primer dari Institut Imunologi Kementerian Kesehatan Federasi Rusia // Imunologi. 2005. Nomor 3. S.23-27.
- Bruton O.C. Agammaglobulinemia // Pediatri. 1952. Jil. 9.P.722-726.
- Cunningham-Rundles C. Analisis klinis dan imunologi dari 103 pasien dengan imunodefisiensi variabel umum // J. Clin. kekebalan. 1989. Jil. 9.P.22-33.
- Lloyd A.R. dkk. Kelainan imunologis pada sindrom kelelahan kronis // Med. J.Aus. 1989. Jil. 151. Hal. 122-124.
- Matamoros F.N. dkk... Sindrom imunodefisiensi primer di Spanyol: laporan pertama National Registry pada anak-anak dan orang dewasa // J. Clin. kekebalan. 1997. Jil. 17.P.333-339.
- sekelompok kondisi patologis, sebagian besar bersifat bawaan, di mana ada gangguan dalam pekerjaan tautan kekebalan tertentu. Gejalanya bervariasi, tergantung pada jenis penyakitnya, terutama ada peningkatan kerentanan terhadap agen bakteri dan virus. Diagnosis patologi dilakukan dengan metode penelitian laboratorium, analisis genetik molekuler (dengan bentuk herediter), mempelajari anamnesis pasien. Perawatan termasuk terapi penggantian, transplantasi sumsum tulang, dan tindakan pengendalian infeksi. Beberapa bentuk defisiensi imun tidak dapat disembuhkan.

Informasi Umum
Imunodefisiensi primer telah dipelajari secara aktif sejak 50-an abad XX - setelah kondisi pertama jenis ini, yang menerima namanya, dijelaskan pada tahun 1952 oleh dokter anak Amerika Ogden Bruton. Saat ini, lebih dari 25 jenis patologi diketahui, kebanyakan dari mereka - penyakit yang ditentukan secara genetik. Insiden berbagai jenis imunodefisiensi berkisar antara 1: 1.000 hingga 1: 5.000.000. Sebagian besar pasien adalah anak-anak di bawah usia 5 tahun, bentuk ringan dapat dideteksi untuk pertama kalinya pada orang dewasa. Dalam beberapa kasus, keadaan imunodefisiensi hanya terdeteksi oleh hasil tes laboratorium. Beberapa jenis penyakit digabungkan dengan banyak cacat perkembangan dan memiliki tingkat kematian yang tinggi.

Penyebab imunodefisiensi primer
Keadaan defisiensi imun yang bersifat primer mulai terbentuk pada tahap perkembangan intrauterin di bawah pengaruh berbagai faktor. Seringkali mereka dikombinasikan dengan cacat lain (distrofi, kelainan jaringan dan organ, fermentopati). Atas dasar etiologi, ada tiga kelompok utama patologi bawaan dari sistem kekebalan:
- Karena mutasi genetik. Sebagian besar penyakit timbul dari cacat pada gen yang bertanggung jawab untuk pengembangan dan diferensiasi sel imunokompeten. Warisan autosomal resesif atau terkait seks biasanya dicatat. Ada sebagian kecil dari mutasi spontan dan germinal.
- Akibat efek teratogenik. Masalah bawaan dengan kekebalan dapat disebabkan oleh efek racun dari berbagai sifat pada janin. Imunodefisiensi sering menyertai cacat perkembangan yang disebabkan oleh infeksi TORCH.
- Etiologi yang tidak jelas. Kelompok ini termasuk kasus-kasus ketika tidak mungkin untuk mengidentifikasi penyebab kelemahan sistem kekebalan tubuh. Ini mungkin masih merupakan kelainan genetik yang belum dijelajahi, efek teratogenik yang lemah atau tidak diketahui.
Studi tentang penyebab, patogenesis dan pencarian metode pengobatan imunodefisiensi primer terus berlanjut. Sudah ada indikasi seluruh kelompok kondisi serupa yang tidak memanifestasikan dirinya sebagai gejala yang diucapkan, tetapi dalam kondisi tertentu dapat memicu komplikasi infeksi.
Patogenesis
Mekanisme perkembangan defisiensi imun tergantung pada faktor etiologi. Dalam varian genetik yang paling umum dari patologi, karena mutasi beberapa gen, protein yang dikodekan oleh mereka tidak disintesis atau memiliki cacat. Tergantung pada fungsi protein, proses pembentukan limfosit, transformasinya (menjadi sel T atau B, sel plasma, sel pembunuh alami) atau pelepasan antibodi dan sitokin terganggu. Beberapa bentuk penyakit ditandai dengan penurunan aktivitas makrofag atau defisiensi kompleks dari banyak tautan sistem kekebalan. Varietas imunodefisiensi, yang disebabkan oleh pengaruh faktor teratogenik, paling sering muncul karena kerusakan dasar organ kekebalan - timus, sumsum tulang, jaringan limfoid. Keterbelakangan elemen-elemen tertentu dari sistem kekebalan menyebabkan ketidakseimbangannya, yang dimanifestasikan oleh melemahnya pertahanan tubuh. Imunodefisiensi primer dari setiap genesis menyebabkan perkembangan infeksi jamur, bakteri atau virus yang sering.
Klasifikasi
Jumlah jenis imunodefisiensi primer cukup banyak. Ini disebabkan oleh kompleksitas sistem kekebalan dan integrasi erat dari tautan individualnya, sebagai akibatnya kerusakan atau "penutupan" satu bagian berkontribusi pada melemahnya semua pertahanan tubuh secara keseluruhan. Sampai saat ini, klasifikasi bercabang yang kompleks dari kondisi seperti itu telah dikembangkan. Ini terdiri dari lima kelompok utama defisiensi imun, yang masing-masing mencakup beberapa jenis patologi yang paling umum. Dalam versi yang disederhanakan, klasifikasi ini dapat disajikan sebagai berikut:
- Defisiensi primer imunitas seluler. Kelompok menyatukan kondisi yang disebabkan oleh aktivitas yang tidak mencukupi atau tingkat limfosit T yang rendah. Alasannya mungkin karena insufisiensi timus, fermentopathies, dan kelainan lainnya (terutama genetik). Bentuk paling umum dari jenis imunodefisiensi ini adalah sindrom DiGeorge dan Duncan, orotaciduria, dan defisiensi enzim limfosit.
- Defisiensi primer dari imunitas humoral. Sekelompok kondisi di mana fungsi limfosit B yang dominan berkurang, sintesis imunoglobulin terganggu. Sebagian besar bentuk termasuk dalam kategori disgammaglobulinemia. Sindrom Bruton, West, defisiensi IgM atau transcobalamin II yang paling terkenal.
- Gabungan imunodefisiensi primer. Sekelompok luas penyakit dengan penurunan aktivitas imunitas seluler dan humoral. Menurut beberapa laporan, tipe ini mencakup lebih dari setengah dari semua jenis defisiensi imun. Diantaranya, ada yang parah (sindrom Glanzmann-Riker), sedang (penyakit Louis-Bar, sindrom limfoproliferatif autoimun) dan imunodefisiensi ringan.
- Kegagalan fagosit primer. Patologi genetik menyebabkan penurunan aktivitas makro dan mikrofag - monosit dan granulosit. Semua penyakit jenis ini dibagi menjadi dua kelompok besar - neutropenia dan cacat pada aktivitas dan kemotaksis leukosit. Contohnya adalah Kostman neutropenia, sindrom sel darah putih malas.
- melengkapi kekurangan protein. Sekelompok keadaan imunodefisiensi, yang perkembangannya disebabkan oleh mutasi pada gen yang mengkode komponen pelengkap. Akibatnya, pembentukan kompleks penyerang membran terganggu, fungsi lain yang melibatkan protein ini terganggu. Ini menyebabkan imunodefisiensi primer yang bergantung pada komplemen, kondisi autoimun atau.
Gejala Imunodefisiensi Primer
Gambaran klinis berbagai bentuk defisiensi imun sangat beragam, dapat mencakup tidak hanya gangguan imunologis, tetapi juga malformasi, proses tumor, masalah dermatologis. Hal ini memungkinkan dokter anak atau ahli imunologi untuk membedakan antara berbagai jenis patologi bahkan pada tahap pemeriksaan fisik dan tes laboratorium dasar. Namun, ada gejala umum tertentu yang serupa pada setiap kelompok penyakit. Kehadiran mereka menunjukkan tautan atau bagian mana dari sistem kekebalan yang paling terpengaruh.
Dengan defisiensi primer imunitas seluler, penyakit virus dan jamur terjadi. Ini adalah sering masuk angin, lebih parah dari biasanya, perjalanan infeksi virus masa kanak-kanak (cacar air, gondok), lesi herpes parah. Seringkali ada kandidiasis rongga mulut, alat kelamin, ada kemungkinan besar infeksi jamur pada paru-paru, saluran pencernaan. Individu dengan kekurangan dalam hubungan seluler sistem kekebalan memiliki peningkatan risiko mengembangkan neoplasma ganas - limfoma, kanker berbagai lokalisasi.
Melemahnya pertahanan humoral tubuh biasanya memanifestasikan dirinya peningkatan sensitivitas terhadap agen bakteri. Pasien mengembangkan pneumonia, lesi kulit pustular (pioderma), sering menjadi parah (staphylo- atau streptoderma, erisipelas). Dengan penurunan tingkat sekretori IgA, terutama selaput lendir (konjungtiva mata, permukaan rongga mulut dan hidung), serta bronkus dan usus, terpengaruh. Imunodefisiensi gabungan disertai dengan komplikasi virus dan bakteri. Seringkali, bukan manifestasi dari kurangnya kekebalan yang mengemuka, tetapi gejala lain yang lebih spesifik - anemia megaloblastik, malformasi, tumor timus dan jaringan limfoid.
Neutropenia kongenital dan melemahnya fagositosis granulosit juga ditandai dengan seringnya terjadinya infeksi bakteri. Sering ada proses inflamasi purulen dengan pembentukan abses di berbagai organ, dengan tidak adanya pengobatan, pembentukan phlegmon, sepsis mungkin terjadi. Gambaran klinis dari komplemen-terkait imunodefisiensi disajikan baik sebagai penurunan resistensi tubuh terhadap bakteri, atau dalam bentuk lesi autoimun. Varian terpisah dari gangguan kekebalan yang bergantung pada komplemen - ANO herediter - dimanifestasikan oleh edema berulang dari berbagai bagian tubuh.
Komplikasi
Semua jenis imunodefisiensi primer disatukan oleh peningkatan risiko komplikasi infeksi yang parah. Karena melemahnya pertahanan tubuh, mikroba patogen menyebabkan kerusakan parah berbagai badan... Paling sering, paru-paru (pneumonia, bronkitis, bronkiektasis), selaput lendir, kulit, dan organ saluran pencernaan terpengaruh. Dalam kasus penyakit yang parah, infeksilah yang menyebabkan kematian pada masa bayi. Gangguan bersamaan dapat memperburuk patologi - anemia megaloblastik, anomali dalam perkembangan jantung dan pembuluh darah, kerusakan limpa dan hati. Beberapa bentuk keadaan imunodefisiensi dalam jangka panjang dapat menyebabkan terbentuknya tumor ganas.
Diagnostik
Dalam imunologi, sejumlah besar teknik digunakan untuk menentukan keberadaan dan identifikasi jenis imunodefisiensi primer. Paling sering, keadaan imunodefisiensi bersifat bawaan, sehingga sudah dapat dideteksi pada minggu-minggu dan bulan-bulan pertama kehidupan seorang anak. Sering bakteri atau penyakit virus, terbebani sejarah turun-temurun, adanya malformasi lainnya. Varietas imunodefisiensi yang bermanifestasi lemah dapat ditentukan kemudian, sering ditemukan secara kebetulan selama tes laboratorium. Metode utama untuk mendiagnosis gangguan kekebalan herediter dan bawaan adalah:
- Pemeriksaan umum. Dimungkinkan untuk mencurigai adanya defisiensi imun yang nyata bahkan ketika memeriksa kulit. Pada anak-anak yang sakit, dermatomikosis parah, lesi pustular, atrofi dan erosi selaput lendir sering terdeteksi. Beberapa bentuk juga dimanifestasikan oleh edema jaringan lemak subkutan.
- Tes laboratorium. Rumus leukosit dalam analisis umum darah terganggu - leukopenia, neutropenia, agranulositosis dan anomali lainnya dicatat. Dengan beberapa varietas, peningkatan tingkat kelas leukosit tertentu dimungkinkan. Tes darah biokimia untuk imunodefisiensi primer tipe humoral mengkonfirmasi disgammaglobulinemia, adanya metabolit yang tidak biasa (dengan fermentopathies).
- Studi imunologi spesifik. Untuk memperjelas diagnosis, sejumlah teknik digunakan untuk menentukan aktivitas sistem kekebalan tubuh. Ini termasuk analisis leukosit teraktivasi, aktivitas fagositosis granulosit, tingkat imunoglobulin (secara umum dan fraksi individu - IgA, E, G, M). Juga, studi tentang tingkat fraksi komplemen, interleukin dan status interferon pasien dilakukan.
- Analisis genetik molekuler. Jenis turun-temurun dari imunodefisiensi primer dapat didiagnosis dengan mengurutkan gen yang mutasinya menyebabkan satu atau lain bentuk penyakit. Ini adalah bagaimana diagnosis dikonfirmasi dalam sindrom Di Giorgi, Bruton, Duncan, Wiskott-Aldrich dan sejumlah keadaan imunodefisiensi lainnya.
Diagnosis banding terutama dilakukan dengan imunodefisiensi sekunder yang didapat, yang dapat disebabkan oleh kontaminasi radioaktif, keracunan zat sitotoksik, patologi autoimun dan onkologis. Sangat sulit untuk membedakan penyebab defisiensi dengan bentuk yang dihaluskan, terutama ditentukan pada orang dewasa.
Pengobatan imunodefisiensi primer
Prinsip pengobatan yang seragam untuk semua bentuk patologi tidak ada karena perbedaan etiologi dan patogenesis. Dalam kasus yang paling parah (sindrom Glanzmann-Rinicker, agranulositosis Kostman), tindakan terapeutik apa pun bersifat sementara, pasien meninggal karena komplikasi infeksi. Beberapa jenis defisiensi imun primer diobati dengan sumsum tulang atau transplantasi jaringan timus janin. Kurangnya kekebalan seluler dapat dilemahkan dengan penggunaan faktor perangsang koloni khusus. Dalam kasus fermentopati, terapi dilakukan dengan menggunakan enzim atau metabolit yang hilang - misalnya, sediaan biotin.
Dengan disglobulinemia (imunodefisiensi humoral primer), terapi substitusi digunakan - pengenalan imunoglobulin dari kelas yang hilang. Dalam pengobatan bentuk apa pun, sangat penting untuk memperhatikan penghapusan dan pencegahan infeksi. Pada tanda-tanda pertama infeksi bakteri, virus atau jamur, pasien diberi resep obat yang sesuai. Seringkali, dosis yang lebih tinggi diperlukan untuk menyembuhkan patologi infeksi sepenuhnya. obat... Semua vaksinasi dibatalkan pada anak-anak - dalam banyak kasus mereka tidak efektif, dan beberapa bahkan berbahaya.
Prakiraan dan pencegahan
Prognosis dari imunodefisiensi primer sangat bervariasi dengan jenis yang berbeda patologi. Bentuk parah bisa tidak dapat disembuhkan, menyebabkan kematian pada bulan-bulan pertama atau tahun-tahun kehidupan seorang anak. Varietas lain dapat berhasil dikendalikan dengan terapi substitusi atau metode pengobatan lain, dengan hanya sedikit penurunan kualitas hidup pasien. Bentuk ringan tidak memerlukan intervensi medis biasa, namun, pasien harus menghindari hipotermia dan kontak dengan sumber infeksi, jika ada tanda-tanda infeksi virus atau bakteri, hubungi spesialis. Tindakan pencegahan, mengingat sifat imunodefisiensi primer yang turun-temurun dan seringkali bawaan, terbatas. Ini termasuk konseling medis dan genetik orang tua sebelum mengandung anak (dengan faktor keturunan) dan diagnosis genetik prenatal. Selama kehamilan, wanita harus menghindari kontak dengan zat beracun atau sumber infeksi virus.