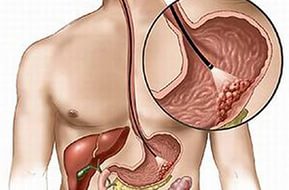
Protokol rancangan untuk diferensial diagnosis dan pengobatan sindrom kolestasis pada bayi baru lahir. Penyakit peradaban pada anak-anak: lebih lanjut tentang kolestasis
Pada 10 Mei 2012, konferensi ilmiah-praktis republik "Cholestasis syndrome pada anak-anak" diadakan di Kazan. Penyelenggara langsung konferensi adalah Departemen Rumah Sakit Anak-anak KSMU (kepala departemen, profesor V. P. Bulatov). Sejumlah dokter anak Republik Tatarstan, ahli neonatologi, dokter spesialis terkait diundang untuk berpartisipasi dalam konferensi - total sekitar 150 orang. Kepala dokter anak dari Kementerian Kesehatan Republik Tatarstan, I.G. Chigvintsev, Profesor A.P. Kiyasov - Wakil Rektor untuk Karya Ilmiah dan Inovatif KSMU, Kepala Dokter Rumah Sakit Klinis Anak-Anak Republik Kementerian Kesehatan Republik Tatarstan Shavaliyev.
 Menurut kepala dokter anak republik Irina G. Chigvintseva Dalam 20 tahun terakhir, banyak yang berubah dalam diagnosis dan pengobatan penyakit pada saluran empedu dan hati. “Dalam banyak hal, pengalaman klinis kami, perluasan berbagai studi diagnostik memungkinkan kami untuk mengisolasi berbagai nosologi dari kelas penyakit umum. Sindrom kolestasis hanyalah salah satunya. Ini terjadi cukup sering di antara bayi baru lahir dan dikaitkan dengan komplikasi parah pada periode prenatal, adalah akibat dari kebangkrutan bawaan dari sistem hepatobilier. Dalam kondisi kami, ketika kami beralih ke perawatan anak-anak dengan berat lahir sangat rendah, masalah diagnosis dan perawatan tepat waktu mendapatkan makna saat ini yang serius bagi kami.
Menurut kepala dokter anak republik Irina G. Chigvintseva Dalam 20 tahun terakhir, banyak yang berubah dalam diagnosis dan pengobatan penyakit pada saluran empedu dan hati. “Dalam banyak hal, pengalaman klinis kami, perluasan berbagai studi diagnostik memungkinkan kami untuk mengisolasi berbagai nosologi dari kelas penyakit umum. Sindrom kolestasis hanyalah salah satunya. Ini terjadi cukup sering di antara bayi baru lahir dan dikaitkan dengan komplikasi parah pada periode prenatal, adalah akibat dari kebangkrutan bawaan dari sistem hepatobilier. Dalam kondisi kami, ketika kami beralih ke perawatan anak-anak dengan berat lahir sangat rendah, masalah diagnosis dan perawatan tepat waktu mendapatkan makna saat ini yang serius bagi kami.
“Pada bayi baru lahir dan bayi pada hari pertama kehidupan, sindrom kolestasis adalah salah satu manifestasi paling awal dari penyakit hati dan saluran empedu. Prasyarat utama adalah fitur morfo-fungsional dari sistem hepatobilier pada usia ini. Pada usia ini, ada jumlah asam amino yang relatif rendah, serta ketidakmatangan semua tahap sirkulasi hepatik dan usus. Fitur morfologis dan fungsional menunjukkan perkembangan kondisi patologis dalam kondisi tertentu, "kata profesor. Di bawah sindrom kolestasis umumnya dipahami sebagai pelanggaran formasi ekskresi empedu dalam sistem empedu, yang mengarah pada peningkatan komponen empedu dalam darah dan aliran yang tidak mencukupi dalam usus. Sindrom kolestasis memiliki manifestasi klinis dan laboratorium yang khas. Dalam kebanyakan kasus, sindrom kolestasis dikombinasikan dengan sindrom sitolisis dari peningkatan aktivitas enzim transaminase, tetapi juga dengan tanda-tanda insufisiensi hepatoseluler. Manifestasi klinis kolestasis adalah ikterus, hepatomegali, tinja Acholia, warna urin jenuh. Taktik pengobatan anak-anak dengan sindrom kolestasis melibatkan identifikasi faktor-faktor yang berkontribusi terhadap perkembangan kolestasis, maka perlu untuk mengecualikan penyakit hati, efektivitas pengobatan yang tergantung pada waktu pelaksanaannya. Setelah itu, pengobatan yang memadai dari penyakit yang mendasarinya diperlukan, pengecualian atau pembatasan obat hepatotoksik dan produk darah, awal paling awal dari nutrisi enteral, pengenalan nutrisi terapeutik dengan peningkatan kadar CT, vitamin yang larut dalam lemak setelah 10 hari, pemberian obat hormon dikontraindikasikan, pemberian obat hormon dikontraindikasikan. Menurut profesor, semua penyakit pada saluran empedu biasanya dibagi menjadi kolestasis ekstrahepatik dan kolestasis intrahepatik. Dalam kolestasis intrahepatik, acholium tinja divisualisasikan, dalam kolestasis ekstrahepatik - sebaliknya. Dalam laporan tersebut, pembicara juga menguraikan sindrom Byler. Menurut pembicara, anak-anak dengan sindrom ini merupakan kelompok risiko untuk pengembangan kanker. Taktik penatalaksanaan anak dengan ASD 1 dan 2 jenis (penyakit Byler): memberi tahu keluarga bahwa ada risiko terkena tumor ganas, serta kelahiran anak yang sakit dengan kehamilan berulang. Juga, anak-anak dengan sindrom Byler harus dipantau setiap dua atau tiga bulan. Terapi suportif akan terdiri dari nutrisi terapeutik, penggunaan vitamin yang larut dalam lemak, mikro-dan makronutrien, obat-obatan yang mengurangi pruritus. Profesor itu menyebutkan manajemen anak-anak dengan sindrom Alagille. Prognosis hidup pada sindrom Alajille tergantung pada perjalanan penyakit, upaya koreksi bedah salah. Anna Vladimirovna membahas pertanyaan tentang diagnosis dan pengobatan hepatitis neonatal, peradangan hati yang disebabkan oleh patogen hepatotropik: yang paling sering bersifat oportunistik. Gangguan metabolisme juga disajikan kepada peserta konferensi. Ini termasuk: tirosinemia, fruktosemia, gangguan sintesis asam empedu, kolestasis intrahepatik keluarga progresif, fibrosis kistik, dan banyak lagi. Dimungkinkan untuk mencurigai gangguan metabolik seperti itu jika analisis keluarga berisi kasus kematian anak-anak sebelumnya dari sepsis dengan patogen yang tidak dikenal, sindrom kematian mendadak, penyebab yang tidak teridentifikasi. Selain itu, gejala gangguan metabolisme adalah gangguan kondisi umum: regurgitasi, muntah, penurunan berat badan.
Kemudian kepala departemen terapi rumah sakit KSMU, profesor V.P. Bulatov. Dia mempresentasikan laporan "Penyakit batu empedu di masa kanak-kanak: pendekatan berbeda untuk terapi." "Penyakit batu empedu (ICD) adalah penyakit peradaban," profesor itu memulai. Menurut laporan itu, frekuensi cholelithiasis (cholelithiasis) meningkat di kalangan orang muda usia 16-35 tahun, dengan USG bayi baru lahir dari empat hari pertama, batu empedu ditemukan 0,5%. Peningkatan pertumbuhan cholelithiasis dijelaskan oleh peningkatan diagnosa, dan pertumbuhan sebenarnya dari penyakit ini berhubungan dengan kekhasan nutrisi, ketidakaktifan fisik, degradasi lingkungan. Alasan pembentukan batu empedu kolesterol adalah penurunan fungsi kontraktil kantong empedu, suatu kelebihan kolesterol empedu. Menurut profesor, lumpur empedu (akumulasi empedu asing) terbentuk pada wanita yang menggunakan kontrasepsi oral dan pada wanita hamil, serta pasien dengan nutrisi parenteral atau pada orang yang kelaparan. Juga, faktor-faktor pembentukan lumpur bilier meliputi penggunaan diet rendah kalori untuk mengurangi berat badan, serta penyakit-penyakit seperti mikrosit dan anemia sel sabit, sirosis hati, virus hepatitis. Dari tahun 1997 hingga 2012, 99 pasien dengan JCB dirawat di Rumah Sakit Klinis Republik Anak Kementerian Kesehatan Republik Tajikistan, jumlah yang berlaku di antara mereka adalah anak perempuan berusia 12-14 tahun. Pada 30% pasien, kecenderungan herediter tercatat terutama pada garis ibu. Pasien seperti ini direkomendasikan diet - tabel nomor 5. "Ini adalah pengobatan yang efektif 50%," kata profesor. Dalam laporannya, profesor juga menyoroti indikasi untuk terapi konservatif pada tahap kedua GCB. Jika batu empedu terdeteksi dan tanpa adanya kolik bilier pada anak di bawah usia tiga tahun, hanya observasi yang direkomendasikan. Pada usia tiga hingga dua belas tahun - operasi diindikasikan. Pada anak-anak di masa remaja, hanya taktik hamil yang direkomendasikan.
Selama konferensi, para ahli juga membahas topik-topik seperti Cholestasis Syndrome di Fetal Hepatitis, menganalisis penyebab kolestasis pada anak-anak, serta perawatan anak-anak dengan atresia bilier.
Di akhir konferensi, para peserta bertukar pandangan dan mengajukan pertanyaan kepada para dosen.
Alfiya Khasanova
PROTOKOL GAMBAR
DIAGNOSTIK PERBEDAAN DAN PENGOBATAN SINDROM
CHOLESTASIS PADA ANAK-ANAK BERITA BARU
Pendahuluan
Salah satu gangguan metabolisme yang paling sering terdeteksi pada periode neonatal adalah peningkatan konsentrasi bilirubin serum. Dengan tingkat lebih dari 68 μmol / l, neonatus tampak kulit dan sklera berwarna kuning. Hiperbilirubinemia pada hari-hari pertama kehidupan dapat disebabkan oleh penyebab fisiologis dan patologis dan karenanya selalu memerlukan perhatian khusus. Peningkatan intensitas penyakit kuning, warna kehijauannya bersama dengan peningkatan bertahap dalam ukuran hati, perubahan konsistensi dari elastis menjadi padat, penampilan tinja Acholia dan warna urin gelap menunjukkan pelanggaran fungsi ekskresi sistem hepatobiliary - neonatus kolestasis. Konfirmasi laboratorium dari sindrom ini adalah peningkatan fraksi langsung bilirubin lebih dari 15-20% dari total level, peningkatan konsentrasi kolesterol, beta-lipoprotein (β-LPD), asam empedu (FA), serta tingkat enzim alkaline phosphatase (AP) dan gamma -glutamine transferase (GGT).
Penyebab sindrom kolestasis pada periode neonatal dapat menjadi fitur morfofungsional dari hati dan saluran empedu, yang ditandai dengan tingkat tinggi sintesis asam empedu dan ketidakdewasaan sirkulasi hepato-intestinal mereka. Selain itu, sudah di bulan pertama kehidupan, tanda-tanda klinis pertama yang menunjukkan patologi hati dan saluran empedu, yang bermanifestasi dalam bentuk sindrom kolestasis, dapat dideteksi.
Selama 20 tahun terakhir, pemahaman kami tentang dasar-dasar dan patofisiologi banyak penyakit hati telah semakin dalam. Pengenalan pendekatan baru untuk diagnosis dan pengobatan, akumulasi pengalaman klinis telah memungkinkan untuk menetapkan sejumlah bentuk nosokologis baru, yang sampai saat ini disebut hepatitis neonatal idiopatik. Menimbang bahwa, efektivitas pengobatan penyakit hati bawaan tergantung pada waktu onsetnya, masalah diagnosis dini sangat penting.
Pembentukan kolestasis neonatal mungkin karena penyakit pada sistem hepatobilier, serta kombinasi faktor patologis non-spesifik dari periode perinatal, yaitu, memiliki asal ekstrahepatik.
Terlepas dari etiologi kolestasis, perawatan dari kategori pasien ini melibatkan pengangkatan nutrisi terapeutik, tambahan vitamin yang larut dalam lemak, serta penggunaan obat koleretik asam ursodeoxycholic. Dalam kasus kolestasis karena penyebab ekstrahepatik (sementara) selama pengobatan, ada tren positif dan pemulihan bertahap dari kondisi patologis. Pada penyakit hati dan sistem pengeluaran empedu untuk mengklarifikasi penyebab dan penunjukan tepat waktu terapi etiopatogenetik, anak-anak memerlukan pemeriksaan mendalam di departemen khusus.
Kolestasis neonatal karena penyebab ekstrahepatik.
Struktur penyebab ekstrahepatik pembentukan kolestasis neonatal didominasi oleh kondisi disertai dengan perkembangan hipoksia atau iskemia sistem hepatobilier, hipoperfusi saluran pencernaan, hipoglikemia persisten, asidosis metabolik, dan gagal jantung kongestif .
Gangguan fungsi ekskresi dari sistem hepatobilier dapat dideteksi pada anak-anak dengan penyakit hemolitik pada bayi baru lahir dengan latar belakang peningkatan konsentrasi bilirubin yang signifikan. Pada saat yang sama, ada perubahan dalam sifat koloid dari empedu dan peningkatan viskositasnya. Dalam beberapa kasus, bilirubin dapat memiliki efek toksik langsung pada membran hepatosit dan mitokondria sel. Tempat penting ditempati oleh infeksi bakteri sistemik dan lokal. Sintesis dan ekskresi kaskade mediator inflamasi yang kompleks oleh sel Kupffer, serta hepatosit dan sel endotel sinusoid, memiliki dampak langsung pada pembentukan dan ekskresi empedu. Langkah-langkah terapi yang dilakukan oleh bayi baru lahir di unit perawatan intensif dan perawatan intensif termasuk obat-obatan yang berpotensi hepatotoksik, nutrisi parenteral lengkap, yang juga berkontribusi terhadap gangguan keadaan fungsional sistem hepatobilier. Perkembangan kolestasis lebih sering diamati pada bayi baru lahir prematur dengan aksi simultan dari beberapa faktor patologis dan iatrogenik pada fungsi hati dan kondisi saluran empedu. Perubahan ini didasarkan pada berbagai tingkat perubahan destruktif pada saluran empedu, gangguan permeabilitas membran hepatosit dan senyawa antar sel, yang dalam banyak kasus bersifat reversibel dengan terapi tepat waktu. Ciri khas kolestasis neonatal karena penyebab ekstrahepatik adalah ketergantungannya pada keparahan dan durasi kondisi patologis periode perinatal dan aksi faktor iatrogenik. Ketika kondisi umum anak membaik dan resolusi penyakit yang mendasarinya, dalam kebanyakan kasus terjadi penurunan kolestasis secara bertahap. Namun, efek residualnya dapat bertahan lama, hingga 6-8 bulan kehidupan. Diagnosis kolestasis neonatal, yang merupakan komplikasi dari patologi ekstrahepatik yang parah, ditetapkan dengan mengidentifikasi faktor-faktor yang berkontribusi terhadap perkembangannya dan tidak termasuk penyakit pada sistem hepatobilier.
Terapi dalam kasus-kasus ini termasuk pengobatan yang memadai dari penyakit yang mendasarinya, pembatasan penggunaan obat-obatan yang berpotensi hepatotoksik dan produk-produk darah. Penggunaan sebagian besar preparat koleretik lainnya yang mengandung asam empedu primer (choleenzime, flaminum, allohol, dan lain-lain) memiliki keterbatasan pada periode neonatal, karena pada usia ini mereka ditandai oleh formasi tinggi dengan efek toksik.
Penyakit hati dan saluran empedu, dimanifestasikan oleh sindrom kolestasis pada bayi baru lahir dan anak kecil (Tabel 1).
Tabel 1
Penyakit hati dan saluran empedu, dimanifestasikan oleh sindrom kolestasis pada bayi baru lahir dan anak kecil
Kolestasis ekstrahepatik
Atresia saluran empedu ekstrahepatik
Kista saluran empedu yang umum
- "Sumbat empedu" dan / atau batu saluran empedu
Kompresi saluran empedu umum
Kolestasis intahepatik
1. Kolestasis intrahepatik keluarga progresif (PFW)
Tipe 1 (penyakit Byler)
Tipe 11 (sindrom Byler)
Tipe 111 (defisiensi gen MDR3)
2. Kolestasis intrahepatik jinak keluarga
3. Gangguan metabolisme
Kekurangan alfa-1-antitripsin
Galaktosemia
Fruktosemia
Tirosinemia
Pelanggaran sintesis asam empedu, karena kekurangan enzim
Insufisiensi Peroxisomal (sindrom Zellweiger),
Hemokromatosis neonatal
Niemann-pick tipe penyakit C
Insufisiensi mitokondria
4. Dan penyakit menular (virus, bakteri, disebabkan oleh protozoa)
5. Gangguan endokrin
Hipopituitarisme
Hipotiroidisme
6. Kelainan kromosom
Trisomi 13, 17 atau 18 kromosom
7. Kolestasis terkait dengan nutrisi parenteral lengkap
8. Kolestasis disebabkan oleh efek toksik dari obat-obatan
9. Lainnya
Sindrom Alajille
Bentuk nonsyndromic dari hipoplasia intrahepatik
Kolangitis sclerosing perinatal
Hepatitis neonatal idiopatik
Tergantung pada tingkat kerusakan sistem hepatobilier, sudah lazim untuk mengisolasi penyakit yang dimanifestasikan oleh kolestasis ekstrahepatik dan intrahepatik, diagnosis banding di antara mereka didasarkan pada kombinasi tiga gejala: persistensi acholia tinja, tingkat GGT darah dan visualisasi kandung empedu dengan ultrasound puasa. (tabel 2)
Tabel 2.
Diagnosis banding antara kolestasis ekstrahepatik dan intrahepatik pada bayi baru lahir.
Jenis kolestasis
Indikator:
Extrahepatik
Kolestasis
Kolestasis intahepatik
Kegigihan bangku acholias
Permanen
Tidak konstan
Tingkat darah GGT
Visualisasi kandung empedu dengan USG
Tidak dirender
Divisualisasikan
GGT - gamma glutamine transferase, batu empedu - kantong empedu, ultrasound - ultrasound.
Kolestasis ekstrahepatik.
Sifat terus-menerus dari tinja Acholia, peningkatan kadar serum enzim GGG, dan kurangnya visualisasi kandung empedu selama USG puasa adalah tanda karakteristik kolestasis ekstrahepatik, yang penyebabnya pada usia ini adalah:
1. Atresia saluran empedu ekstrahepatik
2. Kista saluran empedu yang umum
3. "Colokan empedu" dan / atau batu dari saluran empedu yang umum.
Penyebab paling umum dari kolestasis ekstrahepatik dan kolestasis neonatal secara umum adalah atresia saluran empedu ekstrahepatik (AVZHP), fitur karakteristik di antaranya adalah:
1. Dalam kebanyakan kasus, anak-anak dengan AVZHP lahir dengan istilah penuh dengan indikator antropometrik yang sesuai dengan norma fisiologis.
2. Ikterus muncul pada 2-3 hari kehidupan, yaitu, dalam hal normal untuk ikterus fisiologis. Sekitar dua pertiga pasien mencatat adanya "celah terang" - mengurangi intensitas penyakit kuning pada akhir 1-2 minggu kehidupan, diikuti oleh peningkatan bertahap dan munculnya penyakit kuning kehijauan pada akhir 1 bulan.
3. Tinja Aholy adalah tanda klinis awal dan paling persisten dari penyakit ini, penampilannya sering didahului dengan keluarnya mekonium.
4. Karakteristik AVZHP adalah tidak adanya hepatomegali saat lahir dengan peningkatan ukuran hati dan perubahan konsistensi dari elastis menjadi padat selama 2 bulan pertama kehidupan.
5. Pada usia 1 bulan kehidupan, sindrom hemoragik dapat terjadi (perdarahan dari selaput lendir saluran pencernaan, luka umbilikal, perdarahan intrakranial) yang disebabkan oleh kekurangan faktor pembekuan darah yang tergantung vitamin K (PTD atau PTV) sebagai akibat dari pelanggaran penyerapan vitamin K dalam usus.
6. Pada usia 1-2 bulan kehidupan, sebagai aturan, defisit berat terbentuk, keparahannya tergantung pada jenis pemberian makan anak.
7. Tanda laboratorium paling awal dari penyakit ini adalah peningkatan bilirubin karena fraksi langsung dalam serum lebih dari 20% dari total kadar bilirubin.
8. Ditandai dengan peningkatan penanda biokimia kolestasis lainnya (gamma-glutamine transferase (GGT), β-lipoprotein, kolesterol, alkali fosfatase, asam empedu, dll.), Keparahan yang dalam dinamika meningkat dari peningkatan minimum dalam 2-3 minggu pertama kehidupan hingga peningkatan signifikan menjadi 2-3 bulan.
9. Enzim sitolisis (ALT, AST) meningkat secara moderat, dan, biasanya, tertunda. Dalam kebanyakan kasus, selama 2-3 minggu pertama setelah kelahiran, angka-angka ini tetap dalam kisaran normal dan kemudian secara bertahap meningkat.
10. Indikator yang mencerminkan fungsi protein-sintetik hati (albumin, fibrinogen, PTI, dan lainnya) tidak berubah pada tahap awal penyakit.
11. Metode visualisasi sistem hepatobilier yang informatif adalah pemindaian ultrasound, di mana kandung empedu saat perut kosong tidak divisualisasikan atau dideteksi sebagai "tali hiperekhoik". Dalam beberapa kasus, atresia saluran empedu mengungkapkan perluasan saluran empedu intrahepatik, lebih jarang - kista di gerbang hati dan polisplen.
12. Skintigrafi hepatobilier, kolesistokolangiografi retrograde (RCPG), pencitraan resonansi magnetik (MRI) dan biopsi hati merupakan nilai diagnostik tambahan. Dengan skintigrafi hepatobiliari, yang memiliki sensitivitas dan spesifisitas yang cukup tinggi pada pasien dengan AVHP, ada kekurangan zat radioisotop yang memasuki usus, bersama dengan penyerapan yang memuaskan dan fungsi akumulatif hati. Melakukan RHPG memiliki sejumlah keterbatasan teknis pada anak-anak selama bulan-bulan pertama kehidupan.
13. Sebuah studi morfologis biopsi hati menunjukkan gumpalan empedu dengan berbagai tingkat keparahan, proliferasi saluran empedu, pembengkakan saluran portal dan fibrosis.
Diagnosis galaktosemia ditegakkan berdasarkan peningkatan serum galaktosa, mengurangi zat dalam urin, defisiensi enzim galaktosa-1-fosfat uridyltransferase dalam eritrosit, leukosit dan hepatosit. Pengujian genetik terhadap lokus spesifik juga dimungkinkan.
Metode utama pengobatan adalah diet dengan eliminasi lengkap galaktosa dan laktosa (Pregestimil, Nutramigen, AL110, dan lainnya). Awal nutrisi terapi yang tepat waktu mengarah pada pemulihan total pasien. Pemantauan efektivitas nutrisi klinis disarankan untuk dilakukan dengan menentukan tingkat galaktosa - 1 - fosfat dalam eritrosit. Dianggap dapat meningkatkan metabolit ini menjadi 3 mg / dl.
Dengan pengangkatan nutrisi terapeutik tepat waktu, prognosisnya menguntungkan. Kasus yang jarang dari sirosis hati dan / atau karsinoma hepatoseluler telah dijelaskan. Indeks intelektual yang rendah dengan gangguan pemikiran abstrak, ucapan dan persepsi visual, hipotonia otot, tremor, ataksia dan keterbelakangan mental juga dapat dicatat. Selain itu, kasus gangguan fungsi reproduksi pada wanita dengan pembentukan hipogonadisme hipergonadotropik dijelaskan.
Gangguan endokrin. Sindrom kolestasis adalah salah satu manifestasi hipotiroidisme atau hipopituitarisme, yang memiliki manifestasi klinis dan laboratorium yang khas. . Tingkat hormon yang relevan rendah menegaskan diagnosis. Gangguan endokrin bawaan berfungsi sebagai indikasi untuk terapi penggantian hormon.
Efek toksik dari obat.Dalam kebanyakan kasus, dengan kolestasis yang disebabkan oleh efek racun dari obat, ada indikasi penggunaan obat yang berpotensi hepatotoksik, yang memiliki nilai tertentu dalam diagnosis. Untuk berpotensi obat hepatotoksik dapat ditugaskan antibiotik tertentu (tetrasiklin, eritromisin, lincomycin, novobiosin, asam klavulanat, ampisilin, kloramfenikol, gentamisin, sefalosporin 1 generasi, tienil), diuretik (Lasix), non-steroid anti-inflamasi (indometetsin), nitrofurans (furagin 5 -Box), obat sulfonylamide, antikonvulsan dan neuroleptik. Pengobatan kerusakan hati toksik meliputi pengecualian obat yang berpotensi hepatotoksik, terapi koleretik dan posindromik.
Nutrisi parenteral panjang penuh. Kolestasis karena nutrisi parenteral penuh yang berkepanjangan (SPT) dapat didiagnosis pada bayi baru lahir yang menerima SPT selama lebih dari 2 minggu dan pada anak yang lebih tua lebih dari 3-4 minggu. Setelah awal nutrisi enteral, penurunan kolestasis adalah karakteristik. Perawatan etiopatogenetik yang paling efektif dalam kasus ini adalah onset nutrisi enteral yang paling awal, serta terapi koleretik.
Hepatitis neonatal idiopatik. Diagnosis hepatitis neonatal idiopatik ditegakkan dengan mengesampingkan semua penyebab sindrom kolestasis yang diketahui dan identifikasi transformasi sel raksasa hepatosit selama pemeriksaan histologis bahan biopsi hati.
Ciri khas penyakit dengan lesi dominan saluran empedu intrahepatik, serta defisiensi a-1-antitripsin adalah kondisi kesehatan pasien yang memuaskan dan tidak adanya perubahan patologis organ dan sistem lain. (tabel 3). Kekurangan α-1-antitrypsin selama bulan pertama kehidupan dimanifestasikan oleh sindrom kolestasis, sedangkan perubahan patologis pada paru-paru berkembang jauh setelahnya, setelah 3-5 tahun kehidupan. Kadar alpha-1-antitrypsin dan alpha-1-globulin serum yang rendah memiliki nilai diagnostik.
Dalam subkelompok ini, sindrom Alagille ditetapkan secara kondisional. Ini ditandai oleh anomali dan / atau malformasi organ lain, tetapi dalam kebanyakan kasus mereka tidak memiliki signifikansi klinis. Diagnosis sindrom Alajille didasarkan pada pengidentifikasian ciri-ciri karakteristik fenotip dan 2 atau lebih kelainan tipikal dan / atau malformasi organ lain:
1. Identifikasi tanda-tanda hipotrofi intrauterin (tingkat pertumbuhan berat badan untuk bayi baru lahir jangka penuh, korespondensi berat saat lahir dengan usia kehamilan selama kelahiran prematur).
2. Identifikasi fitur fenotipik (lebar, dahi yang menonjol, hipoplasia sepertiga tengah wajah, mata yang dalam, dan mata yang terpisah (hypertelorism), hidung lurus panjang dengan penebalan di ujung, dagu menonjol, dermatoglyphics yang menonjol, dll.)
3. ECHO-KG (stenosis perifer atau hipoplasia arteri pulmonalis)
4. Konsultasi dengan Dokter Spesialis Mata (embriotoxon posterior atau anterior)
5. X-ray tulang belakang - proyeksi langsung (membelah tubuh vertebral dalam bentuk kupu-kupu.
Yang kurang umum dengan sindrom ini adalah kelainan pada sistem urin dan organ-organ lain.
Biopsi tusuk hati dilakukan untuk mengkonfirmasi diagnosis, di mana hipoplasia saluran empedu intrahepatik terdeteksi. Tidak ada pengobatan etiopatogenetik untuk sindrom ini. Dengan terbentuknya sirosis dan tidak adanya kelainan jantung atau ginjal, satu-satunya pengobatan radikal adalah transplantasi hati.
PSVH tipe 3
(Kekurangan gen MDR3)
Tidak adanya fosfolipid dalam empedu
PSVH tipe 3 - kolestasis intrahepatik keluarga progresif, gen MDR3 - gen resistensi multi-obat, g. n. - saluran empedu.
Deteksi hipoplasia saluran empedu intrahepatik (dengan tidak adanya tanda-tanda karakteristik sindrom Alagille) menunjukkan bentuk non-sindrom hipoplasia saluran empedu intrahepatik. Deteksi proliferasi saluran empedu membutuhkan retrograde tambahan atau kolangiografi perkutan. Deformitas saluran empedu, terdeteksi oleh kolangiografi dalam kombinasi dengan proliferasi saluran empedu selama pemeriksaan histologis spesimen biopsi hati, memungkinkan diagnosis kolangitis sklerosis perinatal. Tidak adanya perubahan dalam penelitian ini menunjukkan kolestasis intrahepatik familial progresif (PFC) tipe 3, yang dikonfirmasi oleh tidak adanya fosfolipid dalam empedu.
Pengobatan simtomatik sindrom kolestasis
Pengobatan simtomatik ditujukan untuk pencegahan dan pengobatan komplikasi sindrom kolestasis jangka panjang dan sirosis hati yang muncul
Pada semua penyakit yang dimanifestasikan oleh sindrom kolestasis dengan pengecualian atresia saluran empedu ekstrahepatik, kista saluran empedu umum dan gangguan sintesis asam empedu, karena fermentopati, terapi koleretik dengan asam ursodeoksikolat (Ursofalk) diindikasikan. Penggunaan obat koleretik lainnya memiliki keterbatasan pada anak-anak selama bulan-bulan pertama kehidupan, karena banyak dari mereka (choleenisme, flamin dan lain-lain) mengandung empedu sapi kering dan, oleh karena itu, FA primer, formasi yang pada usia ini sudah tinggi. Asam Ursodeoxycholic (UDCA) adalah asam empedu tersier non-toksik (FA), yang biasanya terkandung dalam empedu manusia dalam jumlah kecil (tidak lebih dari 5% dari total kumpulan asam empedu). Ini lebih polar dan hidrofilik daripada LCD lainnya. Properti ini menyebabkan hampir tidak adanya toksisitas senyawa ini, serta aktivitas kolekinetiknya yang tinggi. Rentang efek terapi UDCA mencakup beberapa mekanisme dasar:
1. UDCA membentuk misel campuran dengan FA hidrofobik non-polar, yang secara signifikan mengurangi potensi toksisitasnya dan meningkatkan eksositosisnya dengan mengaktifkan alpha-protein kinase yang bergantung kalsium.
2. UDCA menginduksi koleress yang kaya akan bikarbonat, yang mengarah pada peningkatan aliran empedu dan merangsang ekskresi FA toksik dan bilirubin.
3. Dimer non-polar FA ini tertanam di lapisan dalam membran hepatosit, menstabilkan struktur mereka.
4. UDCA memiliki kemampuan untuk mengurangi penyerapan FA toksik dan lipofilik dan komponen empedu lainnya dalam ileum.
5. UDCA mengurangi ekspresi antigen kompleks histokompatibilitas utama (HLA kelas 1 pada hepatosit dan HLA kelas 2 pada sel epitel saluran empedu), yang menyebabkan aktivasi limfosit T sitotoksik.
Persiapan asam ursodeoxycholic diresepkan pada tingkat 15-20 mg / kg / hari. Dengan efektivitas yang tidak memadai, dosis dapat ditingkatkan menjadi 30 mg / kg / hari. Ketika melakukan pengobatan jangka panjang selama lebih dari 1-2 bulan, dosis pemeliharaan 10 mg / kg / hari digunakan.
Untuk memastikan tingkat pertumbuhan yang normal, anak-anak tersebut membutuhkan peningkatan protein dan beban kalori dibandingkan dengan anak-anak yang sehat, serta konten dalam diet trigliserida rantai menengah (CTL). Dalam hal ini, kondisi penting adalah keseimbangan diet. Ini dapat dicapai dengan menggunakan diet terapi khusus dalam diet. Jika ini tidak mengarah ke efek yang diinginkan, nutrisi dilakukan melalui nutrisi parenteral nasogastrik atau parsial.
Dengan adanya ASI dan tidak adanya kontraindikasi untuk penerimaannya pada anak, perlu untuk meresepkan persiapan enzim (CREON - 1 ribu U / kg / hari) atau menggabungkan ASI dengan campuran terapeutik yang mengandung PTS.
Dengan tidak adanya menyusui, kebutuhan anak-anak untuk bahan makanan utama dapat dicapai dengan menggunakan makanan terapeutik yang mengandung STR atau nutrisi parenteral parsial.
Jumlah CCT yang diperlukan untuk anak-anak dengan sindrom kolestasis (50-60%) terkandung dalam campuran manusia-medis, SCR, serta dalam campuran berdasarkan protein hidrolisat (Pregestimil, Alphare, dll.). Penggunaan yang terakhir ini tidak sepenuhnya dibenarkan dalam kategori pasien ini, karena dalam kebanyakan kasus mereka tidak memiliki gangguan dalam penyerapan protein dan alergi terhadapnya, dan campuran ini memiliki rasa yang secara signifikan lebih buruk dan biaya yang lebih tinggi. Pengalaman kami dengan penggunaan campuran Humana-CTC pada anak-anak dengan penyakit hati progresif kronis menunjukkan tolerabilitasnya yang baik dan peningkatan signifikan dalam status gizi pasien.
Komponen penting nutrisi adalah vitamin yang larut dalam lemak dan elemen pelacak, yang kekurangannya tercatat pada semua pasien dengan sindrom kolestasis yang bertahan lama. Dosis yang disarankan dari vitamin dan elemen yang larut dalam lemak disajikan dalam tabel 6 .
Tabel 6.
dengan sindrom kolestasis.
Nama:
Dosis:
Rute administrasi:
Multiplisitas:
Vitamin D
30.000 - 60.000 IU
* 5.000 - 8.000 IU
1 kali / bulan
1 kali / hari
Vitamin A
25.000 - 50.000 IU
* 5.000-20.000 ME
1 kali / bulan
1 kali / hari
Vitamin E
* 25 IU / kg / hari
peros (tokoferol polietilen glikol 1000 suksinat)
1 kali / 2 minggu.
Vitamin K (vikasol)
1 mg / kg (maks - 10 mg)
1 kali / 1-2 minggu.
1 kali / hari
Seng (seng sulfat)
1 kali / hari
* dengan tidak adanya pemantauan kadar vitamin dalam darah, preferensi harus diberikan pada rute pemberian oral.
** dari perhitungan Ca dasar, rasio Ca / F = 2.
Sebagian besar penyakit hati kronis yang bermanifestasi sebagai sindrom kolestasis disertai dengan pruritus, yang secara signifikan mengganggu kualitas hidup pasien. Ada berbagai metode yang mengurangi rasa gatal. Ini adalah obat dengan mekanisme aksi yang berbeda (cholesteramine, rifampicin, ursofalk, heptral, dll.), Fototerapi, plasmapheresis, dan operasi bilier. Juga digunakan adalah agen yang bertindak pada alat reseptor kulit, seperti minyak mentol, lanolin, mandi air hangat, dll.
Komplikasi sirosis hati adalah hipertensi portal, sindrom hepatorenal dan hepatopulmoner, peritonitis bakteri dan / atau kolangitis, serta ensefalopati hepatik. Pengobatan hipertensi portal termasuk pembatasan garam, penggunaan obat diuretik, penggantian albumin dalam darah, dan dalam kasus yang parah - paracentesis. Vena yang meluas dari kerongkongan dan lambung adalah indikasi untuk pengangkatan H2-blok dan, dalam beberapa kasus, penerapan skleroterapi. Pembentukan sindrom hepatorenal dan hepatopulmonary merupakan indikasi mutlak untuk transplantasi hati. Dengan komplikasi bakteri, terapi antibiotik dilakukan. Munculnya tanda-tanda ensefalopati berfungsi sebagai dasar untuk penunjukan diet rendah protein dan penggunaan persiapan laktulosa (Duphalac, dll.).
Jadi, Kolestasis neonatal adalah salah satu tanda awal dari berbagai penyakit pada hati dan saluran empedu, dan mungkin juga berasal dari ekstrahepatik. Efektivitas pengobatan banyak penyakit herediter dan bawaan dari sistem hepatobiliary tergantung pada waktu onsetnya, dan oleh karena itu menentukan perlunya diagnosis dini mereka. Algoritma diagnosis diferensial menyediakan daftar studi yang optimal yang diperlukan untuk menegakkan diagnosis sesegera mungkin.
Suatu bentuk khusus kolestasis intrahepatik pertama kali dijelaskan pada tahun 1965 oleh Clayton. Hal ini ditandai dengan pelanggaran sekresi bilirubin, asam empedu dan bromsulfalein dan dimanifestasikan oleh perkembangan sirosis hati keluarga secara bertahap, yang menyebabkan kematian. literatur berisi deskripsi dengan nama yang berbeda: penyakit Baylera, yang fatal familial kolestasis intrahepatik, keluarga kolestasis intrahepatik, kolestasis berat familial intrahepatik, sebuah kolestasis intrahepatik fatal, progresif familial kolestasis intrahepatik, progresif familial sirosis kolestasis dengan gangguan metabolisme asam empedu, intrahepatik kolestasis keluarga dengan keterbelakangan mental pengembangan dan pertumbuhan. Dengan dua lusin pengamatan yang tersedia dalam literatur, jika kita secara ketat mengikuti definisi utama Clayton, 11 dari pengamatan kita dapat ditambahkan, 6 kasus lain, tampaknya, juga dapat dikaitkan dengan nosologi ini, meskipun kurangnya sifat kekeluargaan.
Gejala penyakit Byler. Manifestasi klinis kolestasis pada sekitar setengah dari kasus dimulai pada 3 bulan pertama kehidupan, sisa kasus - selama tahun pertama kehidupan. Kolestasis biasanya tidak lengkap. Ikterus dengan intensitas yang bervariasi, seringkali sedang, disertai dengan penggelapan urin dan sebagian oleh tinja yang berwarna merah. Pruritus selalu dini dan sangat parah. Ini mendominasi gambaran klinis dalam intensitas dan efeknya pada kondisi umum, mengganggu tidur. Gatal bervariasi sesekali ketika cholestyramine diberikan, berbeda dengan apa yang diamati dengan kolestasis yang terkait dengan lesi anatomi saluran empedu. Fenobarbital seringkali memiliki efek sedatif terbaik pada gatal. Pembesaran hati, konsistensi padat atau padat, berkembang secara konstan dan cepat.
Munculnya splenomegali menunjukkan manifestasi portal penyakit fibrogenik intrahepatik. Sebagai aturan, tidak ada kelainan pertumbuhan atau kelainan visceral lainnya. Salah satu anak kami menderita rakhitis parah, mudah dihilangkan dengan vitamin D dosis besar. Namun, ada beberapa laporan rakhitis parah, yang tidak terlalu sensitif terhadap vitamin D. Dalam satu kasus rakhitis yang diucapkan, diperlakukan dengan buruk dengan vitamin D2, kami menggunakan turunan hidroksilasi vitamin D. Kekurangan vitamin K dapat menyebabkan manifestasi hemoragik yang parah.
Data laboratorium. Tingkat bilirubin terkonjugasi cukup tinggi. Sampel dengan ekskresi bromsulfalein bersifat patologis, namun, sebagai aturan, kadar kolesterol total dan total lipid mendekati normal, bahkan jika kolestasis telah berlangsung selama beberapa bulan. Disosiasi antara penundaan kolesterol dan lipid dan kandungan bilirubin merupakan karakteristik penyakit ini. Seperti Williams, kami mengamati satu pasien dengan retensi lipid dan xanthoma kulit, dan Linarelli dalam satu kasus mencatat keterlambatan kolesterol sedang. Menurut data retrospektif, beberapa pasien kami tanpa kolesterol dan retensi lipid pada tahun-tahun pertama penyakit kemudian mengembangkan hiperkolesterolemia untuk kedua kalinya. Namun, bahkan kemudian, sifat moderat dari kolesterol dan lipid yang tertunda ini sangat kontras dengan apa yang biasanya diamati dengan kolestasis dari tipe anatomi. Peningkatan aktivitas alkali fosfatase terus diamati, kandungan asam empedu total selalu meningkat tajam.
Sesuai dengan aturan, pada semua pasien yang diamati oleh penulis lain dan kami, durasi kolestasis berfungsi sebagai indikasi laparotomi untuk memeriksa patensi saluran empedu ekstrahepatik. Dalam setiap kasus, pemeriksaan bedah ditentukan oleh peningkatan hati, hijau, dengan permukaan halus atau sudah rumit.
Data histologis. Perubahan histologis tidak spesifik: fibrosis portal umum berkembang sangat dini dengan infiltrasi inflamasi moderat sel mononuklear. Kadang-kadang fibrosis portal dikombinasikan dengan fibrosis intralobular yang nyata, hampir mencapai dan mengeksfoliasi zona sentrolobular. Di tempat-tempat fibrosis portal, sebagai suatu peraturan, ada proliferasi non-tubular, yang membuatnya sulit untuk menilai integritas duktula. Dengan studi histologis berulang, perkembangan bertahap dari fibrosis portal dan intralobular, yang mencerminkan sifat progresif penyakit, dinyatakan.
Perjalanan penyakit ditandai dengan eksaserbasi kolestasis dengan remisi periodik, kurang lebih lengkap. Setiap eksaserbasi sering dipicu oleh infeksi kambuhan, terutama nasofaring. Oleh karena itu, untuk mencegah eksaserbasi kolestasis, kami mengusulkan untuk melakukan adenoidektomi dan tonsilektomi. Eksaserbasi dimanifestasikan terutama oleh kembalinya pruritus, yang seringkali merupakan yang pertama dan untuk waktu yang lama tetap merupakan satu-satunya tanda kolestasis. Tanda-tanda klinis lainnya muncul beberapa minggu kemudian. Eksaserbasi panjang dengan t mungkin dari beberapa minggu hingga 12 bulan. Pada kenyataannya, remisi tidak pernah lengkap, hepatomegali selalu ada. Secara bertahap, remisi menjadi kurang dan kurang diucapkan, hati menjadi keras, tidak merata, nodular, sesuai dengan sirosis bilier. Kematian terjadi karena perdarahan gastrointestinal karena hipertensi portal dekompensasi atau gagal hati progresif pada usia yang berbeda antara 2 dan 15 tahun. Rentang hidup yang panjang (20-25 tahun) juga dijelaskan.
Dalam beberapa pengamatan kami, ada megaspanchenia bilier bersamaan, kolelitiasis, kalsifikasi pankreas, atau gambaran makroskopis pankreatitis kronis, ditemukan pada laparotomi. Namun, biasanya, batu kandung empedu atau pankreas tidak menunjukkan gejala.
Sifat kekeluargaan dari penyakit ini mudah diketahui jika ada lesi pada beberapa anak dari keluarga yang sama atau hubungan darah dengan orang tua, yang merupakan karakteristik dari penularan resesif autosom. Ada juga kemungkinan bentuk sporadis, yang, di hadapan semua manifestasi lainnya, tidak boleh menolak diagnosis penyakit Byler.
Perawatan. Perawatan untuk penyakit Byler sangat terbatas. Cholestyramine lebih atau kurang efektif mempengaruhi gatal, tetapi tidak mencegah proses sirosis progresif. Fenobarbital dapat memiliki efek simptomatik murni: mengurangi gatal dan tingkat hiperbilirubinemia, tetapi tidak mempengaruhi durasi eksaserbasi atau perjalanan penyakit yang jauh. Masih sulit untuk menetapkan manfaat nyata bagi pasien dari kegiatan ini. Kami hanya mencatat bahwa dalam kasus yang dijelaskan oleh Williams, drainase bilier eksternal juga efektif, sedangkan dalam kasus Gray dan Saunders dan kasus Clayton, efeknya kontroversial.
Identifikasi kasus terisolasi tanpa adanya riwayat keluarga, untuk mendapatkan tanda-tanda biokimia penyakit tetap sulit. Beberapa penulis telah menemukan dalam serum asam lipocholic yang abnormal, yang sifat fibrogeniknya telah ditetapkan. Namun, pengamatan ini belum dikonfirmasi, dan sejauh ini tidak ada garam empedu serum abnormal yang ditemukan pada anak-anak dari kelompok ini. Namun, hipotesis metabolisme garam empedu yang abnormal adalah yang paling masuk akal; pekerjaan lebih lanjut diperlukan untuk penentuan biokimia atau enzimatik dari penyakit ini.
Majalah wanita www.
Kembali ke nomor
Kolestasis intrahepatik progresif (penyakit Byler)
Ringkasan
Sindrom penyakit kuning pada anak-anak disebabkan oleh banyak kondisi. Jika hemolitik, parenkim, dan kurang umum pada anak-anak, ikterus mekanis sudah diketahui dengan baik, yang disebut bentuk keluarga (sindrom hiperbilirubinemik fungsional) sering menjadi bagian dari kasus kasuistis. Perlu dicatat bahwa pasien dengan gangguan fungsional metabolisme bilirubin untuk waktu yang cukup lama (menurut beberapa data, dari 6 bulan hingga 3 tahun atau lebih) diamati dengan diagnosa yang keliru pada awalnya. Sementara itu, mengingat penyakit berarti mendiagnosisnya hingga 50%.
Pada anak kecil, diagnosis banding sindrom kolestasis menyebabkan kesulitan tertentu. Berkat penelitian aktif dalam beberapa tahun terakhir penyakit langka jenis ini, hasil yang signifikan telah dicapai dalam memahami esensi dari mekanisme penyakit kuning kolestatik. Peristiwa penting dalam hal ini adalah isolasi penyakit Byler dan penyakit terkait.
Penyakit Byler tidak diragukan lagi merupakan penyakit langka. Namun, ini sangat menarik baik dari sudut pandang klinis maupun patofisiologis. Untuk pertama kalinya pelanggaran ini dideskripsikan pada anak-anak Jacob Byler dan sejak itu dinamai menurut namanya.
Sampai baru-baru ini, konsep "kolestasis intrahepatik keluarga progresif" (PFHR) dan "penyakit Byler" telah diidentifikasi. Hari ini, berkat kemajuan dalam genetika molekuler, ada tiga jenis PFC. Yang pertama adalah penyakit Byler.
Perkembangan PFHD adalah karena pelanggaran yang ditentukan secara genetik dari struktur membran tubular hepatosit. Penyakit ini memiliki mode pewarisan autosom resesif dan mencakup tiga jenis (Tabel 1).
Yang paling banyak dipelajari adalah tipe PSCHV - Penyakit Byler. Dasar dari gangguan ini adalah defisiensi enzim yang terikat membran - ATPase tipe-P, yang memainkan peran penting dalam pengangkutan asam empedu melalui membran tubulus hepatosit. Sebagai akibatnya, asam empedu primer menumpuk di dalam sel hati dan merusaknya.
Pada saat yang sama, asam empedu primer tidak memasuki sistem empedu dan lebih jauh ke dalam usus. Hal ini menyebabkan gangguan penyerapan, termasuk vitamin A, D, E, K. yang larut dalam lemak
Tanda-tanda pertama kolestasis paling sering dicatat sudah pada bayi baru lahir, kurang sering - pada usia 1-10 bulan. hidup. Keunikan dari perubahan laboratorium dalam PSPC tipe I adalah aktivitas rendah gamma-glutamyl transpeptidase (GGTP) dan rendahnya kadar kolesterol darah. Pada saat yang sama, ada peningkatan indeks penanda kolestasis lainnya, termasuk aktivitas alkali fosfatase (alkaline phosphatase), tingkat fraksi langsung bilirubin dan asam empedu.
Enzim GGTP terikat pada membran, dilokalisasi terutama pada sel epitel saluran empedu intrahepatik. Sekresinya terutama dirangsang oleh asam empedu, yang tidak ada dalam sistem empedu intrahepatik dengan penyakit ini. Gen yang bertanggung jawab untuk pengembangan penyakit ini terletak di wilayah lengan panjang kromosom ke-18 (18q21).
Pada PSC tipe II, ekskresi melalui membran tubular dari hepatosit asam chenodeoxycholic sebagian besar terganggu karena tidak adanya P-glikoprotein pada permukaannya. Patogenesis perubahan serupa dengan perubahan PSPC tipe I. Fitur laboratorium juga aktivitas GGTP rendah dan kolesterol serum rendah, peningkatan aktivitas alkali fosfatase. Karena ada pelanggaran terhadap ekskresi hanya satu asam empedu primer, jenis aliran ini kurang parah dibandingkan dengan tipe I.
Tipe II PVC dideskripsikan pada populasi yang terisolasi di Timur Tengah, Greenland dan Swedia. Gen yang bertanggung jawab untuk sintesis P-glikoprotein terlokalisasi pada kromosom 2 (2q24). Struktur molekul gen mirip dengan struktur gen yang bertanggung jawab untuk pengembangan PSPC tipe I.
Di jantung tipe III psvh adalah pelanggaran ekskresi fosfolipid (terutama fosfatidilkolin) melalui membran tubular hepatosit, yang dikaitkan dengan kurangnya MDR-3-P-glikoprotein pada permukaannya.
Biasanya, fosfolipid mengikat asam empedu dalam misel, mencegah efek toksik asam empedu bebas pada sel epitel saluran empedu intrahepatik. Pada tipe III psvh, fosfolipid tidak memasuki sistem empedu intrahepatik. Ini mengarah pada penghancuran saluran di bawah aksi asam empedu. Penghancuran tubulus mengarah pada pengembangan sindrom kolestasis, yang dimanifestasikan oleh peningkatan aktivitas GGTP dan kadar kolesterol serum. Ini adalah perbedaan utama dari jenis FSP I dan II. Gen yang bertanggung jawab untuk pengembangan PSPC tipe III terlokalisasi pada kromosom 7 (7q21.1).
Gejala klinis wajib PSVH adalah penyakit kuning dan gatal. Awalnya, kolestasis (ikterus) diselesaikan secara independen setelah beberapa minggu atau bulan. Kemudian intensitas penyakit kuning meningkat secara bertahap, rasa gatal yang menyakitkan bergabung. Hati dan limpa meningkat secara signifikan. Selain itu, steatorrhea diamati.
Penyakit kuning bersifat intermiten dan berhubungan dengan episode kolestasis berulang. Relaps kolestasis dapat memicu infeksi saluran pernapasan bagian atas. Penyakit kuning disertai dengan penggelapan urin dan tinja ringan. Pasien dengan penyakit Byler memiliki kelainan pertumbuhan, rakhitis, dan diatesis hemoragik.
Pada pemeriksaan histologis pada tahap awal penyakit, hati mempertahankan arsitektonik normal, kemudian muncul pengelompokan kembali hepatosit yang membentuk struktur tubular, saluran pseudo. Kadang-kadang hiperplasia saluran empedu atau pengurangannya terdeteksi. Kolestasis diekspresikan baik di saluran empedu maupun di hepatosit. Perkembangan penyakit mengarah pada pembentukan gambaran klasik sirosis bilier.
Prognosis untuk penyakit ini tidak menguntungkan. Sebagian besar pasien meninggal antara usia 2 dan 15 tahun akibat komplikasi sirosis hati. Namun, masing-masing pasien dengan harapan hidup hingga 25 tahun dijelaskan. Mungkin perkembangan sirosis kanker hati.
Pengobatan penyakit Byler mirip dengan pengobatan sirosis bilier. Pasien biasanya diresepkan pengobatan simtomatik, yang meliputi pencegahan dan koreksi komplikasi sindrom kolestasis. Vitamin A, D, E, K diresepkan untuk mengkompensasi kekurangan endogen. Kalsium glukonat digunakan dalam kombinasi dengan vitamin D. Untuk mengurangi pruritus yang diresepkan: cholestyramine (4-16 g / hari), phenobarbital (5 mg / kg / hari), rifampicin (8-10 mg / kg / hari). Juga digunakan untuk pengobatan obat diuretik (veroshpiron, furosemide) dan dana koleretik.
Salah satu perawatan adalah transplantasi hati. Menurut sejumlah penulis, tindak lanjut pasien dalam 5-10 tahun pertama setelah transplantasi hati menunjukkan bahwa metode ini efektif dan tidak ada kekambuhan penyakit.
Berdasarkan hal di atas, dapat dikatakan bahwa penyakit Byler sebagai penyakit herediter yang jarang menyebabkan kesulitan diagnostik yang cukup besar. Keterlambatan perkembangan anak, kulit yang gatal seringkali menjadi yang utama, dan kadang-kadang merupakan manifestasi klinis pertama. Perjalanan kolestasis yang bergelombang, di mana aktivitas GGTP yang rendah dan kadar kolesterol yang rendah diamati, bersama dengan peningkatan penanda kolestasis lainnya, adalah kriteria diagnostik utama untuk penyakit ini.
Karena terapi simtomatik yang dimulai tepat waktu, kualitas hidup anak meningkat secara signifikan dan durasinya meningkat. Penyebab utama kematian bagi pasien yang tidak menerima pengobatan adalah perdarahan saluran cerna yang disebabkan oleh kekurangan vitamin K. Namun, hal itu dapat dicegah dengan resep obat vitamin K.
Satu-satunya pengobatan radikal untuk penyakit Byler adalah transplantasi hati ortotopik.
Bilirubin adalah turunan dari hemoglobin. Harapan hidup sel darah merah yang mengandung hemoglobin (eritrosit) hanya empat bulan. Kemudian mereka dihancurkan, dan yang baru terbentuk sebagai gantinya. Hemoglobin, yang tidak terkandung di dalam eritrosit, beracun, dan tubuh menghancurkannya. Bagian protein dihilangkan, zat besi diproses dan digunakan untuk membentuk sel darah merah baru, dan residu diubah menjadi bilirubin. Begitu banyak usaha - dan semuanya sia-sia, karena bilirubin masih beracun dan harus dikeluarkan dari tubuh.
Bilirubin adalah zat yang larut dalam lemak dan karenanya tidak dapat dihilangkan dengan urin atau empedu, yang terdiri dari air dan zat yang larut dalam air. Untungnya, hati dapat menggabungkan (konjugat) bilirubin dengan zat lain; bilirubin yang terikat dapat larut dalam air dan dilepaskan bersama dengan empedu. Ini adalah bilirubin yang memberi warna spesifik pada tinja (dan menjelaskan mengapa pada beberapa penyakit hati tinja menjadi putih). Bilirubin terkait dalam usus tidak terserap. Tetapi, di sana, bagian dari bilirubin sekali lagi dibuat larut dalam lemak dan diserap lagi ke dalam darah. Ini disebut sirkulasi enterik-hati bilirubin.
Semua ini terjadi di tubuh anak dan orang dewasa, tetapi tidak pada janin. Janin tidak dapat mengeluarkan bilirubin dengan empedu (tidak membuang air besar di dalam rahim, meskipun ini terjadi saat melahirkan dan menunjukkan kondisi patologis janin), sehingga bilirubin diekskresikan melalui plasenta ke dalam hati ibu. Agar dapat melewati plasenta, bilirubin harus larut dalam lemak. Hati janin tidak dapat mengikat bilirubin, karena kalau tidak bilirubin yang terikat tidak dapat menembus plasenta dan akan tetap berada dalam darah bayi, berakumulasi secara bertahap di sana sampai konsentrasi mematikan.
Dengan persalinan untuk bayi semuanya mengubah paru-paru, sehingga dipenuhi dengan air, sekarang harus menghirup udara. Sebelumnya, ia menulis semua tulisan melalui plasenta, sekarang ia harus makan, mencerna, dan mengasimilasi zat-zat bermanfaat. Ginjal, yang sebelumnya tidak harus menghilangkan zat beracun dari tubuh (cairan ketuban - sebenarnya, urin janin - tidak berbahaya, karena janin minum sama) sekarang perlu mulai menyaring dan mengisolasi mereka. Dan pada saat yang sama, hatinya harus mulai mengikat bilirubin. Bagi sebagian besar bayi yang baru lahir, semua perubahan ini terjadi dengan cepat, pada saat yang sama dan tanpa masalah.
Butuh waktu bagi hati bayi untuk bekerja dengan kapasitas penuh, dan beberapa hari pertama bilirubin menumpuk di dalam tubuhnya, menyebabkan anak menjadi sedikit kuning. Fakta bahwa hati mulai berjalan sangat lambat kemungkinan besar bukan cacat, tetapi, sebaliknya, dikandung oleh alam. Bilirubin dewasa berbahaya, tetapi pada bayi baru lahir ia bertindak sebagai antioksidan. Sedikit kekuningan pada bayi baru lahir sangat membantu. Tapi tidak terlalu kuat; kadar bilirubin yang terlalu tinggi dalam darah dapat menyebabkan kerusakan otak yang serius (bilirubin encephalopathy).
Alam tidak dapat memperkirakan bahwa kami akan memisahkan bayi yang baru lahir dari ibu, menempelkan puting dan botolnya dan membiarkannya menyusui hanya setiap empat jam sekali. Bayi yang tidak menyusu sedikit, buang air besar kurang, sehingga bilirubin yang terkait dalam empedu tetap berada di usus untuk waktu yang lama dan diserap kembali ke dalam darah. Hati tidak mampu mengikat semua bilirubin yang dikembalikan dari usus, dan anak menjadi semakin kuning. Inilah yang disebut "jaundice menyusui", meskipun beberapa percaya bahwa akan lebih tepat untuk menyebutnya "jaundice defisiensi menyusui." Cara terbaik untuk mencegah perkembangannya adalah mulai menyusui dengan benar: menyusui pertama tepat di ruang bersalin, kemudian meninggalkan bayi dengan ibu sepanjang waktu, memberi makan pada permintaan, dan memastikan bahwa perawat dan bidan membantu ibu untuk menyusui di posisi yang tepat.
Karena bilirubin berguna dalam jumlah kecil untuk bayi, ASI mengandung zat yang membantu beberapa bilirubin menjadi lemak yang larut dalam usus. Pada bayi yang diberi susu botol, penyakit kuning fisiologis benar-benar menghilang di suatu tempat dalam waktu satu minggu, sedangkan bayi yang disusui dapat tetap kekuningan selama beberapa minggu, bahkan hingga dua atau tiga bulan. Ini biasanya disebut sebagai "jaundice menyusui." Nama itu bodoh, menyesatkan orang, dan saya percaya bahwa dalam beberapa tahun seseorang di Barat akan berpikir untuk mengubahnya. Tapi sejauh ini saya harus hidup dengan ini.
Beberapa dokter anak yang tidak memiliki pengalaman yang cukup dalam mengamati bayi dengan pemberian ASI normal (mereka jarang sampai baru-baru ini) takut dengan penyakit kuning yang berkepanjangan dan menuntut bayi dianalisis dengan analisis. Ini tidak perlu. Jika bayinya sangat kuning, lakukan tes darah. Jika tingkat bilirubin sangat tinggi (18 mg / dl), masuk akal untuk menunggu beberapa hari dan melakukan analisis lain - periksa apakah bilirubin telah meningkat lebih tinggi lagi. Jika analisis kedua menunjukkan bahwa tingkat bilirubin telah menurun, tidak perlu untuk terus memantau bagaimana kadar bilirubin menurun dari 16 menjadi 13, kemudian ke 11, 8, 5, 7, dan seterusnya. Dan sudah jelas bahwa dia akan terus menurun secara bertahap dan itu akan memakan waktu beberapa minggu.
Hampir sepertiga dari semua bayi icteric yang sehat tetapi tersisa selama lebih dari sebulan adalah sindrom Gilbert - mutasi yang diwariskan pada gen yang memengaruhi pengikatan bilirubin ke hati (ini bukan penyakit, orang-orang dengan sindrom Gilbert hidup sampai berusia seratus tahun). Di masa dewasa, sindrom Gilbert secara berkala dapat menyebabkan penyakit kuning ringan, sering kali bersamaan dengan timbulnya penyakit lain, seperti influenza. Masalahnya adalah ketika ini terjadi, para dokter panik dan mengirim untuk melakukan tes - mereka berpikir bahwa pasien menderita hepatitis. Untuk mengetahui bahwa ini hanyalah sindrom Gilbert dan tidak ada yang perlu dikhawatirkan, bagi seseorang selalu ada rasa lega. Jika Anda tahu ada orang-orang dengan sindrom Gilbert di keluarga Anda (atau Anda tidak tahu, tetapi Anda menebak - katakan, beberapa kerabat terkadang mencurigai penyakit kuning, tetapi dokter tidak menemukan apa-apa), beri tahu dokter anak tentang hal itu.
Karena bilirubin dihilangkan melalui hati, dan tidak dengan urin, minum lebih banyak cairan tidak berguna. Dengan tetesan glukosa, penyakit kuning tidak dapat dicegah atau disembuhkan.
Pada kadar bilirubin yang sangat tinggi dalam darah, fototerapi digunakan. Cahaya dari lampu khusus, jatuh di kulit, menghancurkan bilirubin. Jika semua yang dibutuhkan bayi Anda adalah fototerapi, tidak perlu menempatkannya di unit perawatan intensif neonatal; Lampu fototerapi bergerak dengan mudah dan, jika perlu, dapat dibawa dan dipasang di kamar Anda. Bersikeras bahwa anak diizinkan untuk tinggal bersama Anda. Ini harus disusui sesering mungkin - pertama, untuk mengurangi kadar bilirubin, kedua, akan membutuhkan lebih banyak cairan dari panas lampu (biasanya cukup untuk meningkatkan frekuensi makan, tetapi dalam beberapa kasus mungkin perlu menuangkannya dengan air). Bertahun-tahun yang lalu diyakini bahwa jika bayi baru lahir mulai mengalami kekuningan, ia tidak boleh diberi payudara selama beberapa hari. Beberapa dokter masih menyarankan ini, walaupun sudah terbukti bahwa itu tidak perlu dilakukan. Dalam kasus-kasus di mana penyakit kuning disebabkan oleh penyakit lain atau konflik rhesus, menyusui juga tidak boleh terganggu.
Dalam kasus-kasus langka ketika tingkat bilirubin dalam darah bayi yang baru lahir begitu tinggi sehingga bayi dalam bahaya nyata, ia harus melakukan transfusi darah, sepenuhnya mengganti darahnya sendiri dengan yang baru. Dengan penyakit kuning “normal”, alasannya adalah bahwa bayi tidak menerima susu, dan yang oleh dokter disebut penyakit kuning fisiologis bayi baru lahir (atau paraphysiological, yaitu, kondisi "hampir normal"), ini sangat jarang terjadi. Namun, penyakit kuning dapat memiliki banyak alasan lain: ketidakcocokan dalam golongan darah atau faktor Rh, masalah hati, infeksi, dll. Tergantung pada usia anak dan gejalanya, dokter mungkin ingin melakukan tes yang diperlukan untuk memastikan bahwa tidak ada tidak ada yang serius.
Di zaman kita, fototerapi diresepkan untuk bayi sehat dua-tiga hari hanya jika tingkat bilirubin dalam darah mereka mencapai 20, dan transfusi darah pada 25. Pada masa sebelumnya, fototerapi diresepkan jauh lebih awal, tetapi terbukti bahwa tidak ada kebutuhan nyata untuk itu. Untuk bayi yang sakit atau prematur, penyakit kuning adalah bahaya yang jauh lebih besar, dan karenanya harus mulai mengobatinya lebih awal.
Hari ini di Barat, rumah sakit bersalin dilepaskan sebelum bayi punya waktu untuk menjadi kuning. Periksa warna anak Anda - wajah, kaki, putih mata. Jika beberapa hari kemudian, ketika Anda kembali ke rumah, Anda melihat dengan jelas bahwa anak tersebut telah menjadi lebih kuning, mengunjungi klinik atau kembali ke rumah sakit. Selalu periksa warna kulit Anda di bawah sinar matahari, cahaya dari lampu sering kekuningan dan dapat menyesatkan.
Banyak dokter dan perawat untuk memerangi penyakit kuning disarankan untuk menempatkan bayi di bawah sinar matahari langsung. Ini sebuah kesalahan. Di rumah sakit bersalin, anak-anak disimpan di bawah lampu fototerapi sepanjang waktu (dan hanya ditransfer untuk makan). Tetapi dalam iklim Spanyol kami tanpa krim pelindung (dengan tingkat perlindungan setidaknya 30 unit) Anda tidak dapat meninggalkan bayi di bawah sinar matahari langsung selama lebih dari sepuluh menit. Jika Anda membiarkannya di bawah sinar matahari, tanpa mengolesi tabir surya, selama satu jam penuh, anak akan mendapatkan sengatan matahari yang serius, tetapi ini tidak akan membantunya dengan penyakit kuning, karena terlalu sedikit untuk sekitar satu jam. Jangan memperhatikan saran seperti itu. Anak itu perlu fototerapi (di rumah sakit atau, jika Anda memiliki lampu fototerapi profesional, di rumah), atau tidak (dan, karenanya, Anda tidak perlu meletakkannya di bawah sinar matahari). Yang benar-benar dia butuhkan adalah sering menyusui.
Bilirubin (unit): 1 mg / dl sesuai dengan 17,1 μmol / l.
Laboratorium menentukan berbagai fraksi:
- Total bilirubin (TV).
- Bilirubin (B) yang tidak terkonjugasi.
- Sun: bilirubin terkonjugasi (terkait dengan asam glukuronat).
- [D] -bilirubin: terikat secara kovalen dengan albumin.
- Bilirubin langsung: jumlah bilirubin di- dan mono terkonjugasi + [D] -bilirubin.
- Diagram fraksi bilirubin.
Ikterus fisiologis: dimulai dengan 3 hari kehidupan, berlangsung maksimal 8 hari. Tingkat maksimum bilirubin pada bayi baru lahir cukup bulan tidak melebihi 17 mg / dl.
Penyakit kuning patologis:
- bilirubin darah tali pusat\u003e 6 mg / dL.
- Icterus praecox - tingkat bilirubin dalam 36 jam pertama kehidupan\u003e 12 mg / dl (200 μmol / l).
- Icterus gravis - kadar bilirubin total\u003e 20 mg / dl.
- Icterus prolongatus (ikterus yang berkepanjangan) bertahan setelah 2 minggu kehidupan (\u003e 14 hari).
Penyebab penyakit kuning pada bayi baru lahir
Penyakit kuning pada bayi baru lahir dapat disebabkan oleh berbagai alasan, berdasarkan peningkatan kadar bilirubin yang tidak terkonjugasi atau terkonjugasi. Spektrum kondisi yang mengarah pada pengembangan hiperbilirubinemia terutama disebabkan oleh bilirubin tak terkonjugasi, menurut R.S. Chandra dan J.Th. Stacker, termasuk status berikut.
Peningkatan pembentukan bilirubin tak terkonjugasi:
- penyakit hemolitik pada bayi baru lahir, karena ketidakcocokan faktor Rh, lebih jarang - menurut sistem ABO atau kelompok lain;
- sepsis;
- eritrositopati;
- hemoglobinopati;
- hematoma, trauma kelahiran;
- polisitemia, transfusi ibu-janin atau janin-ibu;
- obat-obatan.
Pelanggaran transportasi bilirubin dalam darah:
- hipoksia;
- asidosis;
- hipoalbuminemia;
- obat-obatan;
- Intralipid.
Gangguan transportasi dan konjugasi bilirubin di hati:
- pengurangan perfusi sinusoidal;
- sindrom Gilbert;
- penyakit kuning dari ASI;
- hipoglikemia;
- hipotiroidisme;
- obstruksi usus tinggi;
- defisiensi glukuronil transferase tipe I dan II;
- obat-obatan.
Gangguan transportasi hati dan usus bilirubin:
- obstruksi usus rendah;
- ileus mekoneal.
Keadaan di mana ada peningkatan kadar bilirubin terkonjugasi adalah sebagai berikut.
Obstruksi ekstrahepatik:
- atresia saluran empedu;
- stenosis saluran empedu;
- sclerosing cholangitis;
- batu;
- tumor;
- colokan lendir / bilier.
Patologi hati:
- hepatitis sel raksasa;
- kurangnya saluran empedu intrahepatik;
- hepatitis sindroma (Alagilya);
- hepatitis non-sindrom;
- sindrom Byler (penyakit hepatoselular progresif dengan kolestasis intrahepatik persisten);
- cacat dalam metabolisme asam empedu (asidemia trihydro-xycoprostanic).
Anomali kongenital:
- fibrosis hati bawaan;
- penyakit caroli.
Kerusakan toksik:
- nutrisi parenteral penuh;
- sepsis;
- endotoksemia.
Penyakit kromosom:
- sindrom Down;
- trisomi 17-18.
Gangguan metabolisme bawaan:
- asam amino: tirosinemia;
- karbohidrat: galaktosemia; fruktosemia; penyakit penyimpanan glikogen, tipe IV;
- lipid: Penyakit Gaucher; Penyakit Niemann-Pick; Penyakit Wolman;
- defisiensi glikolipid, α-antitripsin.
Pelanggaran campuran:
- fibrosis kistik;
- penyakit penyimpanan zat besi neonatal;
- sirosis anak-anak India dengan kandungan tembaga berlebih;
- sindrom serebrohepathorenal Zellweger;
- hipopituitarisme;
- hipotiroidisme.
Infeksi:
- virus: sitomegalovirus; hepatitis B; virus herpes simpleks; Virus Coxsackie; ECHO; reovirus, tipe III; parvovirus, tipe B 19;
- bakteri: TBC; sifilis; listeriosis; yang paling sederhana; toksoplasmosis.
Lesi sistemik:
- sel Langerine (histiocytosis X);
- limfohistiositosis erythrophagic familial.
Lainnya:
- gagal jantung.
Ada beberapa sindrom metabolik bilirubin yang diturunkan. Dengan sindrom Crigler-Nayar dan Gilbert, konjugasi bilirubin dengan perkembangan hiperbilirubinemia tidak terkonjugasi terjadi. Hiperbilirubinemia terkonjugasi terjadi pada sindrom Dabin-Johnson dan Rotor.
Sindrom Crigler - Nayar - penyakit resesif autosomal herediter yang terkait dengan ketiadaan atau defisiensi glukuroniltransferase. Ini dimanifestasikan oleh penyakit kuning pada bayi baru lahir pada hari ke-2 - ke-4 kehidupan. Bergantung pada keparahan fermentopati, dan akibatnya, intensitas hiperbilirubinemia dan prognosis, tipe sindrom I dan II dibedakan. Pada tipe I dari sindrom Kriegler-Nayar, tidak adanya enzim glucuronyltransferase sepenuhnya terjadi. yang menyebabkan peningkatan penyakit kuning yang stabil karena bilirubin tidak langsung dan berakhir dengan kematian selama tahun pertama kehidupan. Hati baik memiliki struktur normal, atau ditandai dengan peningkatan empedu yang ditandai dalam saluran empedu. Perubahan ultrastruktural tidak spesifik. Pada pewarisan dominan autosom tipe II, prognosisnya lebih baik, karena terdapat defisiensi parsial pada enzim glukuronil transferase. Kemungkinan koreksi hiperbilirubinemia fenobarbital dan fototerapi secara medis, diikuti oleh pemulihan enzim.
Sindrom Gilbert adalah penyakit yang ditandai dengan peningkatan kadar bilirubin tidak langsung dan perjalanan tanpa gejala. Penyebab hiperbilirubinemia adalah penurunan penetrasi bilirubin tidak langsung ke dalam hepatosit dan insufisiensi relatif enzim glukuronil transferase. Diagnosis biasanya dibuat pada masa remaja atau usia muda, ketika penyakit bermanifestasi dengan meningkatnya tekanan fisik atau mental, infeksi berulang, puasa.
Sindrom Dabin-Johnson adalah gangguan resesif autosomal, di mana ada kekurangan sekresi bilirubindiglucuronide kanalikuli. Hepatosit di bagian tengah lobulus hati mengandung endapan butiran pigmen coklat keemasan, yang memiliki tanda tinctorial melanin. Namun, mikroskop elektron mengungkapkan bahwa butiran ini bukan melanosom, tetapi memiliki tanda-tanda lisosom.
Sindrom rotor berbeda dari sindrom Dabin-Johnson secara klinis dan morfologis. Hati tidak berubah secara histologis, tetapi mikroskop elektron menunjukkan kanalikuli bilier yang belum matang dan butiran lisosom osmiofil.
Ikterus kolestatik dapat disebabkan oleh gangguan transportasi intrahepatik dan ekstrahepatik serta sekresi empedu. Untuk gangguan intrahepatik, blok mungkin pada tingkat saluran empedu intrahepatik, kolangiol, hepatosit, aparatus sekretori bilier, atau saluran empedu. Dalam beberapa kasus, lokalisasi blok tidak diketahui. Mekanisme kolestasis kanalikuli meliputi ketidakmatangan saluran empedu, kerusakan pada aliran membran dan aktivitas vesikuler, perubahan lipid membran, senyawa, gangguan koneksi antara hepatosit, gangguan komposisi empedu di tubulus, perubahan struktur mikrofilamen aktin dalam tubulus.
Meskipun berbagai penyakit yang terkait dengan hiperbilirubinemia terkonjugasi, yang tercantum di atas, 70% kasus kolestasis pada bayi baru lahir disebabkan oleh hepatitis neonatal atau atresia pada saluran empedu.
Komplikasi penyakit kuning pada bayi baru lahir
Ensefalopati bilirubin dengan bilirubin tak terkonjugasi tingkat tinggi. Ensefalopati bilirubin akut.
Fase awal: lesu, gangguan mengisap.
Fase menengah: tingkat sedang, mudah marah dan hipertensi. Suhu dan tangisan menusuk bergantian dengan kantuk dan hipotensi. Hypertonus dengan tekukan berlebihan pada leher (retrocollis) dan punggung (opisthotonus). Transfusi darah yang diganti (data tunggal) mungkin dapat membantu dalam fase ini. Fase progresif: kemungkinan kerusakan permanen pada sistem saraf pusat, retrocollis berat dan opisthotonus, tangisan yang menusuk, ketidakmampuan untuk mengisap, sleep apnea, demam, pingsan yang dalam, koma, terkadang kejang-kejang dan kematian.
- Ikterus nukleus (kerusakan permanen) dengan kerusakan motorik sentral (dispnea dan athetosis), retardasi mental, gangguan pendengaran, apnea, dan defek email gigi dari sisa gigi.
- Kolestasis dan sirosis hati dengan bilirubin terkonjugasi tingkat tinggi.
Metode untuk mengukur bilirubin
Secara klinis (warna kulit): ikterus terlihat pada tingkat bilirubin sekitar 5 mg / dL dengan kisaran fluktuasi 3-12 mg / dL. Penilaian visual tentang penyakit kuning sangat tergantung pada warna kulit, pencahayaan dan pengalaman dokter, masing-masing, juga tidak dapat diandalkan. Oleh karena itu, seseorang tidak boleh mengabaikan pengukuran kadar bilirubin serum atau pengukuran bilirubin transkutan. Bahkan pada bayi baru lahir dewasa sehat yang disusui tanpa faktor risiko yang jelas, penyakit kuning nuklir dan / atau gangguan pendengaran dapat terjadi.
Perhatian: bahaya hilangnya hiperbilirubinemia, yang membutuhkan terapi, timbul terutama dalam kasus persalinan rawat jalan atau keluar dari rumah sakit bersalin hingga 3 hari hidup. Oleh karena itu, sangat penting bahwa dalam 2 hari berikutnya (maksimum 3), resepsi dokter anak dan pertukaran informasi standar tentang pasien terjadi.
Pengukuran tingkat bilirubin perkutan (indeks bilirubin perkutan (indeks-tcB); perusahaan bilirubinometer Minolta atau Bilicheck):
- bilicheck harus dikalibrasi sebelum setiap pengukuran, ini menunjukkan nilai absolut. Satu pengukuran relatif mahal;
- metode ini hanya berlaku untuk bayi cukup bulan dengan massa\u003e 2500 g, yang belum menerima fototerapi atau transfusi darah pengganti.
- pengukuran harus dilakukan pada dahi atau sternum dengan pengecualian sianosis stagnan dan perwakilan dari ras berwarna;
kesimpulan terapi hanya dilakukan setelah mengukur kadar bilirubin dalam serum. Kontrol laboratorium diperlukan, misalnya, ketika:
- tcB-index\u003e 16 dengan faktor risiko untuk penyakit kuning nuklir;
- tcB-index\u003e 20 dengan tidak adanya faktor risiko untuk penyakit kuning nuklir;
- selalu dalam kasus penyakit kuning rgaesoh (< 24 часов жизни);
- setelah minggu pertama kehidupan untuk menghilangkan kolestasis.
Perhatian: Tingkat bilirubin yang diukur secara transkutan tidak terstandarisasi. Ada perbedaan antar perangkat. Oleh karena itu, untuk setiap perangkat perlu mengetahui batas indeks bilirubin perkutan.
Pengalaman kami: tingkat bilirubin dalam serum maksimum setinggi tingkat perkutan, tidak pernah lebih tinggi.
Metode laboratorium
Fraksi bilirubin (bilirubin total, bilirubin tak terkonjugasi dan terkonjugasi) di banyak klinik diukur dengan menggunakan spektrometri refleksi (Kodak Ektachem). Pada bayi baru lahir dan bayi prematur (karena masalah teknis), apa yang disebut "bilirubin neonatal" (Bing, bilirubin terkonjugasi dan non-terkonjugasi) dapat ditentukan. Karena pada bayi baru lahir bagian utama dari bilirubin biasanya adalah bilirubin yang tidak terkonjugasi, level ini dapat digunakan untuk membuat keputusan terapeutik.
Di banyak tempat, sistem analitik untuk penentuan bilirubin terkonjugasi dan tak terkonjugasi rutin dan darurat tidak dipasang. Dalam hal ini, adalah mungkin untuk menentukan bilirubin total menggunakan pereaksi diazo dan akselerator reaksi (kafein) dan mengukur bilirubin langsung tanpa akselerator. Bilirubin tidak langsung adalah perbedaan dari dua bilirubin ini.
Definisi apa yang disebut "neonatal bilirubin" adalah metode yang sangat sederhana, murah, mungkin dari seluruh darah, tetapi sangat sensitif terhadap gangguan. Indikasi untuk transfusi darah pengganti tidak dapat ditentukan hanya dengan tingkat "bilirubin neonatal."
Bilirubin yang diukur oleh penganalisis gas berkorelasi baik dengan pengukuran biokimia ke tingkat 15 mg / dl (250 μmol / l), dan karena itu, karena volume sampel yang kecil, sangat cocok untuk skrining pada anak-anak icteric.
Perhatian: kolestasis tidak dapat didiagnosis dan dievaluasi menggunakan apa yang disebut. "Neonatal bilirubin".
Diagnosis minimum:
- Golongan darah ibu dan anak, termasuk faktor Rh.
- Reaksi Coombs langsung dan total protein atau albumin pada anak.
- Sejarah keluarga.
- Periksa apakah skrining dilakukan untuk TSH. Kalau tidak, perlu untuk menentukan TSH, T4 gratis, T3.
- Pemeriksaan: hematoma, cephalhematoma, dll.
Perhatian: Jika dicurigai infeksi, lakukan urinalisis.
Diagnosis yang diperluas:
- Alternatif: Sorotan Masyarakat Perawatan Intensif Neonatal dan Pediatrik: Leitlinien GNPI.
- Ikterus yang berkepanjangan (Icterus prolongatus): diduga gangguan metabolisme.
- Kolestasis: bilirubin terkonjugasi menyumbang paling sedikit 10% dari total bilirubin dengan penentuan ganda atau tingkat di atas 2 mg / dl.
Evaluasi kritis hiperbilirubinemia
Bayi baru lahir yang sehat tanpa hemolisis patologis: untuk waktu yang lama telah ada diskusi tentang perbedaan antara penyakit kuning fisiologis dan patologis dan, dengan demikian, batas-batas fototerapi dan transfusi darah yang dapat diganti. Situasi ini telah disederhanakan dalam banyak cara, karena saat ini ada “Ketentuan utama masyarakat kedokteran neonatal dan pediatrik intensif: Leitlinien GNPI, yang sangat dekat dengan rekomendasi dari American Academy of Pediatrics. Rekomendasi didasarkan pada kadar bilirubin total.
Banyak fakta menunjukkan bahwa batasan ini juga dapat diterapkan pada bayi prematur dengan usia kehamilan\u003e 35 minggu, berat badan\u003e 2000 g, dan juga ketidakcocokan ABO.
Ada peningkatan risiko pengembangan penyakit kuning nuklir dengan:
- Hemolisis karena ketidakcocokan Rh.
- Hipoksia, asidosis, hipoalbuminemia, hipoglikemia, hipotermia, sepsis.
- Penggunaan obat-obatan yang memaksa bilirubin tidak berhubungan dengan albumin (misalnya, ceftriaxone, digoxin, lasix, valium, theo-filin, kafein, ibuprofen!).
- Defisiensi glukosa-6-fosfat dehidrogenase dalam kombinasi dengan sindrom Crigler-Najar.
Diagnosis ikterus pada bayi baru lahir
Data klinis dan biokimia tidak selalu memungkinkan untuk membedakan ikterus karena lesi non-obstruktif dari yang karena obstruksi saluran empedu ekstrahepatik. Oleh karena itu, seringkali perlu dilakukan biopsi hati, yang memungkinkan Anda untuk menegakkan diagnosis dengan benar pada 90-95% kasus. Hati bayi yang baru lahir bereaksi terhadap berbagai cedera yang relatif stereotip, dan dengan kolestasis, sebagian besar anak menunjukkan transformasi hepatosit sel raksasa. Pada saat yang sama, hepatosit yang secara signifikan membesar mengandung empat inti atau lebih, memiliki sitoplasma yang heterogen dengan area pucat dan pemadatan (kondensasi) dari bahan tersebut. Di sitoplasma, pigmen empedu, lipofuscin, dan zat besi sering terdeteksi. Transformasi sel raksasa mempengaruhi jumlah sel yang berbeda. Paling sering terdeteksi pada usia 3 bulan, setelah itu frekuensi deteksi transformasi sel raksasa berkurang secara signifikan. Pandangan sebelumnya mengenai spesifisitas diagnostik transformasi sel raksasa hepatosit pada infeksi virus tertentu telah terbukti keliru. Transformasi hypercellular hepatosit sebenarnya diamati pada semua sindrom kolestatik bayi baru lahir, termasuk atresia saluran empedu, hepatitis neonatal, berbagai infeksi, gangguan metabolisme, defisiensi α1 antitripsin, dan sindrom saluran empedu intrahepatik.
Hepatitis neonatal adalah penyakit hati pada bayi baru lahir yang sifatnya tidak diketahui. Ini juga dikenal sebagai kolangiopati obstruktif idiopatik, di mana biasanya termasuk kasus hepatitis neonatal, atresia saluran empedu, dan kista saluran empedu. Hal ini tersirat bahwa kerusakan awal menyebabkan peradangan pada beberapa tingkat sistem hepatobiliary dengan dominasi gangguan hepatoselular, bermanifestasi sebagai hepatitis neonatal, dan dominasi kerusakan saluran empedu ekstrahepatik, bermanifestasi sebagai atresia saluran empedu.
Pencarian intensif untuk agen virus tidak membuahkan hasil, namun, ada asumsi tentang peran reovirus tipe III dalam sindrom hepatitis kolestatik dan atresia saluran empedu.
Secara makroskopis, hati dapat membesar, biasanya dengan permukaan halus dan berwarna hijau gelap. Secara histologis, kolestasis biasanya diamati di dalam hepatosit dan di saluran empedu bagian tengah lobulus hati, jarang di saluran empedu interlobular, dan ada juga transformasi sel raksasa hepatosit. Hepatosit juga mungkin dalam keadaan degenerasi balon, nekrosis asidofilik. Pembentukan struktur pseudo-besi dapat dicatat. Sel-sel mononuklear jarang ditemukan baik di lobulus hati maupun di saluran portal. Erythropoiesis ekstramular biasanya terdeteksi. Area portal, sebagai suatu peraturan, tidak melebar, saluran empedu normal atau dapat dideteksi dengan susah payah. Kadang-kadang, proliferasi moderat dari saluran empedu interlobular diamati. Prognosis penyakitnya baik. Pemulihan biasanya diamati, dan penyakit hati persisten kadang-kadang mungkin terjadi.
Kolestasis familial dikaitkan dengan sejumlah sindrom, yang meliputi sindrom Alagille, sindrom Byler, sindrom kolestasis Norwegia, sindrom kolestasis berulang jinak, dan sindrom kolestasis Indian Amerika Utara. Pada bayi baru lahir dan bayi, sindrom Byler adalah yang paling umum. Jenis warisan adalah resesif autosom. Patologi terbatas pada hati. Manifestasi ekstrahepatik terkait dengan kolestasis. Perubahan patologis dikurangi menjadi hepatitis sel raksasa, yang dalam beberapa kasus dikombinasikan dengan kurangnya saluran empedu intrahepatik. Penyakit ini berkembang dengan cepat menjadi sirosis bilier, pasien jarang hidup sampai dewasa. Mikroskop elektron juga menunjukkan kolestasis dan gangguan mitokondria, yang, bagaimanapun, tidak bersifat patognomonik.
Kolestasis India Amerika Utara, yang pertama kali dijelaskan oleh anggota suku asli Amerika di Quebec barat laut, memanifestasikan dirinya pada minggu-minggu pertama kehidupan. Gambar hepatitis neonatal terjadi di bahan biopsi hati. Mikroskopi elektron menunjukkan penebalan di daerah pericanalicular dengan akumulasi filamen aktin, yang mungkin mengarah pada pelanggaran sekresi empedu. Seiring waktu, penyakit ini berkembang dengan berkembangnya sirosis mikronodular, yang menyebabkan kematian.
Faktor risiko paling signifikan untuk kolestasis pada anak-anak pada nutrisi parenteral penuh adalah prematur dengan usia kehamilan rendah dan berat saat lahir. Insiden penyakit meningkat dengan meningkatnya waktu yang dihabiskan untuk nutrisi parenteral. Jika melebihi 60 hari, risiko kolestasis adalah 80%. Kemungkinan kolestasis juga meningkat dengan adanya patologi saluran pencernaan (necrotizing enterocolitis, gastroschisis) atau reseksi usus. Penanda awal penyakit ini adalah peningkatan kadar asam empedu dalam serum, yang dapat dicatat 5 hari setelah dimulainya nutrisi parenteral. Hiperbilirubinemia biasanya muncul hanya setelah 3-4 minggu sejak dimulainya infus.
Perubahan histologis dalam hati berhubungan dengan kolestasis dengan akumulasi empedu, baik di dalam hepatosit dan di kapiler empedu, yang terutama diucapkan di tengah lobulus hepatik. Disosiasi hemoragik, distrofi balon hepatosit, hiperplasia sel Kupffer dengan adanya lipofuscin juga dicatat. Pada hepatosit, zat besi ditentukan. Transformasi sel raksasa dan pseudoacinar dapat terjadi, dan fokus nekrosis hepatosit tersebar. Erythropoiesis ekstramular dan infiltrasi limfositik sedang atau berat dapat dicatat, kadang-kadang dengan campuran leukosit neutrofilik dan eosinofilik. Proliferasi saluran empedu mungkin sama dengan obstruksi ekstrahepatik. Steatosis jarang terjadi. Mikroskop elektron menunjukkan ekspansi kapiler empedu karena luapan empedu, kehilangan mikrovili, hipertrofi retikulum endoplasma halus yang mengandung bahan padat elektron lemah, serat kolagen di ruang Disse.
Dalam kebanyakan kasus, setelah pemulihan nutrisi enteral, tanda-tanda klinis dan morfologis kolestasis menghilang. Namun, ada kemungkinan berkembangnya sirosis dan gagal hati.
Pada anak-anak dengan displasia bronkopulmonalis, komplikasi lain dari nutrisi parenteral lengkap adalah kolelitiasis karena stasis empedu.
Penyakit kuning neonatal pada penyakit menular. Penyakit radang hati yang bersifat infeksi pada periode neonatal dapat disebabkan oleh virus, bakteri, dan protozoa. Metode infeksi: transplasental, intrapartum, postnatal.
Hepatitis virus pada bayi baru lahir di antara penyebab ikterus neonatal sering terjadi. Virus herpes, virus rubella, cytomegalovirus, dan juga virus hepatitis A dan B adalah yang paling penting.
Infeksi virus herpes biasanya terjadi antara 4 dan 6 hari. Infeksi sering terjadi selama kelahiran dari ibu, yang gejala penyakitnya tidak ada, juga mungkin infeksi transplasenta. Ada hepatomegali dan ikterus, dalam kasus yang parah, DIC berkembang. Gambaran makroskopis kerusakan hati sangat khas - banyak fokus putih dengan diameter 1-2 mm ditentukan. Secara histologis, mereka adalah fokus nekrosis koagulasi, di mana hepatosit mengandung inklusi herpes tipe I dan II. Perubahan hepatosit tipe "inti kosong" lebih sering terjadi. Infeksi dapat dibuktikan secara imunohistokimia.
Infeksi rubella terjadi secara intrauterin. Bayi baru lahir biasanya memiliki berat badan lahir rendah, sering memiliki hepatosplenomegali, penyakit kuning dan trombositopenia, serta kerusakan pada sistem kardiovaskular dan mata. Perubahan histologis di hati mirip dengan manifestasi hepatitis neonatal. Proliferasi saluran empedu dan fibrosis portal dapat dideteksi kemudian.
Dalam kasus infeksi cytomegalovirus, infeksi dapat terjadi melalui rute transplasental, intranatal atau setelah kelahiran melalui sekresi yang terinfeksi, selama transfusi darah atau produk-produknya. Gejala klinis mungkin tidak ada atau memiliki ikterus dan hepatosplenomegali. Dengan infeksi intrauterin awal, berat badan lahir rendah, mikrosefali, kalsifikasi otak, chorioretinitis, dan trombositopenia dicatat. Pemeriksaan histologis hati selain tanda-tanda kolestasis neonatal mengungkapkan karakteristik metamorfosis sitomegalovirus ("sitomegal") dari epitel saluran empedu dan hepatosit yang lebih jarang. Dengan mikroskop elektron dan imunohistokimia, virus dapat diidentifikasi dengan tidak adanya sel sitomegalovirus. Manifestasi klinis kerusakan hati bisa minimal, jarang terjadi hipertensi portal non-sirosis. Ada laporan tentang hubungan infeksi sitomegalovirus dengan atresia saluran empedu, serta kurangnya saluran empedu intrahepatik.
Virus hepatitis A dan B adalah penyebab langka hepatitis neonatal.
Agen penyebab hepatitis A - virus hepatitis A yang mengandung RNA, termasuk dalam kelompok enterovirus. Infeksi terjadi secara enteral, masa inkubasi berlangsung 2 hingga 7 minggu. Virus ini memiliki efek sitolitik pada hepatosit. Anak-anak dari tahun pertama kehidupan tidak sakit dengan hepatitis A, sebagai suatu peraturan. Pada bayi baru lahir, infeksi dapat terjadi melalui transfusi darah, tetapi biasanya tidak menunjukkan gejala.
Penularan hepatitis B terjadi pada trimester ke-3 kehamilan dari ibu dengan hepatitis akut, atau dalam kasus ketika ibu adalah pembawa HBsAg. Pada bayi baru lahir, gejalanya biasanya tidak ada, tetapi mereka menjadi HBsAg positif dan mungkin memiliki kadar transaminase yang sedikit meningkat. Seiring waktu, anak-anak ini dapat mengembangkan hepatitis aktif kronis dengan hasil pada sirosis hati dan pengembangan karsinoma hepatoseluler. Sejumlah kecil pasien dapat mengembangkan hepatitis akut, termasuk bentuknya yang fulminan.
Manifestasi histologis hepatitis virus akut adalah penguraian lobulus dan peradangan hati. Kerusakan hepatosit diwakili oleh balon distrofi dan nekrosis sel-sel individu dengan kehadiran tubuh Cowsilmen asidofilik. Aktivitas regeneratif yang bersamaan dimanifestasikan oleh mitosis dan adanya sel-sel binuklear dan berinti banyak. Infiltrat seluler bersifat mononuklear dan terletak di lobulus dan traktus portal. Daerah portal secara seragam diinfiltrasi dengan limfosit. Sekresi plasma, ceutrofil dan granulosit asidofilik dapat ditemukan. Infiltrat dapat menyebar ke bagian periportal lobulus, tetapi tidak seperti hepatitis aktif kronis, nekrosis periporgal tidak khas dan semua area portal terlibat secara seragam. Ada hiperplasia sel-sel yang melapisi sinusoid, sel-sel Kupffer sarat dengan lipofuscin.
Dalam studi biopsi hati, dimungkinkan untuk mendeteksi penanda tidak langsung dari virus hepatitis B. Ini termasuk hepatosit matte-vitreous, “pasir” inti hepatosit, Caunsilmen calf. Hepatosit Matt-vitreous dengan mikroskop konvensional memiliki penampilan sel besar dengan sitoplasma berbutir halus eosinofilik pucat, dipisahkan dari membran sel dengan pelek ringan, nukleus digeser ke membran sel. Untuk mengidentifikasi sel-sel tersebut, metode pewarnaan trikonik Masson digunakan pada bagian semi-tipis yang tertutup epon dan diwarnai dengan toluidine blue. Dalam sitoplasma hepatosit tersebut, sebagai suatu peraturan, antigen HBsAg dideteksi dengan berbagai metode. Perubahan nuklir yang dijelaskan adalah karakteristik dari antigen HBcAg. Counselor Taurus adalah tubuh apoptosis. Mereka memiliki bentuk formasi bundar dengan sitoplasma eosinofilik homogen, di mana nukleus tidak ada atau sisa-sisanya dilacak. Lokalisasi: balok hati atau lumen sinusoid, di mana mereka dapat difagositosis oleh sel Kupffer. Dapat juga dideteksi pada infeksi mononukleosis, penyakit hati herpes.
Bentuk klinis dan anatomi hepatitis virus berikut dibedakan: siklik akut (ikterik); anicteric; nekrotik (ganas, fulminan); kolestatik dan kolangiolitik; kronis.
Bentuk siklik akut - hati membesar, jaringannya tertutup, merah (hati merah besar). Secara histologis: kebanyakan, pembengkakan, proliferasi sel Kupffer, infiltrasi histiolymphocytic dari saluran portal. Hepatosit utuh atau distrofi granularnya dicatat. Mikroskop elektron mengungkapkan virus dalam sel, peningkatan fungsi sintesis protein hepatosit, hipertrofi dan pembengkakan mitokondria, hipertrofi, dan hiperplasia ribosom. Dengan munculnya jaundice, vakuolar, degenerasi balon hepatosit meningkat dengan hasil pada nekrosis kolejasional atau degenerasi hyalinovacapal dengan hasil dalam koagulasi nekrosis. Badan apoptosis Kaunsilmen, yang terletak di ruang perisinusoidal, diidentifikasi. Nekrosis fokal hepatosit mengarah pada pembentukan nodul Buchner (reaksi makrofag sel-sel Kupffer) dan perkembangan kolapsnya stroma reticular dengan sklerosis berikutnya. Cholestasis, infiltrasi histiolymphocytic dari saluran portal dan lobulus hati limfoid dicatat. Bentuk anicteric - mengubah karakteristik periode preicteric dari bentuk siklik.
Ganas, atau fulminan, bentuknya ditandai oleh nekrosis hati masif. Bentuk kolestatik dan kolangiolitik dimanifestasikan oleh adanya trombus empedu di lumen kapiler empedu dan kolestasis intraseluler, sebagai aturan, kolestasis dikombinasikan dengan kolangiolitis, kolangitis, periholangitis. Infiltrasi lobulus dan traktus portal dengan limfosit dan leukosit polimorfonuklear dicatat.
Bentuk kronis adalah penyakit hati inflamasi yang belum terselesaikan yang berlangsung lebih dari 6 bulan. Biopsi hati diperlukan untuk diagnosis, menentukan indeks aktivitas histologis dan tahap proses. Aktivitas proses ditentukan oleh nekrosis dan distrofi hepatosit, infiltrasi inflamasi, perubahan sinusoid, dan kerusakan saluran empedu. Untuk menilai aktivitas histologis dan tahap (keparahan fibrosis) dari proses, ada beberapa sistem akuntansi. Dengan mempertimbangkan kelangkaan diagnosis hepatitis virus kronis pada anak-anak pada tahun pertama kehidupan, dalam panduan ini, sistem akuntansi peringkat tidak diberikan, mereka tersedia dalam berbagai manual dan monograf tentang penyakit ini.
Hepatitis bakteri, sebagai suatu peraturan, merupakan manifestasi dari sepsis (lebih sering flora oportunistik). Secara histologis membedakan hepatitis bakteri dan bentuk abses difus dengan abses multipel atau mikronodular.
Sifilis bawaan pada bayi baru lahir (sering lahir mati) - daerah abu-abu, dibatasi dengan buruk ditentukan melalui kapsul lobus kanan, yang memiliki semacam jaringan fibrosa padat, putih, dalam sayatan, yang sepenuhnya menggantikan parenkim. Jenis lesi yang lebih sering adalah difus fibrosis interstitial sifilis.
Toksoplasmosis kongenital - pemeriksaan histologis hati menunjukkan stasis bilier, distrofi hepatosit, nekrosis fokal, infiltrat periportal dari limfosit, histiosit, neutrofil, dan eosinofil. Pseudokista atau toksoplasma dapat dideteksi dengan imunofluoresensi.
Ikterus fisiologis pada bayi baru lahir
Ikterus fisiologis tidak terdaftar pada semua bayi baru lahir, tetapi membutuhkan lebih banyak perhatian. Biasanya, karena ketidakmatangan sistem enzim sel-sel hati, karena penguraian sel darah merah yang dipercepat yang mengandung apa yang disebut hemoglobin janin (disintesis secara intrauterin), tingkat bilirubin anak meningkat dalam darah, dan ketika konsentrasi tertentu tercapai, kulit menjadi agak kuning. Kekuningan mulai terlihat pada hari ke 2-3 kehidupan, sementara selaput lendir dan sklera menjadi kuning, tetapi feses dan urin tetap berwarna biasa.
Perubahan warna massa tinja (perubahan warna), urin gelap, dan perkembangan penyakit kuning sejak hari pertama kehidupan, pertumbuhannya kembali setelah periode kekuningan atau hilangnya kekuningan, lamanya retensi penyakit kuning selama lebih dari 10 hari dalam jangka penuh dan 20 hari pada bayi prematur menunjukkan sifat patologis proses tersebut. Gejala-gejala tersebut memerlukan pemeriksaan serius pada anak untuk mengklarifikasi diagnosis.
Pengobatan penyakit kuning pada bayi baru lahir
Bayi baru lahir yang sehat:
Tes Coombs negatif, tidak ada ketidakcocokan grup:
- Dengan tingkat bilirubin transkutan yang meningkat dengan cepat - kontrol kadar bilirubin serum.
- Pada hiperbilirubinemia berat: ulangi tes Coombs.
- Kemungkinan diagnosis lebih lanjut.
Coombs menguji konstelasi positif dan / atau kelompok, ketidakcocokan Rh:
Waspadalah terhadap tes Coombs positif palsu sebagai akibat dari profilaksis anti-B pada usia kehamilan 28 minggu.
Kuning susu ibu:
- "Onset dini": dengan perlekatan yang tidak memadai pada dada dan "menyusu" dengan glukosa
- "Onset lambat": jika kadar bilirubin tinggi, selama 24-48 jam, asi ASI dan beri susu bayi dengan susu formula untuk pemberian makanan buatan. Pada hari ke 3, kadar bilirubin harus menurun secara signifikan, yang berarti terus menyusui. Pastikan untuk meyakinkan ibu tentang perlunya menyusui.
- Hilangkan atresia saluran empedu (peningkatan kadar bilirubin terkonjugasi)!
Perhatian: "Penyakit kuning ASI" adalah diagnosis pengecualian.
Bayi baru lahir yang sakit dan bayi prematur:
Peningkatan risiko dengan gangguan sawar darah-otak, misalnya, dalam asidosis (pH< 7,25), гипотермии, гипопротеинемии (общий белок < 5 г/дл), при неврологической патологии.
Nilai batas pastinya tidak diketahui, semua nilai murni empiris.
Perhatian: pada bayi prematur yang sangat tidak matang, kemungkinan tindakan perlindungan bilirubin sebagai "perangkap radikal" (perlindungan terhadap retinopati prematuritas) dibahas.
Batas-batas untuk transfusi darah yang dapat dipertukarkan pada bayi prematur bahkan lebih kontroversial daripada anak-anak yang sudah dewasa. Jika, terlepas dari fototerapi dengan lampu "biru" dan fototerapi intensif, bilirubin terus meningkat dengan cepat dan melampaui batas fototerapi berikutnya, maka keputusan harus dibuat secara individual.
Kegiatan praktis
Fototerapi (jika mungkin gunakan lampu "biru" dengan panjang gelombang 460 nm):
Jarak lampu anak harus serendah mungkin.
Iradiasi permukaan tubuh yang paling besar (popok kecil atau khusus!).
Mata tertutup (Pelindung Mata RTM dengan jepitan lengket adalah pelindung mata yang andal).
Setiap 3-4 jam untuk mengubah posisi anak untuk iradiasi perut dan punggung (maksimum 12 jam). Bilirubin dapat berdifusi ke bagian permukaan tubuh yang tidak disinari. Jika tidak mungkin mengubah posisi tubuh (misalnya, prematur), maka setelah 4 jam fototerapi, Anda perlu berhenti selama 3-4 jam.
Fototerapi intensif
Iradiasi dari kedua sisi menggunakan "bilirubin mat", misalnya, Biliblanket Plus (Ohmeda) dari bawah, lampu dari atas.
Inkubator (tetapi bukan lampu) membungkus aluminium foil untuk memantulkan cahaya sekitar.
Peningkatan kebutuhan cairan pada bayi prematur dan bayi baru lahir dalam perawatan intensif harus diperhitungkan, untuk memantau suhu konstan dalam inkubator.
Infus protein:
Hanya dengan hipoproteinemia (misalnya, Biseko).
Perhatian: Banyak preparasi albumin manusia dikontraindikasikan, karena stabilisator yang digunakan atau fraksinasi alkohol melanggar kemampuan mengikat albumin dan konstanta ikatan kompleks albumin-bilirubin.
Biseko dalam komposisinya sesuai dengan serum tanpa faktor koagulasi dengan kandungan albumin 5%, sementara itu tidak mengandung zat penstabil.
Fenobarbital:
Sangat kontroversial! Ini diindikasikan untuk ikterus berkepanjangan Ikterus prolongatus (efeknya tidak lebih awal dari setelah 3 hari).
Dosis: 5 mg / kg / hari (jika ibu menerima 100 mg / hari sebelum melahirkan).
Beberapa tahun masih dapat diperdebatkan: memblokir hemoksigenase (SN-mesoporphyrin) dan enzim glukuronisasi (Fluminicol).
Jika orang tua datang:
Hentikan fototerapi, lepaskan penutup mata.
Menyusui diizinkan (menyusui setiap 2 jam). Untuk mengurangi resirkulasi enterohepatik, tinja yang teratur lebih efektif daripada sumbangan glukosa oral saja!
Kontraindikasi untuk fototerapi
Kontraindikasi absolut adalah porfiria eritropoietik bawaan atau indikasi riwayat porfiria pada anggota keluarga. Fotodermatitis berat dengan lepuh dan fotosensitisasi
Penggunaan obat fotosensitisasi.
Efek samping
Sindrom anak perunggu selama fototerapi pada anak-anak dengan kolestasis
- Pewarnaan kulit, serum, dan urin berwarna abu-abu gelap.
- Agaknya: akumulasi porfirin.
- Namun, bukan kontraindikasi terhadap fototerapi, mengurangi efektivitasnya.
Sangat jarang purpura dan perubahan kulit bulosa.
Kehilangan cairan yang meningkat.
Sering buang air besar.
Kontroversial: pelanggaran mekanisme perbaikan DNA dan peningkatan kerapuhan kromosom.
Oksidasi asam lemak dengan kemungkinan pembentukan produk toksik: untuk menutup larutan infus emulsi lemak atau menggunakan sistem infus pelindung cahaya khusus.
Dengan fototerapi berkepanjangan (selama beberapa tahun) dengan sindrom Crigler Naijar, pewarnaan coklat dan atrofi kulit mungkin terjadi.